Clear Sky Science · de
Molekulare Wirkungsweise von NZ2114, einem überlegenen Plectasin‑Derivat
Warum winzige Pilzmoleküle für zukünftige Antibiotika wichtig sind
Da immer mehr bakterielle Infektionen nicht mehr auf unsere besten Antibiotika ansprechen, suchen Forschende nach neuen Wegen, Erreger zu töten, ohne rasch Resistenz zu fördern. Ein vielversprechender Ansatz stammt von kleinen Abwehrmolekülen, die Pilze und Tiere produzieren. Diese Studie untersucht, wie eines dieser Moleküle — eine im Labor veränderte Version des natürlichen Peptids Plectasin namens NZ2114 — gefährliche Bakterien wie Staphylococcus aureus, einschließlich schwer behandelbarer MRSA‑Stämme, bekämpft. Indem die Arbeit seine schrittweise Wirkung an der bakteriellen Zellwand aufdeckt, liefert sie Hinweise für ein intelligenteres Design der nächsten Antibiotikageneration.
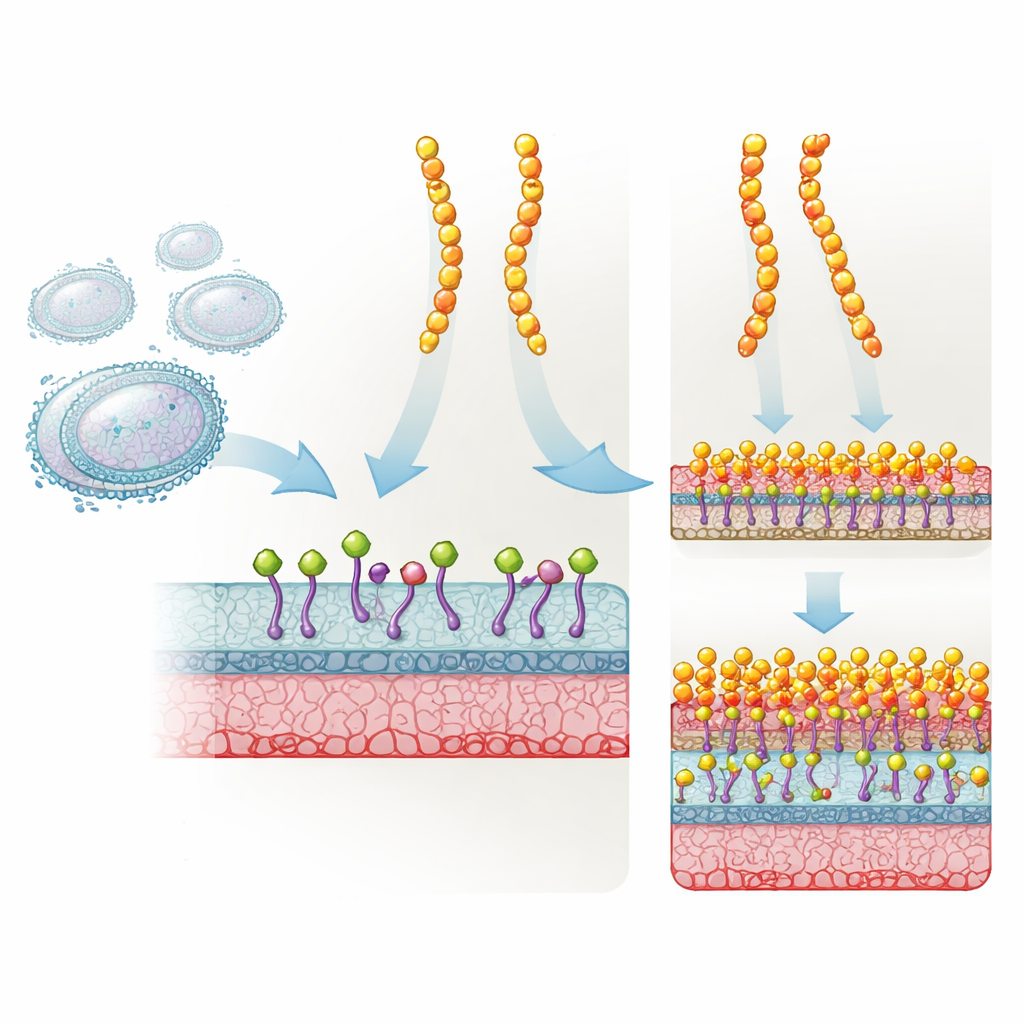
Ein natürlicher Schutzschild als stärkere Waffe
Plectasin ist ein kurzes, robustes Protein, das von einem Pilz gebildet wird und natürlich gegen viele Gram‑positive Bakterien schützt. Es wirkt, indem es an Lipid II bindet, einen entscheidenden Baustein, den Bakterien zum Aufbau ihrer Zellwand verwenden. Wenn Lipid II blockiert ist, kann die Zellwand nicht mehr korrekt gebildet werden, und das Bakterium stirbt schließlich. Wirkstoffentwickler veränderten Plectasin an drei spezifischen Positionen, um NZ2114 zu erzeugen, das in Tiermodellen gegen Staphylokokken und Streptokokken weitaus wirksamer war. Trotz seines Erfolgs und klinischen Interesses war lange unklar, warum dieser Dreifachmutant deutlich besser funktionierte als das Original.
Nicht stärkeres Festhalten, sondern eine andere Art zu halten
Eine einfache Erklärung wäre gewesen, dass NZ2114 möglicherweise stärker an eine „besondere“ Form von Lipid II in Staphylococcus aureus bindet, während Plectasin dieses veränderte Ziel schlecht erkennen würde. Die Autoren prüften diese Idee direkt mit einem Bündel struktureller und Bindungsexperimente. Sie untersuchten, wie beide Peptide mit mehreren Versionen von Lipid II interagieren, einschließlich solcher mit für Staphylokokken typischen chemischen Modifikationen, und maßen die Bindungsstärke in verschiedenen Membrantypen. Überraschenderweise bindeten sowohl Plectasin als auch NZ2114 alle Lipid‑II‑Varianten sehr gut, oft binde Plectasin sogar leicht stärker. Damit ließ sich die Zielerkennung als Hauptgrund für die überlegene Wirkung von NZ2114 ausschließen.
Wie kleine Änderungen Bewegung und Zusammenarbeit umgestalten
Um zu sehen, was sich tatsächlich änderte, nutzte das Team Kernspinresonanz (NMR) und Computersimulationen, um die drei substituierten Aminosäuren in NZ2114 zu untersuchen. Diese Mutationen modifizierten subtil ein Netzwerk von Wasserstoffbrücken in der Nähe einer negativ geladenen Stelle, die Calcium‑ und Magnesiumionen anziehen kann. Das veränderte wiederum die Form und Flexibilität der N‑terminalen Schleife des Peptids und eines angrenzenden Segments, das Lipid II kontaktiert. Festkörper‑NMR und Hochgeschwindigkeits‑Rasterkraftmikroskopie zeigten anschließend, wie sich diese lokalen Änderungen auf einer Membranoberfläche auswirken. Bei niedrigen Calciumspiegeln bildete NZ2114 kleine, hochmobile Cluster in der bakteriellen Membran, während Plectasin bereits in größere, teppichartige Assemblies überging. Bei hohem Calciumgehalt durchlief NZ2114 eine globale Umordnung und schnappte in große, geordnete Teppiche um, die den von Plectasin gebildeten sehr ähnlich waren.
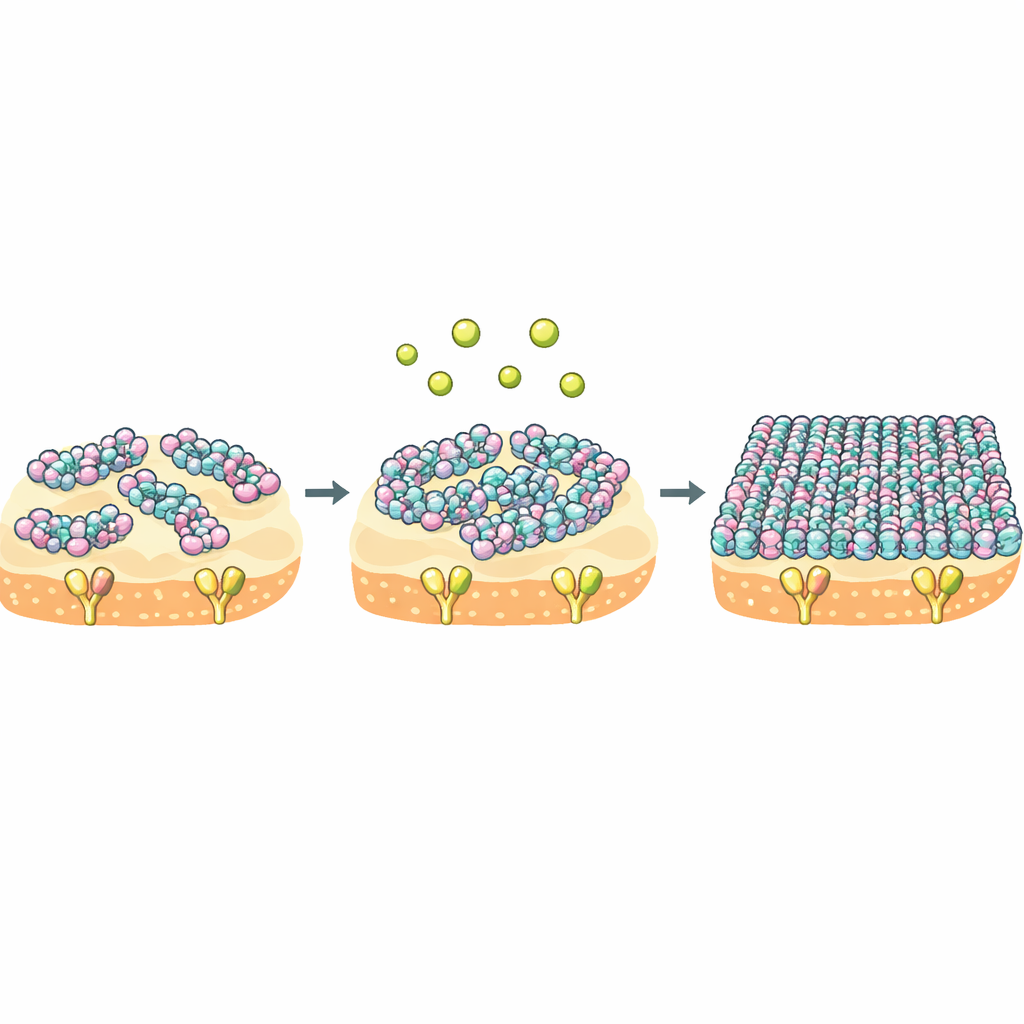
Calcium als Schalter für kollektives Molekülverhalten
Die zentrale Erkenntnis ist, dass NZ2114 und Plectasin dasselbe Ziel teilen, sich aber in ihrem „Verhalten in der Masse“ unterscheiden, sobald sie die Membran erreichen. Für NZ2114 wirkt Calcium als starker Schalter: Es versetzt das Peptid von einem lockeren, dynamischen Zustand in eine starre, hochorganisierte Schicht, die die Membran überzieht und Lipid II lange Zeit einkapselt. Thermodynamische Messungen zeigen, dass NZ2114 beim Binden seines Ziels deutlich weniger Entropiekosten zahlt, das heißt, der gebundene Zustand bleibt mobiler und variabler. Da Bindung und Selbstassemblierung gekoppelt sind, könnte dieses flexible, durch Calcium regulierbare Verhalten es NZ2114 erlauben, seine supramolekulare Struktur an unterschiedliche Umgebungen auf der bakteriellen Oberfläche anzupassen und so seine Wirksamkeit zu erhöhen.
Was das für das Design zukünftiger Antibiotika bedeutet
Die Hauptbotschaft der Studie für Nicht‑Fachleute ist, dass der Vorteil von NZ2114 nicht daher rührt, ein anderes Schloss zu greifen, sondern darin, eine effektivere Gemeinschaft um dasselbe Schlüsselloch zu bilden. Kleine, gezielt platzierte Mutationen veränderten, wie das Peptid auf Calciumionen reagiert und wie es sich mit seinen Nachbarn auf der bakteriellen Membran organisiert. Indem gezeigt wurde, dass Lipid‑II‑Modifikationen in Staphylococcus aureus nicht die Ursache für Plectasins schwächere Leistung sind, lenkt die Arbeit die Aufmerksamkeit auf die Kontrolle von Peptidform, Flexibilität, Ladung und Ionenempfindlichkeit, um kollektives Verhalten zu steuern. Diese Einsichten können das Design neuer peptidbasierter Antibiotika leiten, die für Bakterien schwerer zu umgehen und gegen resistente Stämme wirksamer sind.
Zitation: Derks, M.G.N., Jekhmane, S., Maity, S. et al. Molecular action of NZ2114, a superior plectasin derivative. npj Antimicrob Resist 4, 34 (2026). https://doi.org/10.1038/s44259-026-00196-6
Schlüsselwörter: antimikrobielle Peptide, Lipid II, MRSA, calciumabhängige Antibiotika, supramolekulare Assemblies