Clear Sky Science · fr
Action moléculaire de NZ2114, un dérivé supérieur de la plectasine
Pourquoi de petites molécules fongiques comptent pour les antibiotiques du futur
Alors que de plus en plus d’infections bactériennes cessent de répondre à nos meilleurs antibiotiques, les scientifiques recherchent de nouvelles façons d’éliminer les germes sans provoquer une résistance rapide. Une piste prometteuse provient de petites molécules défensives produites par des champignons et des animaux. Cette étude explore comment l’une de ces molécules, une version optimisée en laboratoire du peptide naturel plectasine appelée NZ2114, combat des bactéries dangereuses comme Staphylococcus aureus, y compris des souches de MRSA difficiles à traiter. En révélant son action étape par étape sur la paroi bactérienne, le travail ouvre la voie à une conception plus intelligente des antibiotiques de prochaine génération.
Un bouclier naturel transformé en arme plus puissante
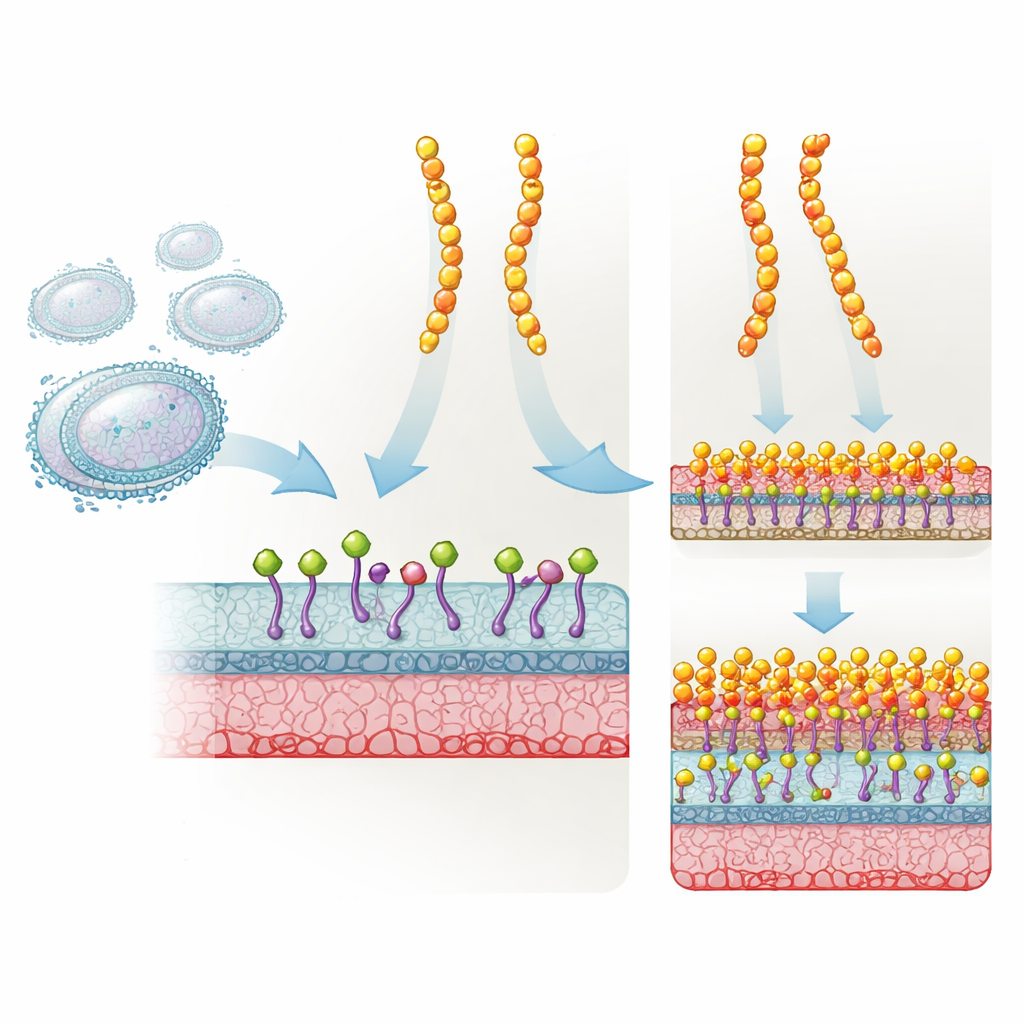
La plectasine est une protéine courte et robuste produite par un champignon qui défend naturellement contre de nombreuses bactéries à Gram positif. Elle agit en s’attachant au Lipid II, un élément de construction crucial que les bactéries utilisent pour fabriquer leur paroi cellulaire. Lorsque le Lipid II est neutralisé, la paroi ne peut plus être correctement synthétisée et la bactérie finit par mourir. Les développeurs de médicaments ont modifié la plectasine en trois positions spécifiques pour créer NZ2114, qui s’est révélée beaucoup plus efficace dans des modèles animaux contre les staphylocoques et les streptocoques. Pourtant, malgré son succès et l’intérêt clinique, on ignorait pourquoi ce triple mutant fonctionnait si nettement mieux que l’original.
Pas une meilleure affinité, mais une façon différente de s’y prendre
Une explication simple était que NZ2114 pourrait s’accrocher plus fortement à une forme « spéciale » de Lipid II trouvée chez Staphylococcus aureus, alors que la plectasine se lierait mal à cette cible modifiée. Les auteurs ont soumis cette idée à un test direct en utilisant une série d’expériences structurales et de liaison. Ils ont examiné comment les deux peptides interagissent avec plusieurs variantes de Lipid II, y compris celles portant des modifications chimiques typiques des staphylocoques, et ont mesuré l’affinité de chaque peptide dans différents types de membranes. Le résultat surprenant fut que plectasine et NZ2114 se liaient très bien à toutes les variantes de Lipid II, souvent avec une affinité légèrement supérieure pour la plectasine. Cela écarte la reconnaissance de la cible comme principale raison de la supériorité létale de NZ2114.
Comment de petites modifications reconfigurent le mouvement et le travail d’équipe
Pour comprendre ce qui avait réellement changé, l’équipe a utilisé la résonance magnétique nucléaire (RMN) et des simulations informatiques pour examiner les trois acides aminés substitués dans NZ2114. Ces mutations ont subtilement reconfiguré un réseau de liaisons hydrogène près d’une zone chargée négativement capable d’attirer des ions calcium et magnésium. Cela a, à son tour, modifié la forme et la flexibilité de la boucle N‑terminale du peptide et d’un segment adjacent qui contacte le Lipid II. La RMN en état solide et la microscopie à force atomique à grande vitesse ont ensuite montré comment ces ajustements locaux se manifestaient à la surface d’une membrane. À faibles concentrations de calcium, NZ2114 formait de petits agrégats très mobiles sur la membrane bactérienne, tandis que la plectasine se répartissait déjà en assemblages plus larges, en nappes. En présence d’un excès de calcium, NZ2114 subissait une réorganisation globale et se transformait en larges nappes ordonnées ressemblant étroitement à celles formées par la plectasine.
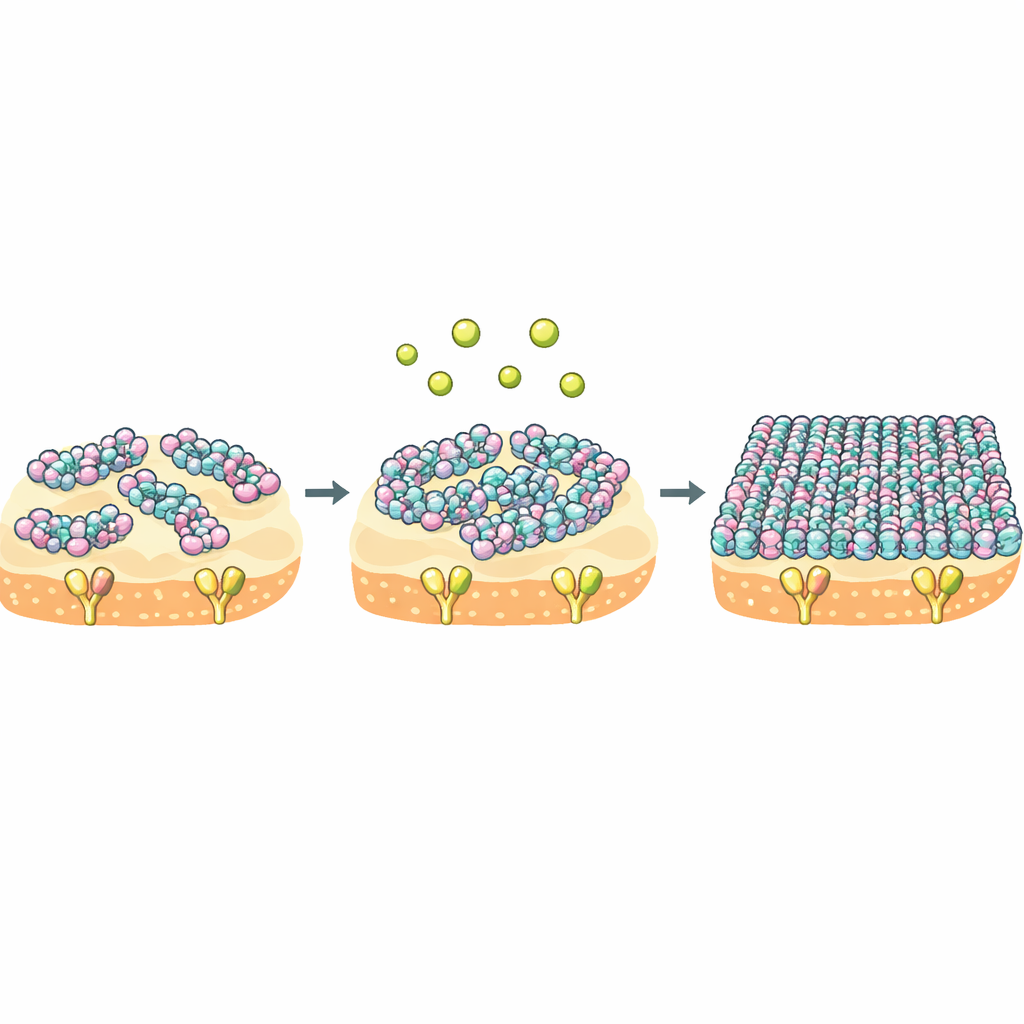
Le calcium comme interrupteur du comportement collectif moléculaire
L’idée centrale est que NZ2114 et la plectasine partagent la même cible mais diffèrent par leur « comportement de foule » une fois qu’ils atteignent la membrane. Pour NZ2114, le calcium agit comme un interrupteur puissant : il fait passer le peptide d’un état lâche et dynamique à une couche rigide et fortement organisée qui recouvre la membrane et emprisonne le Lipid II pendant longtemps. Les mesures thermodynamiques montrent que NZ2114 paie beaucoup moins le coût entropique lors de la liaison à sa cible, ce qui signifie que l’état lié reste plus mobile et variable. Parce que la liaison et l’auto‑assemblage sont couplés, ce comportement flexible mais modulable par le calcium peut permettre à NZ2114 d’adapter sa structure supramoléculaire à différents environnements à la surface bactérienne, augmentant ainsi son efficacité létale.
Ce que cela signifie pour la conception d’antibiotiques futurs
Le message principal de l’étude pour un public non spécialiste est que l’avantage de NZ2114 ne provient pas d’un changement de serrure, mais de la formation d’une foule plus efficace autour de la même serrure. De petites mutations placées avec précision ont modifié la façon dont le peptide répond aux ions calcium et dont il s’organise avec ses voisins sur la membrane bactérienne. En montrant que les modifications du Lipid II chez Staphylococcus aureus ne sont pas responsables de la moindre performance de la plectasine, le travail oriente l’attention vers le contrôle de la forme, de la flexibilité, de la charge et de la sensibilité aux ions des peptides pour ajuster leur comportement collectif. Ces connaissances peuvent guider la conception de nouveaux antibiotiques peptidiques plus difficiles à contourner pour les bactéries et plus puissants contre les souches résistantes.
Citation: Derks, M.G.N., Jekhmane, S., Maity, S. et al. Molecular action of NZ2114, a superior plectasin derivative. npj Antimicrob Resist 4, 34 (2026). https://doi.org/10.1038/s44259-026-00196-6
Mots-clés: peptides antimicrobiens, Lipid II, MRSA, antibiotiques dépendants du calcium, assemblages supramoléculaires