Clear Sky Science · pl
Mechanizm działania molekularnego NZ2114, ulepszonego pochodnego plektasyny
Dlaczego maleńkie molekuły grzybów mają znaczenie dla przyszłych antybiotyków
W miarę jak coraz więcej zakażeń bakteryjnych przestaje odpowiadać na nasze najlepsze antybiotyki, naukowcy poszukują nowych sposobów zabijania zarazków bez wywoływania szybkiej oporności. Jednym z obiecujących tropów są małe cząsteczki obronne wytwarzane przez grzyby i zwierzęta. W badaniu tym analizowano, jak jedna z takich cząsteczek — zmodyfikowana w laboratorium wersja naturalnego peptydu plektasyny, nazwana NZ2114 — zwalcza niebezpieczne bakterie, takie jak Staphylococcus aureus, w tym trudne do leczenia szczepy MRSA. Odkrywając jej krok po kroku działanie na ścianę komórkową bakterii, praca ta wskazuje drogę do mądrzejszego projektowania kolejnej generacji antybiotyków.
Naturalna tarcza przekształcona w silniejszą broń
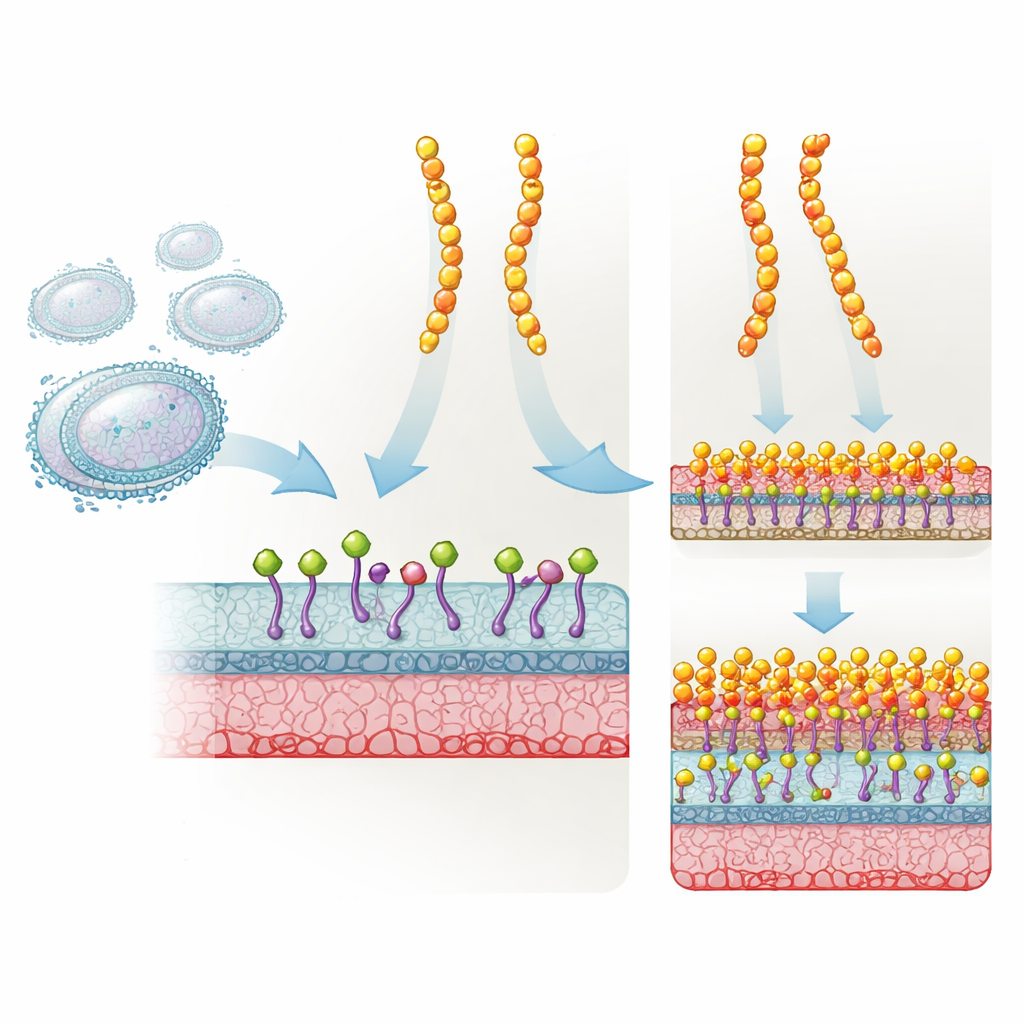
Plektasyna to krótki, stabilny peptyd wytwarzany przez grzyba, który naturalnie broni przed wieloma bakteriami Gram-dodatnimi. Działa, wiążąc Lipid II — kluczowy składnik budulcowy używany przez bakterie do wytwarzania ściany komórkowej. Gdy Lipid II zostaje unieruchomiony, ściana komórkowa nie może być prawidłowo zbudowana i bakteria ostatecznie ginie. Projektanci leków zmodyfikowali plektasynę w trzech konkretnych pozycjach, tworząc NZ2114, który okazał się znacznie skuteczniejszy w modelach zwierzęcych przeciwko gronkowcom i paciorkowcom. Mimo tego sukcesu i zainteresowania klinicznego nikt do tej pory dokładnie nie wiedział, dlaczego ten potrójny mutant działa tak dużo lepiej niż oryginał.
Nie silniejsze ściskanie, lecz inny sposób trzymania
Prostym wytłumaczeniem mogło być to, że NZ2114 przyczepia się mocniej do „specjalnej” formy Lipid II występującej w Staphylococcus aureus, podczas gdy plektasyna wiązałaby się słabo z tym zmienionym celem. Autorzy postawili ten pomysł na bezpośredniej próbie, stosując zestaw eksperymentów strukturalnych i pomiarów wiązania. Zbadali, jak oba peptydy oddziałują z kilkoma wersjami Lipid II, w tym z wariantami zawierającymi modyfikacje chemiczne typowe dla gronkowców, oraz zmierzyli, jak silnie każdy peptyd wiąże się w różnych typach błon. Zaskakujący wynik był taki, że zarówno plektasyna, jak i NZ2114 bardzo dobrze wiązały wszystkie warianty Lipid II, często z nieznaczną przewagą wiązania plektasyny. Wykluczyło to rozpoznanie celu jako główną przyczynę lepszej skuteczności NZ2114.
Jak małe zmiany przekształcają ruch i współpracę
Aby zobaczyć, co naprawdę się zmieniło, zespół użył jądrowego rezonansu magnetycznego (NMR) i symulacji komputerowych, aby przyjrzeć się trzem podstawionym aminokwasom w NZ2114. Te mutacje subtelnie przeorganizowały sieć wiązań wodorowych w pobliżu ujemnie naładowanej plamy, która może przyciągać jony wapnia i magnezu. To z kolei zmieniło kształt i elastyczność pętli N‑terminus oraz sąsiedniego fragmentu kontaktującego Lipid II. Następnie metoda NMR w stanie stałym i szybkiej mikroskopii sił atomowych ujawniły, jak te lokalne poprawki ujawniają się na powierzchni błony. Przy niskim stężeniu wapnia NZ2114 tworzył małe, wysoce ruchome klastry na błonie bakteryjnej, podczas gdy plektasyna już rozpraszała się w większe, dywanopodobne zespoły. Gdy wapnia było dużo, NZ2114 przeszedł globalną przemianę i złożył się w duże, uporządkowane dywany bardzo podobne do tych tworzonych przez plektasynę.
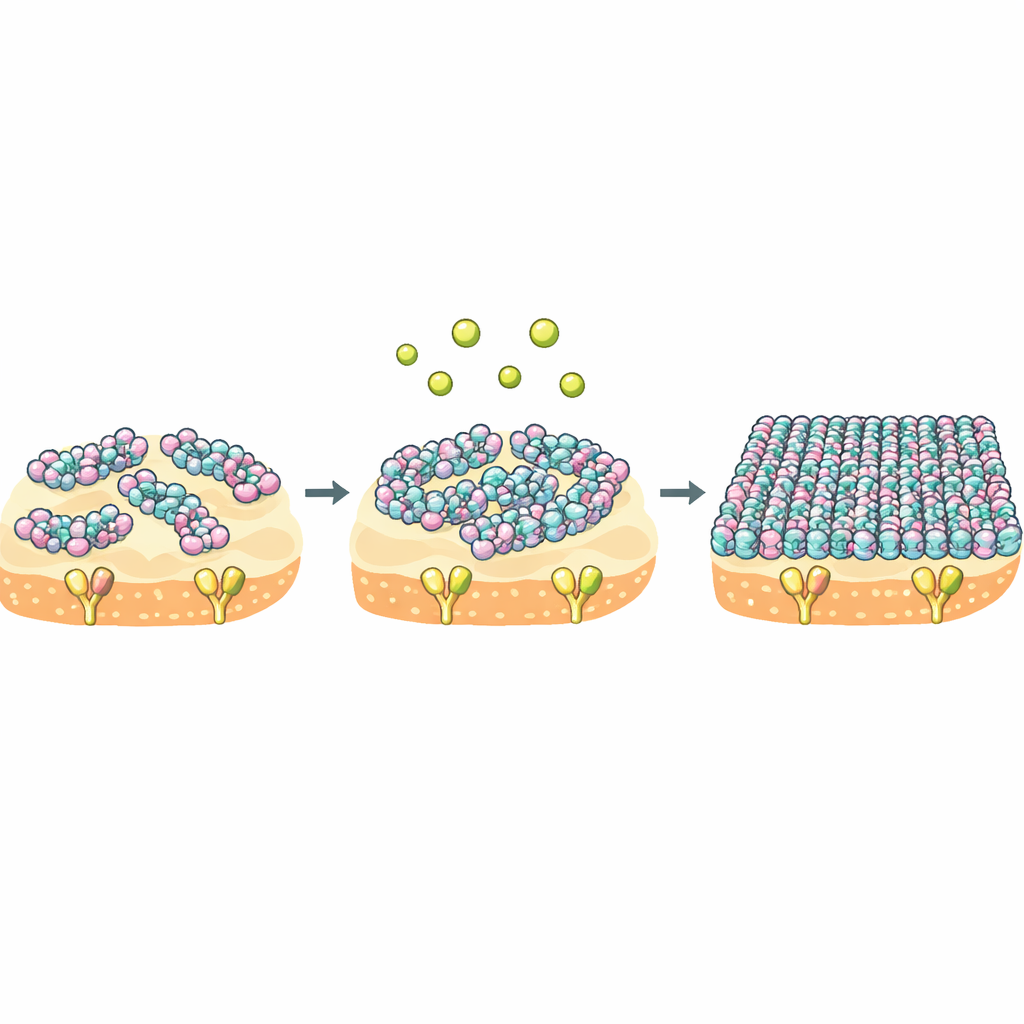
Wapń jako przełącznik zachowań molekularnego tłumu
Główna obserwacja jest taka, że NZ2114 i plektasyna mają ten sam cel, ale różnią się „zachowaniem tłumu”, gdy dotrą do błony. Dla NZ2114 wapń działa jak silny przełącznik: przesuwa peptyd ze stanu luźnego i dynamicznego w stan sztywny, wysoko zorganizowaną warstwę, która pokrywa błonę i długotrwale unieruchamia Lipid II. Pomiary termodynamiczne pokazują, że NZ2114 płaci znacznie mniejszy koszt entropii przy wiązaniu celu, co oznacza, że stan związany pozostaje bardziej ruchomy i zróżnicowany. Ponieważ wiązanie i samoorganizacja są sprzężone, to elastyczne, a jednocześnie regulowane przez wapń zachowanie może pozwalać NZ2114 dostosować swoją strukturę supramolekularną do różnych środowisk na powierzchni bakterii, zwiększając w ten sposób jego efektywność zabijania.
Co to oznacza dla projektowania przyszłych antybiotyków
Główne przesłanie badania dla odbiorców nie‑specjalistów jest takie, że przewaga NZ2114 nie wynika z chwycenia innego zamka, lecz z utworzenia skuteczniejszego tłumu wokół tego samego zamka. Małe, precyzyjnie umieszczone mutacje zmieniły sposób, w jaki peptyd reaguje na jony wapnia oraz jak organizuje się z sąsiadami na błonie bakteryjnej. Pokazując, że modyfikacje Lipid II w Staphylococcus aureus nie tłumaczą słabszej wydajności plektasyny, praca kieruje uwagę ku kontrolowaniu kształtu peptydu, jego elastyczności, ładunku i wrażliwości na jony, aby stroić zachowanie zbiorowe. Te wnioski mogą naprowadzić projektowanie nowych antybiotyków opartych na peptydach, które będą trudniejsze do ominięcia przez bakterie i skuteczniejsze wobec szczepów opornych.
Cytowanie: Derks, M.G.N., Jekhmane, S., Maity, S. et al. Molecular action of NZ2114, a superior plectasin derivative. npj Antimicrob Resist 4, 34 (2026). https://doi.org/10.1038/s44259-026-00196-6
Słowa kluczowe: peptydy przeciwdrobnoustrojowe, Lipid II, MRSA, antybiotyki zależne od wapnia, zespoły supramolekularne