Clear Sky Science · nl
Moleculaire werking van NZ2114, een superieure plectasin‑derivaat
Waarom kleine schimmelmoleculen ertoe doen voor toekomstige antibiotica
Naarmate meer bacteriële infecties niet meer reageren op onze beste antibiotica, zoeken wetenschappers naar nieuwe manieren om ziekteverwekkers te doden zonder snelle resistentie te veroorzaken. Een veelbelovende vondst komt van kleine verdedigingsmoleculen die door schimmels en dieren worden gemaakt. Deze studie onderzoekt hoe één van die moleculen, een in het laboratorium bijgestelde versie van het natuurlijke peptide plectasin genaamd NZ2114, gevaarlijke bacteriën zoals Staphylococcus aureus bestrijdt, inclusief moeilijk te behandelen MRSA‑stammen. Door de stap‑voor‑stap werking op de bacteriële celwand bloot te leggen, wijst het werk de weg naar slimmer ontworpen volgende‑generatie antibiotica.
Een natuurlijke schild veranderd in een sterker wapen
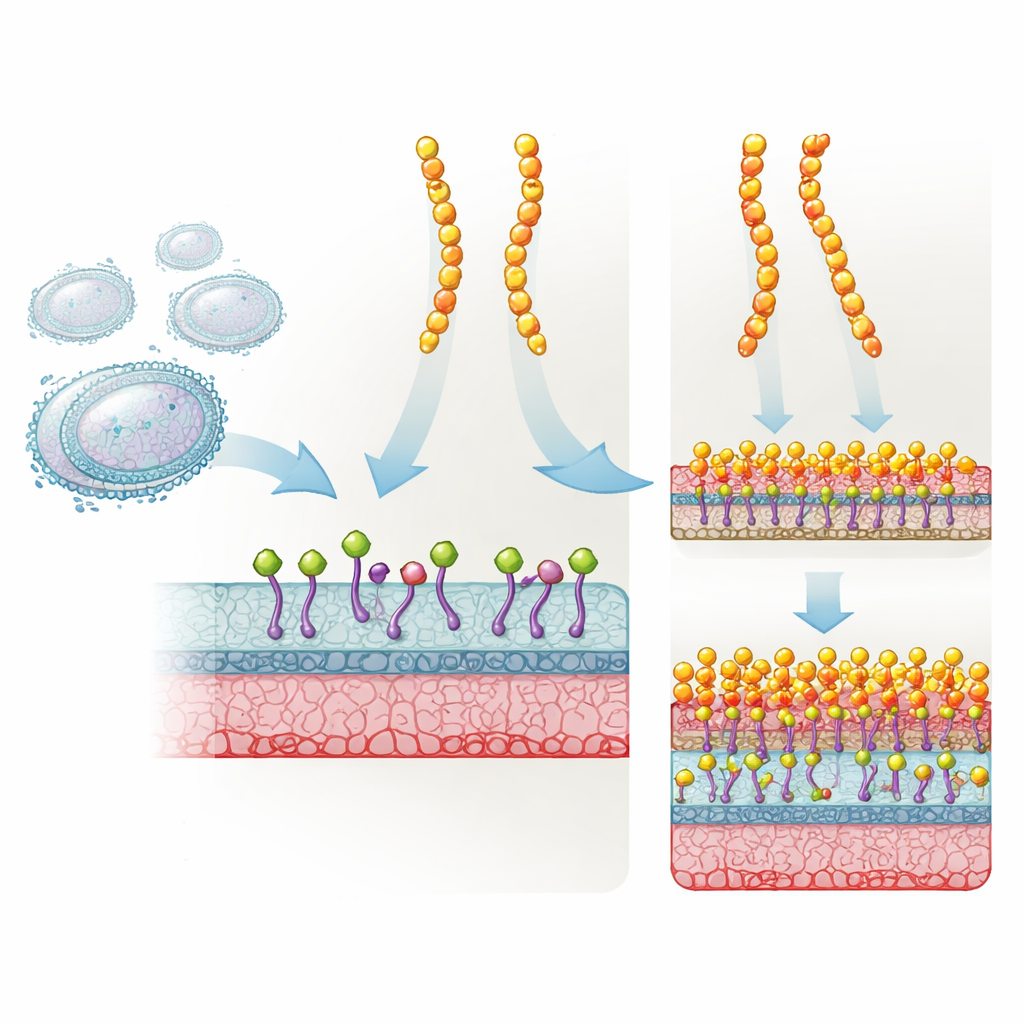
Plectasin is een kort, robuust eiwit gemaakt door een schimmel die van nature beschermt tegen veel Gram‑positieve bacteriën. Het werkt door Lipid II vast te houden, een cruciale bouwsteen die bacteriën gebruiken om hun celwand te maken. Wanneer Lipid II wordt geblokkeerd, kan de celwand niet goed worden opgebouwd en sterft de bacterie uiteindelijk. Geneesmiddelontwikkelaars hebben plectasin op drie specifieke posities aangepast om NZ2114 te creëren, dat veel effectiever bleek in diermodellen tegen stafylokokken en streptokokken. Ondanks het succes en de klinische belangstelling was het echter onduidelijk waarom deze drievoudige mutatie zoveel beter presteerde dan het origineel.
Niet strakker vasthouden, maar een andere manier van vasthouden
Een eenvoudige verklaring was dat NZ2114 mogelijk sterker hecht aan een "speciale" vorm van Lipid II die in Staphylococcus aureus voorkomt, terwijl plectasin slecht zou binden aan dit gewijzigde doelwit. De auteurs testten deze hypothese rechtstreeks met een reeks structurele en bindingsonderzoeken. Ze onderzochten hoe beide peptiden interageren met meerdere versies van Lipid II, inclusief die met chemische aanpassingen typisch voor stafylokokken, en maten hoe sterk elk peptide in verschillende soorten membranen bond. Het verrassende resultaat was dat zowel plectasin als NZ2114 alle Lipid II‑varianten zeer goed binden, vaak waarbij plectasin iets strakker bond. Dit sluit herkenning van het doelwit uit als de belangrijkste reden voor NZ2114's superieure dodingsefficiëntie.
Hoe kleine veranderingen beweging en samenwerking hervormen
Om te zien wat er daadwerkelijk veranderd was, gebruikte het team kernspinresonantie (NMR) en computersimulaties om naar de drie vervangen aminozuren in NZ2114 te kijken. Deze mutaties herschakelden subtiel een netwerk van waterstofbruggen nabij een negatief geladen plek die calcium‑ en magnesiumionen kan aantrekken. Dat wijzigde op zijn beurt de vorm en flexibiliteit van de N‑terminale lus van het peptide en een nabijgelegen segment dat contact maakt met Lipid II. Solid‑state NMR en hogesnelheids‑atoomkrachtmicroscopie toonden vervolgens hoe deze lokale aanpassingen zich op het membraanoppervlak manifesteerden. Bij lage calciumspiegels vormde NZ2114 kleine, zeer mobiele clusters op het bacteriële membraan, terwijl plectasin al in grotere, kleedachtige assemblages verspreid was. Wanneer calcium overvloedig aanwezig was, onderging NZ2114 een globale herschikking en klapte het om in grote, geordende kleedlagen die sterk leken op die van plectasin.
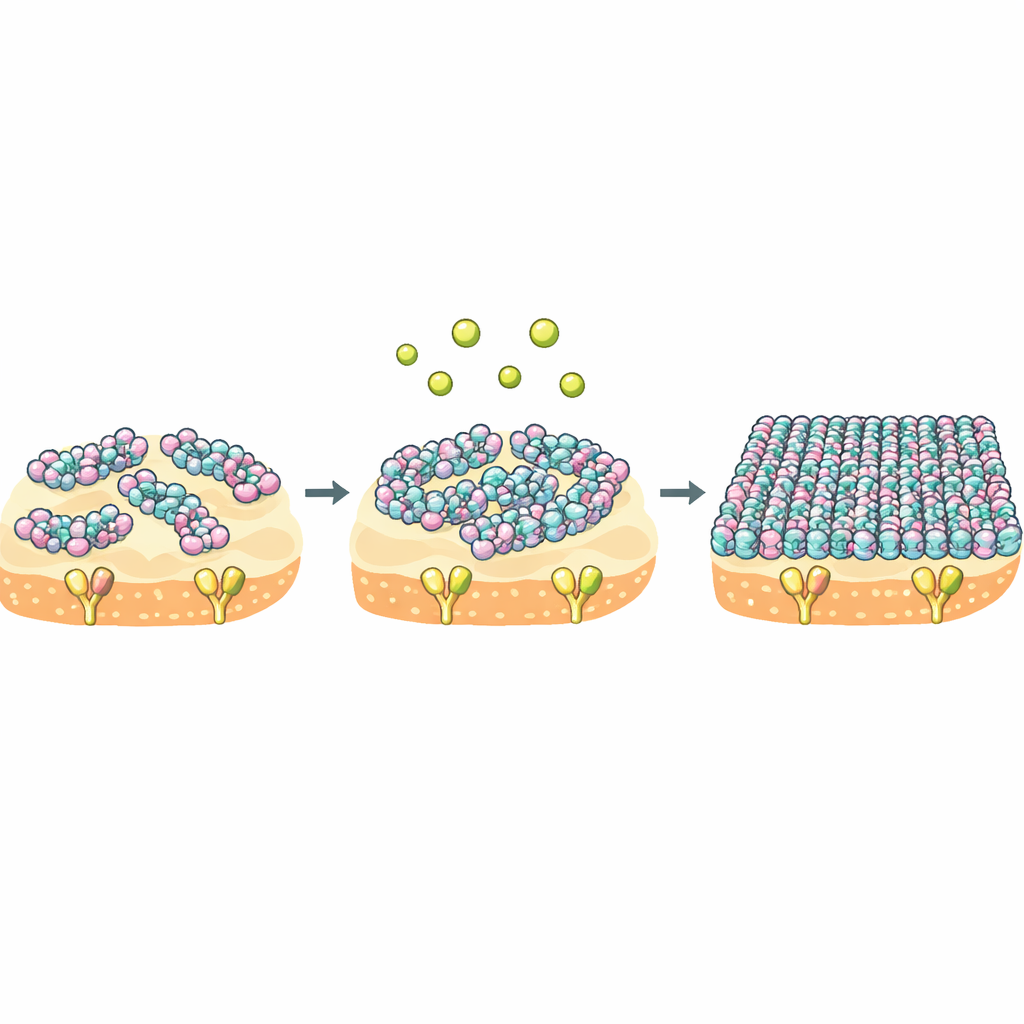
Calcium als schakel voor groepsgedrag van moleculen
De kerninzichten zijn dat NZ2114 en plectasin hetzelfde doel delen maar verschillen in hun "groepsgedrag" zodra ze het membraan bereiken. Voor NZ2114 fungeert calcium als een krachtige schakel: het verschuift het peptide van een losse, dynamische toestand naar een stijf, sterk georganiseerd deken dat het membraan bedekt en Lipid II lange tijd opsluit. Thermodynamische metingen tonen aan dat NZ2114 veel minder entropiekosten betaalt bij het binden van zijn doel, wat betekent dat de gebonden toestand mobieler en gevarieerder blijft. Omdat binden en zelfassemblage gekoppeld zijn, kan dit flexibele maar calcium‑afstelbare gedrag NZ2114 in staat stellen zijn supramoleculaire structuur aan te passen aan verschillende omgevingen op het bacteriële oppervlak, waardoor de dodefficiëntie toeneemt.
Wat dit betekent voor toekomstig antibioticumontwerp
De belangrijkste boodschap van de studie voor niet‑specialisten is dat NZ2114's voordeel niet voortkomt uit het grijpen van een ander slot, maar uit het vormen van een effectievere menigte rond hetzelfde sleutelgat. Kleine, nauwkeurig geplaatste mutaties veranderden hoe het peptide reageert op calciumionen en hoe het zich ordent met zijn buren op het bacteriële membraan. Door aan te tonen dat Lipid II‑modificaties in Staphylococcus aureus niet de oorzaak zijn van plectasin's zwakkere prestatie, verlegt het werk de aandacht naar het beheersen van peptidevorm, flexibiliteit, lading en ionsensitiviteit om collectief gedrag te sturen. Deze inzichten kunnen het ontwerp begeleiden van nieuwe peptidegebaseerde antibiotica die moeilijker voor bacteriën te ontwijken zijn en krachtiger tegen resistente stammen.
Bronvermelding: Derks, M.G.N., Jekhmane, S., Maity, S. et al. Molecular action of NZ2114, a superior plectasin derivative. npj Antimicrob Resist 4, 34 (2026). https://doi.org/10.1038/s44259-026-00196-6
Trefwoorden: antimicrobiële peptiden, Lipid II, MRSA, calcium‑afhankelijke antibiotica, supramoleculaire assemblages