Clear Sky Science · zh
感染噬菌体T4期间选择孔蛋白和LPS突变体促进大肠杆菌对β-内酰胺类抗生素耐药性的出现
这对日常医学为何重要
面对难以根除的细菌引发的感染,医生的可用治疗选项日益减少,诸如使用攻击细菌的病毒(称为噬菌体)等新思路正受到关注。本研究提出了一个简单但关键的问题:当我们用噬菌体对抗细菌时,是否可能无意中让这些细菌更容易获得对抗生素的耐药性,特别是那些常作为最后手段使用的强效药物如碳青霉烯类?
细菌的外部盔甲
许多成问题的细菌,包括大肠杆菌,包裹在坚固的外层中。该外层含有微小通道或孔,可让营养物质进入,也允许许多抗生素渗入。它还携带称为脂多糖(LPS)的糖脂分子,形成致密屏障。孔和LPS层对细菌生存至关重要——但它们同时也是噬菌体附着的靶点。由于相同的外部结构既用于引入抗生素,也被噬菌体利用,任何能保护细菌免受一种威胁的改变,都可能影响它们对另一种威胁的反应。
塑造细菌防御的病毒
研究人员以一种著名的实验室大肠杆菌菌株和一种经典噬菌体T4为研究对象。该噬菌体需要特定的孔(称为OmpC)和内层LPS核心的部分来附着并启动感染。通过在不同条件下用该噬菌体暴露大量细菌,并对幸存者进行基因组测序,团队发现对噬菌体的抗性几乎总是涉及孔、内层LPS核心或两者的变化。有时还会出现调控孔表达的系统被改变的情况。所有这些情形的最终结果都是外层被重塑,使噬菌体不再容易附着。
当对病毒的抗性为药物耐药铺路
接着,团队考察了这些噬菌体抗性细菌在暴露于抗生素时的表现。单独看,大多数阻断噬菌体的突变并不会使细菌对重要的β-内酰胺类抗生素(如碳青霉烯类或先进的头孢类)产生强耐药性。但当细菌携带常见的β-内酰胺酶基因——即可分解β-内酰胺抗生素的酶——时,情况有所不同。在受噬菌体选择产生的突变体中,有一小部分但重要的株系,既有受损的OmpC孔又有严重改变的内层LPS核心,显示出对美罗培南、头孢吡肟和厄他培南等药物的生存能力明显提高。这些水平仍低于完全的临床耐药,但明显高于携带相同酶的原始菌株。
从头重建机制
为确认这并非偶然,科学家们精确构建了在孔基因和选定LPS核心基因上有定义缺失的细菌突变体,然后在有无β-内酰胺酶的背景下测量碳青霉烯类的效果。他们证实,失去OmpC孔同时破坏关键的内层LPS基因,足以复制噬菌体暴露后观察到的耐药模式。影响关键的是内层核心而不是外层装饰。作者认为,这些内层核心缺陷可能扰乱剩余孔的组装或功能,并触发细胞包膜的应激反应,共同降低外膜对抗生素的整体通透性。
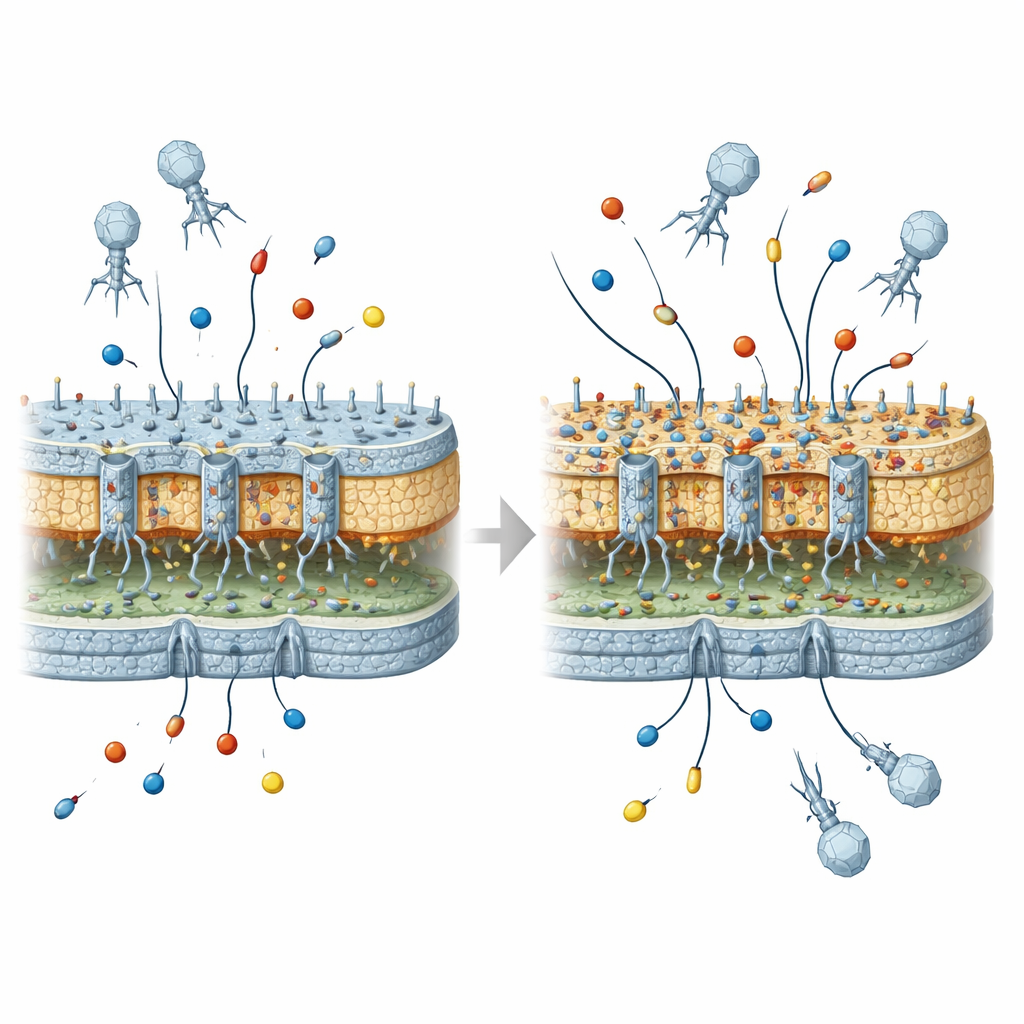
这对未来噬菌体治疗的意义
对非专业读者而言,核心信息是:用于杀灭细菌的噬菌体可能无意间重塑细菌的外层盔甲,使其在将来更能抵御某些抗生素——前提是它们随后获得了合适的耐药酶。噬菌体选择的改变本身并不会产生高度耐药的菌株,但会创造一种“容许性”背景,能将有限的耐药基因放大为更严重的临床问题。随着噬菌体疗法逐步进入常规医疗实践,这项工作提示我们必须谨慎权衡这些进化副作用,设计既能治愈感染又能将帮助细菌迈向抗生素耐药下一步的风险降到最低的噬菌体治疗方案。
引用: Le-Boulch, J., Charneau, E., Chevallereau, A. et al. Selection of porin and LPS mutants during infection by phage T4 facilitates the emergence of β-lactam resistance in Escherichia coli. npj Antimicrob Resist 4, 21 (2026). https://doi.org/10.1038/s44259-026-00193-9
关键词: 噬菌体治疗, 抗生素耐药, 大肠杆菌, β-内酰胺酶, 细菌外膜