Clear Sky Science · pl
Selekcja mutantów porin i LPS podczas infekcji bakteriofagiem T4 ułatwia pojawienie się oporności na β-laktamy w Escherichia coli
Dlaczego ma to znaczenie dla medycyny codziennej
Lekarze kończą się opcje leczenia zakażeń wywołanych przez trudne do zwalczenia bakterie, a nowe pomysły, takie jak użycie wirusów atakujących bakterie — zwanych fagami — zyskują na znaczeniu. To badanie stawia proste, lecz kluczowe pytanie: czy stosując takie wirusy do walki z bakteriami, przypadkowo nie ułatwiamy tym bakteriom rozwoju oporności na antybiotyki, zwłaszcza na silne leki jak karbapenemy, często stosowane jako ostateczność?
Zewnętrzna zbroja bakterii
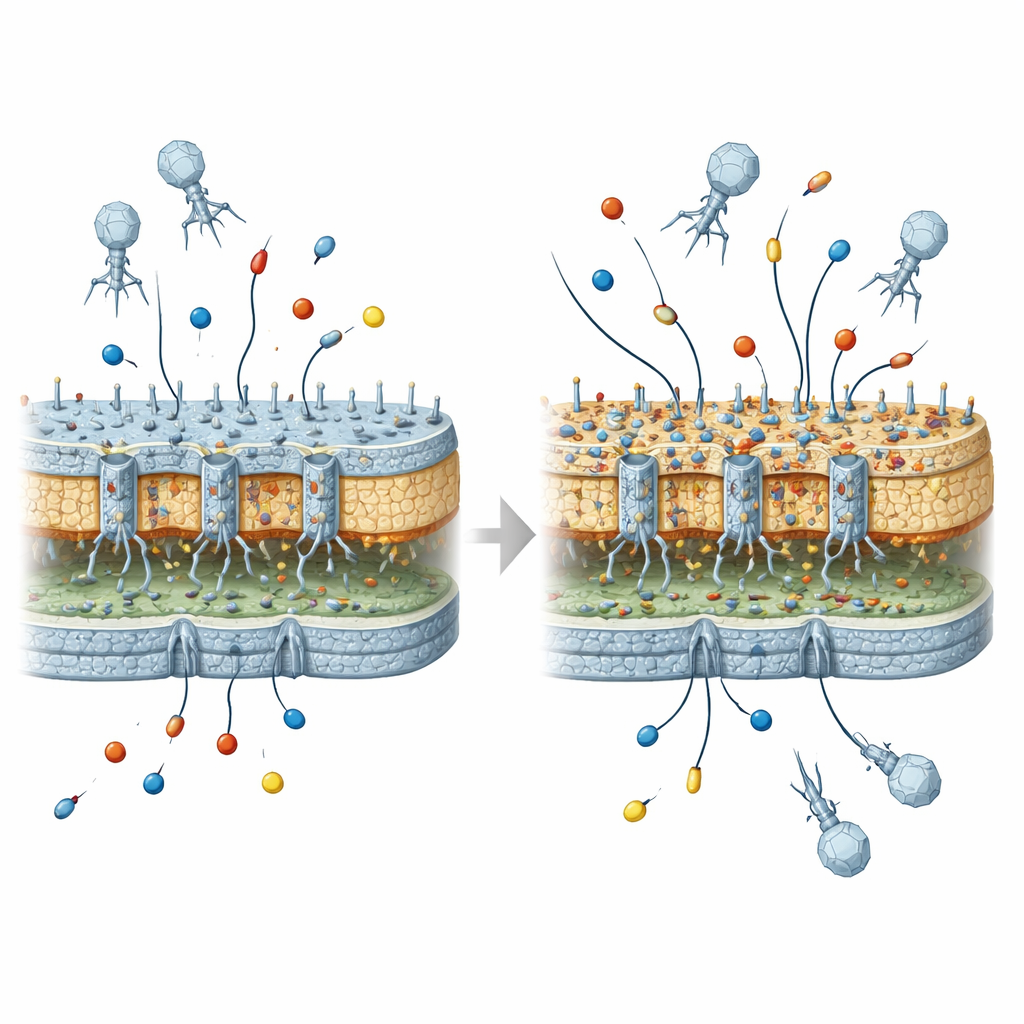
Wiele problematycznych bakterii, w tym Escherichia coli, jest otoczonych twardą zewnętrzną powłoką. Powłoka ta zawiera maleńkie kanały, czyli pory, które wpuszczają składniki odżywcze, a także pozwalają wielu antybiotykom przeniknąć do wnętrza. Zawiera też cząsteczki cukrowo-tłuszczowe znane jako LPS, które tworzą gęstą barierę. Zarówno pory, jak i warstwa LPS są niezbędne do przetrwania bakterii — ale też stanowią punkty przyczepu dla atakujących fagów. Ponieważ te same struktury zewnętrzne służą zarówno do wpuszczania antybiotyków, jak i fagów, wszelkie zmiany chroniące bakterie przed jednym zagrożeniem mogą wpływać na odpowiedź wobec drugiego.
Wirusy kształtujące obronę bakterii
Naukowcy skupili się na dobrze znanym szczepie laboratoryjnym E. coli i klasycznym wirusie go infekującym, zwanym T4. Ten wirus potrzebuje konkretnej pory (nazwanej OmpC) oraz części wewnętrznego rdzenia LPS, by przyczepić się i rozpocząć infekcję. Eksponując duże liczby bakterii na ten wirus w różnych warunkach, a następnie sekwencjonując DNA ocalałych, zespół odkrył, że oporność na wirusa niemal zawsze wiązała się ze zmianami w porze, wewnętrznym rdzeniu LPS lub w obu tych elementach. Czasami ulegały też modyfikacjom systemy regulacyjne kontrolujące produkcję porów. We wszystkich przypadkach końcowym rezultatem była przebudowana zewnętrzna powłoka, która już nie pozwalała wirusowi łatwo się przyczepić.
Kiedy oporność na wirusa tworzy podłoże dla oporności na leki
Następnie zespół zapytał, jak te bakterie odporne na wirusa zachowują się po narażeniu na antybiotyki. Same w sobie, większość mutacji blokujących faga nie czyniła bakterii silnie opornymi na ważne antybiotyki β-laktamowe, takie jak karbapenemy czy zaawansowane cefalosporyny. Jednak gdy bakterie otrzymały geny powszechnych β-laktamaz — enzymów rozkładających antybiotyki β-laktamowe — wyłonił się inny obraz. Mała, lecz istotna podgrupa mutantów wyselekcjonowanych przez wirusa, te z uszkodzoną porą OmpC oraz głęboko zmienionym wewnętrznym rdzeniem LPS, wykazała wyraźnie wyższą przeżywalność przeciwko lekom takim jak meropenem, cefepim i ertapenem. Poziomy te wciąż były poniżej pełnej klinicznej oporności, ale wyraźnie wyższe niż w szczepie wyjściowym niosącym te same enzymy.
Odbudowa mechanizmu od podstaw
Aby upewnić się, że to nie był przypadek, naukowcy inżynierowali precyzyjne mutacje bakteryjne z określonymi delecjami w genie porowym i wybranych genach rdzenia LPS, a następnie mierzyli skuteczność karbapenemów w tych warunkach z β-laktamazami i bez nich. Potwierdzili, że utrata pory OmpC przy jednoczesnym zakłóceniu kluczowych genów wewnętrznego rdzenia LPS wystarczała, by naśladować wzorzec oporności obserwowany po ekspozycji na wirusa. Krytyczne były zmiany wewnątrz rdzenia, a nie zewnętrzne dekoracje. Autorzy sugerują, że te defekty wewnętrznego rdzenia prawdopodobnie zaburzają montaż lub funkcję pozostałych porów i wywołują odpowiedzi stresowe w otoczce komórkowej, co łącznie zmniejsza przepuszczalność zewnętrznej powłoki dla antybiotyków.
Co to znaczy dla przyszłych terapii fagowych
Dla czytelnika niebędącego specjalistą główne przesłanie jest takie: wirusy używane do zabijania bakterii mogą niezamierzenie przebudować ich zewnętrzną zbroję w sposób, który przygotowuje je lepiej do przetrwania niektórych antybiotyków — pod warunkiem, że później przejmą odpowiednie enzymy oporności. Same zmiany wywołane przez wirusa nie tworzą wysoce opornych szczepów, ale tworzą „permisywne” tło, które może zamienić skromne geny oporności w poważniejsze problemy kliniczne. W miarę jak terapia fagowa zbliża się do rutynowego stosowania w medycynie, praca ta sugeruje, że należy starannie rozważać te ewolucyjne skutki uboczne i projektować leczenia wirusowe tak, aby leczyć infekcje, minimalizując jednocześnie ryzyko ułatwiania bakteriom kolejnego kroku w kierunku oporności na antybiotyki.
Cytowanie: Le-Boulch, J., Charneau, E., Chevallereau, A. et al. Selection of porin and LPS mutants during infection by phage T4 facilitates the emergence of β-lactam resistance in Escherichia coli. npj Antimicrob Resist 4, 21 (2026). https://doi.org/10.1038/s44259-026-00193-9
Słowa kluczowe: terapia fagowa, oporność na antybiotyki, Escherichia coli, beta-laktamazy, zewnętrzna błona bakteryjna