Clear Sky Science · de
Selektion von Porin- und LPS-Mutanten während einer Infektion durch Phage T4 fördert das Auftreten von β-Lactam-Resistenz in Escherichia coli
Warum das für die alltägliche Medizin wichtig ist
Ärztinnen und Ärzte gehen die Optionen aus, um Infektionen durch schwer zu beseitigende Bakterien zu behandeln, und neue Ansätze wie der Einsatz von Bakteriophagen — Viren, die Bakterien angreifen — gewinnen an Aufmerksamkeit. Diese Studie stellt eine einfache, aber entscheidende Frage: Könnte der Einsatz solcher Viren gegen Bakterien unbeabsichtigt begünstigen, dass diese Bakterien Resistenzen gegen Antibiotika entwickeln, insbesondere gegen potente Wirkstoffe wie Carbapeneme, die oft als letztes Mittel eingesetzt werden?
Die äußere Panzerung der Bakterien
Viele problematische Bakterien, darunter Escherichia coli, sind von einer robusten äußeren Hülle umgeben. Diese Hülle enthält winzige Kanäle oder Poren, die Nährstoffe hereinlassen und vielen Antibiotika das Eindringen ermöglichen. Sie trägt außerdem zuckerfettähnliche Moleküle, bekannt als LPS, die eine dichte Barriere bilden. Sowohl die Poren als auch die LPS-Schicht sind lebenswichtig für das Bakterium — zugleich dienen sie aber als Andockpunkte für angreifende Phagen. Da dieselben äußeren Strukturen sowohl Antibiotika als auch Phagen Zutritt gewähren, können Veränderungen, die Bakterien vor einer Bedrohung schützen, ihr Verhalten gegenüber der anderen beeinflussen.
Viren, die bakterielle Abwehr formen
Die Forschenden konzentrierten sich auf einen etablierten Laborstamm von E. coli und einen klassischen zugehörigen Phagen, genannt T4. Dieser Phage benötigt einen spezifischen Porenkanal (OmpC) und einen Teil des inneren LPS-Kerns, um sich festzusetzen und eine Infektion zu starten. Durch das Exponieren großer Bakterienpopulationen gegenüber diesem Phagen unter verschiedenen Bedingungen und das anschließende Sequenzieren der DNA der Überlebenden fand das Team heraus, dass Virenresistenz fast immer Veränderungen im Porenkanal, im inneren LPS-Kern oder in beiden Bereichen beinhaltete. Manchmal waren auch Regulationssysteme betroffen, die die Porenbildung steuern. In allen Fällen war das Endergebnis eine umgeformte äußere Hülle, die dem Phagen das Anheften deutlich erschwerte.
Wenn Virenresistenz den Nährboden für Arzneimittelresistenz bildet
Als Nächstes untersuchten die Forschenden, wie sich diese phagenresistenten Bakterien gegenüber Antibiotika verhielten. Allein betrachtet führten die meisten Mutationen, die den Phagen blockierten, nicht zu starker Resistenz gegen wichtige β-Lactam-Antibiotika wie Carbapeneme oder fortgeschrittene Cephalosporine. Trugen die Bakterien jedoch Gene für verbreitete β-Lactamasen — Enzyme, die β-Lactam-Antibiotika abbauen —, zeichnete sich ein anderes Bild ab. Eine kleine, aber bedeutende Untergruppe der durch Phagen selektionierten Mutanten, jene mit sowohl einem geschädigten OmpC-Porenkanal als auch einem stark veränderten inneren LPS-Kern, zeigte deutlich erhöhte Überlebensraten gegen Wirkstoffe wie Meropenem, Cefepim und Ertapenem. Diese Werte lagen zwar noch unterhalb vollständiger klinischer Resistenz, waren aber deutlich höher als beim ursprünglichen Stamm mit denselben Enzymen.
Den Mechanismus von Grund auf rekonstruieren
Um sicherzugehen, dass es sich nicht um einen Zufall handelte, konstruierten die Wissenschaftler präzise bakterielle Mutanten mit definierten Deletionen im Porengen und in ausgewählten LPS-Kern-Genen und maßen dann die Wirksamkeit von Carbapenemen in diesen Hintergründen mit und ohne β-Lactamasen. Sie bestätigten, dass der Verlust des OmpC-Porenkanals bei gleichzeitiger Störung wichtiger innerer LPS-Gene ausreichte, um das nach Phagenexposition beobachtete Resistenzmuster zu imitieren. Entscheidend waren Veränderungen im inneren Kern, nicht äußere Verzierungen. Die Autorinnen und Autoren vermuten, dass diese inneren Kerndefekte wahrscheinlich die Assemblierung oder Funktion der verbleibenden Poren stören und Stressreaktionen in der Zellhülle auslösen, wodurch die Gesamtdurchlässigkeit der äußeren Hülle für Antibiotika verringert wird.
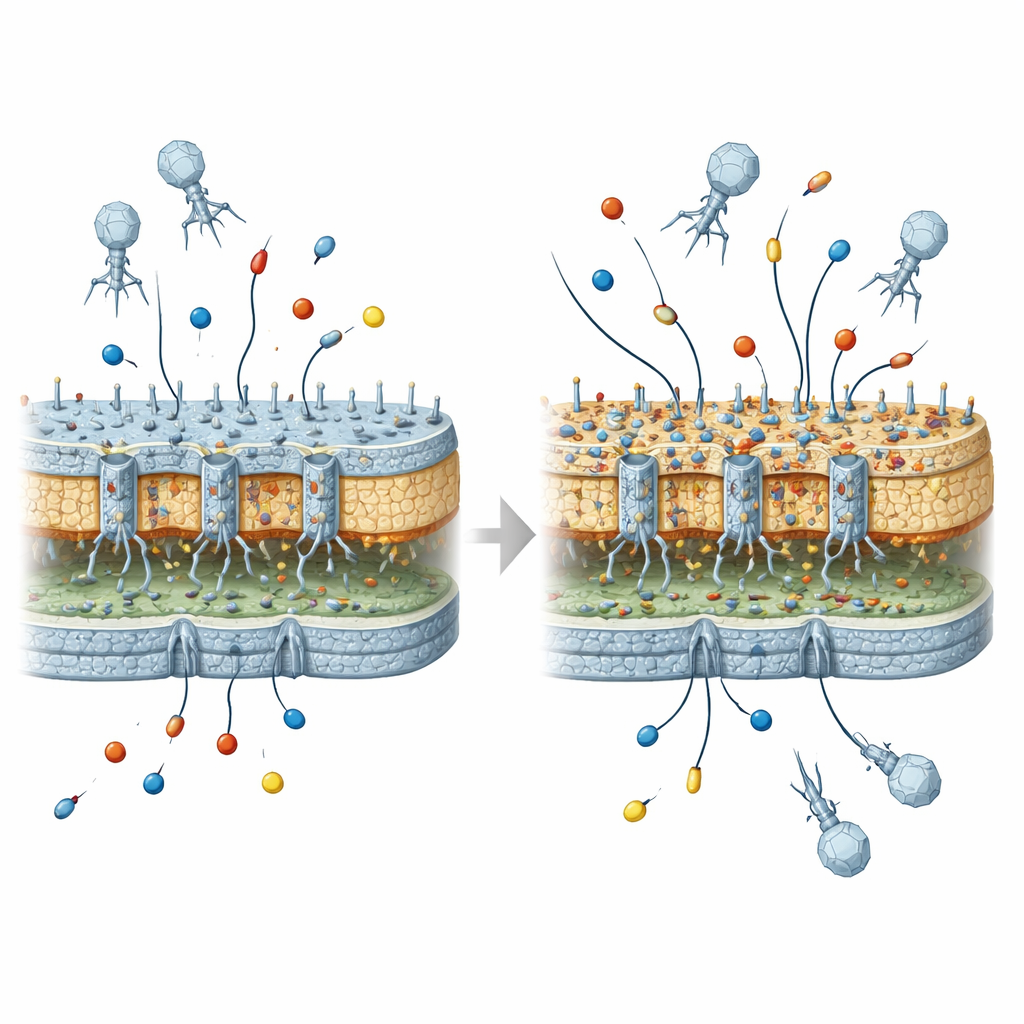
Was das für künftige Phagenbehandlungen bedeutet
Für eine allgemeine Leserschaft lautet die zentrale Botschaft: Viren, die zur Abtötung von Bakterien eingesetzt werden, können unbeabsichtigt die äußere Panzerung der Bakterien so umgestalten, dass diese besser gerüstet sind, bestimmte Antibiotika zu überstehen — vorausgesetzt, sie erwerben später die passenden Resistenzenzyme. Allein erzeugen die durch Phagen selektierten Veränderungen keine stark medikamentenresistenten Stämme, aber sie schaffen einen „permissiven“ Hintergrund, auf dem moderate Resistenzgene zu ernsthafteren klinischen Problemen werden können. Da die Phagentherapie der routinemäßigen medizinischen Anwendung näher rückt, legt diese Arbeit nahe, dass wir diese evolutionären Nebeneffekte sorgfältig bedenken und Phagenbehandlungen so entwickeln müssen, dass Infektionen geheilt werden, ohne das Risiko zu erhöhen, dass Bakterien den nächsten Schritt zur Antibiotikaresistenz machen.
Zitation: Le-Boulch, J., Charneau, E., Chevallereau, A. et al. Selection of porin and LPS mutants during infection by phage T4 facilitates the emergence of β-lactam resistance in Escherichia coli. npj Antimicrob Resist 4, 21 (2026). https://doi.org/10.1038/s44259-026-00193-9
Schlüsselwörter: Phagentherapie, Antibiotikaresistenz, Escherichia coli, β-Lactamasen, äußere bakterielle Membran