Clear Sky Science · sv
Selektion av porin- och LPS-mutander under infektion med fage T4 underlättar framväxten av β-laktamresistens i Escherichia coli
Varför detta spelar roll för vardagsmedicin
Läkarna får allt färre alternativ för att behandla infektioner orsakade av svårutrotade bakterier, och nya idéer som att använda virus som angriper bakterier, så kallade fager, får ökad uppmärksamhet. Denna studie ställer en enkel men avgörande fråga: när vi använder sådana virus för att bekämpa bakterier, kan vi av misstag underlätta för dessa bakterier att bli resistenta mot antibiotika, särskilt kraftfulla läkemedel som karbapenemer som ofta används som sista utväg?
Bakteriernas yttre pansar
Många problematiska bakterier, inklusive Escherichia coli, är omslutna av ett tåligt yttre skal. Detta skal innehåller små kanaler, eller porer, som släpper in näringsämnen och även tillåter många antibiotika att tränga igenom. Det bär också socker–fettsyrakomplex som kallas LPS och som hjälper till att bilda en tät barriär. Både porerna och LPS-lagret är avgörande för bakteriernas överlevnad — men de fungerar också som infästningspunkter för angripande fager. Eftersom samma yttre strukturer används både för att släppa in antibiotika och för att ta emot fager, kan förändringar som skyddar bakterierna mot ett hot påverka hur de reagerar på det andra.
Virus som formar bakteriellt försvar
Forskarna fokuserade på en välkänd laboratoriestam av E. coli och ett klassiskt virus som infekterar den, kallat T4. Detta virus behöver en specifik por (kallad OmpC) och en del av den inre LPS-kärnan för att fästa och påbörja en infektion. Genom att utsätta stora mängder bakterier för detta virus under olika betingelser, och sedan sekvensera DNA från överlevarna, fann teamet att resistens mot viruset nästan alltid innebar förändringar i poren, den inre LPS-kärnan eller båda. Ibland påverkades även regulatoriska system som styr hur porerna produceras. I samtliga fall blev resultatet ett ombyggt yttre skal som inte längre tillät viruset att fästa lätt.
När virusresistens banar väg för läkemedelsresistens
Nästa fråga var hur dessa virusresistenta bakterier beter sig när de utsätts för antibiotika. I sig själva gav de flesta mutationer som blockerade fagen inte stark resistens mot viktiga β-laktamantibiotika såsom karbapenemer eller avancerade cefalosporiner. Men när bakterierna försörjdes med gener för vanliga β-laktamasenzymer — molekyler som bryter ner β-laktamantibiotika — framträdde en annan bild. En liten men betydelsefull delmängd av de fagsorterade mutanterna, de med både en skadad OmpC-por och en djupt förändrad inre LPS-kärna, visade tydligt ökad överlevnad mot läkemedel som meropenem, cefepim och ertapenem. Dessa nivåer låg fortfarande under full klinisk resistens, men var klart högre än i den ursprungliga stammen som bar samma enzymer.
Återskapa mekanismen från grunden
För att säkerställa att detta inte var en tillfällighet skapade forskarna precist definierade bakteriemutanter med bestämda deletioner i porgenen och i utvalda LPS-kärngener, och mätte hur väl karbapenemer fungerade i dessa bakgrunder med och utan β-laktamaser. De bekräftade att förlust av OmpC-poren samtidigt som viktiga inre LPS-gener stördes var tillräckligt för att efterlikna resistensmönstret som observerats efter fagexponering. Förändringar i den inre kärnan, inte yttre utsmyckningar, var avgörande. Författarna föreslår att dessa defekter i den inre kärnan sannolikt stör monteringen eller funktionen hos de återstående porerna och utlöser stressreaktioner i cellmembranet, vilket tillsammans sänker det yttre skalets genomsläpplighet för antibiotika.
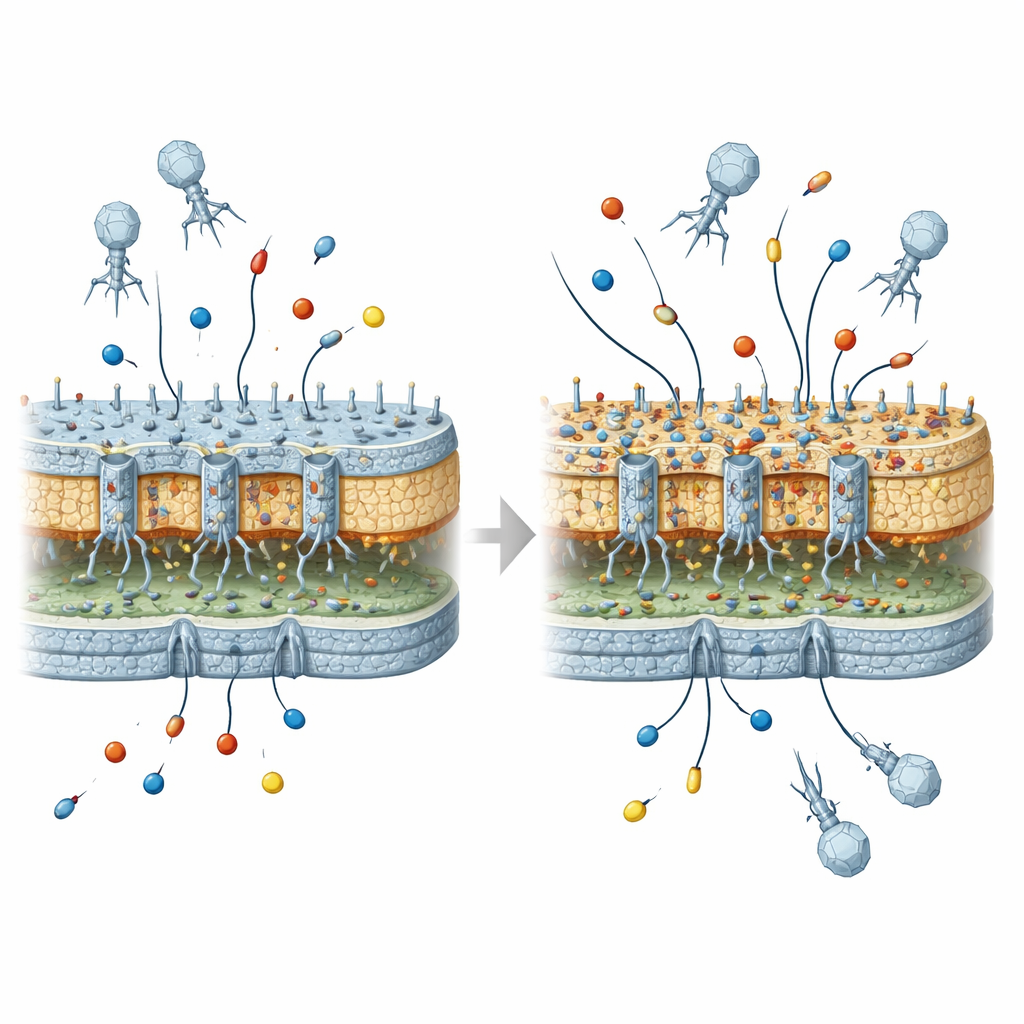
Vad detta betyder för framtida fagbehandlingar
För en lekmannaläsare är huvudbudskapet att virus som används för att döda bakterier oavsiktligt kan omforma bakteriernas yttre pansar på sätt som gör dem bättre rustade att stå emot vissa antibiotika — förutsatt att de senare tar upp rätt resistensenzymer. I sig skapar de fagsorterade förändringarna inte höggradigt läkemedelsresistenta stammar, men de skapar en ”permissiv” bakgrund som kan omvandla måttliga resistensgener till mer allvarliga kliniska problem. I takt med att fagterapi närmar sig rutinmässig medicinsk användning menar denna studie att vi noggrant måste överväga dessa evolutionära sidoeffekter och utforma virusbehandlingar som botar infektioner samtidigt som risken minimeras för att hjälpa bakterier att ta nästa steg mot antibiotikaresistens.
Citering: Le-Boulch, J., Charneau, E., Chevallereau, A. et al. Selection of porin and LPS mutants during infection by phage T4 facilitates the emergence of β-lactam resistance in Escherichia coli. npj Antimicrob Resist 4, 21 (2026). https://doi.org/10.1038/s44259-026-00193-9
Nyckelord: fagterapi, antibiotikaresistens, Escherichia coli, beta-laktamaser, bakteriers yttre membran