Clear Sky Science · ru
Отбор мутантов пор и LPS во время инфекции фагом T4 облегчает появление резистентности к β‑лактамам у Escherichia coli
Почему это важно для повседневной медицины
Врачам всё труднее лечить инфекции, вызванные трудноудаляемыми бактериями, и новые идеи — например применение вирусов, атакующих бактерии, так называемых фагов — привлекают внимание. В этом исследовании поставлен простой, но ключевой вопрос: не приведёт ли применение таких вирусов к тому, что мы невольно облегчим бактериям путь к устойчивости к антибиотикам, особенно к мощным препаратам вроде карбапенемов, которые часто используют как средство последней инстанции?
Наружная броня бактерий
Многие проблемные бактерии, включая Escherichia coli, окружены прочной внешней оболочкой. В этой оболочке есть крошечные каналы, или поры, которые пропускают питательные вещества и через которые проникает множество антибиотиков. Она также содержит молекулы, состоящие из сахаров и липидов, известные как LPS, которые формируют плотный барьер. И поры, и слой LPS необходимы для выживания бактерии — но одновременно они служат точками прикрепления для нападающих фагов. Поскольку одни и те же внешние структуры используются и для проникновения антибиотиков, и для прихода фагов, любые изменения, защищающие бактерию от одной угрозы, могут повлиять на её чувствительность к другой.
Вирусы, формирующие бактериальную защиту
Исследователи сосредоточились на хорошо изученной лабораторной штамме E. coli и классическом фаге, инфицирующем его, — T4. Этот фаг требует специфической поры (OmpC) и части внутреннего ядра LPS для прикрепления и начала инфекции. Подвергая большое число бактерий воздействию этого фага в разных условиях и затем секвенируя ДНК выживших, команда обнаружила, что устойчивость к фагу почти всегда связана с изменениями в поре, во внутреннем ядре LPS или в обоих. Иногда также изменялись регуляторные системы, контролирующие синтез пор. Во всех случаях конечным результатом была перестройка внешней оболочки, после которой фагу стало труднее прикрепляться.
Когда устойчивость к фагу создаёт предпосылки для лекарственной резистентности
Далее учёные изучили, как эти фаг-устойчивые бактерии ведут себя при воздействии антибиотиков. Сами по себе большинство мутаций, блокировавших фаг, не делали бактерии сильно устойчивыми к важным β‑лактамным антибиотикам, таким как карбапенемы или современные цефалоспорины. Но когда бактерии получали гены распространённых β‑лактамаз — ферментов, разрушающих β‑лактамные антибиотики — проявлялась иная картина. Небольшая, но значимая часть фаг‑отобранных мутантов, с сочетанием дефектной поры OmpC и глубоко изменённого внутреннего ядра LPS, демонстрировала заметно более высокую выживаемость при воздействии таких препаратов, как меропенем, цефепим и ертапенем. Эти уровни всё ещё оставались ниже полной клинической резистентности, но были явно выше, чем у исходного штамма с теми же ферментами.
Воссоздание механизма «с нуля»
Чтобы убедиться, что это не случайность, учёные сконструировали точные бактериальные мутанты с определёнными делецией в гене поры и в выбранных генах ядра LPS, затем измеряли эффективность карбапенемов в этих генетических фондах с β‑лактамазами и без них. Они подтвердили, что потеря поры OmpC при одновременном нарушении ключевых генов внутреннего ядра LPS достаточна, чтобы воспроизвести паттерн резистентности, наблюдавшийся после воздействия фага. Критическими оказались изменения внутреннего ядра, а не наружные «декорации». Авторы предполагают, что дефекты внутреннего ядра нарушают сборку или функцию оставшихся пор и вызывают стресс‑ответы в оболочке клетки, что вместе снижает общую проницаемость внешней оболочки для антибиотиков.
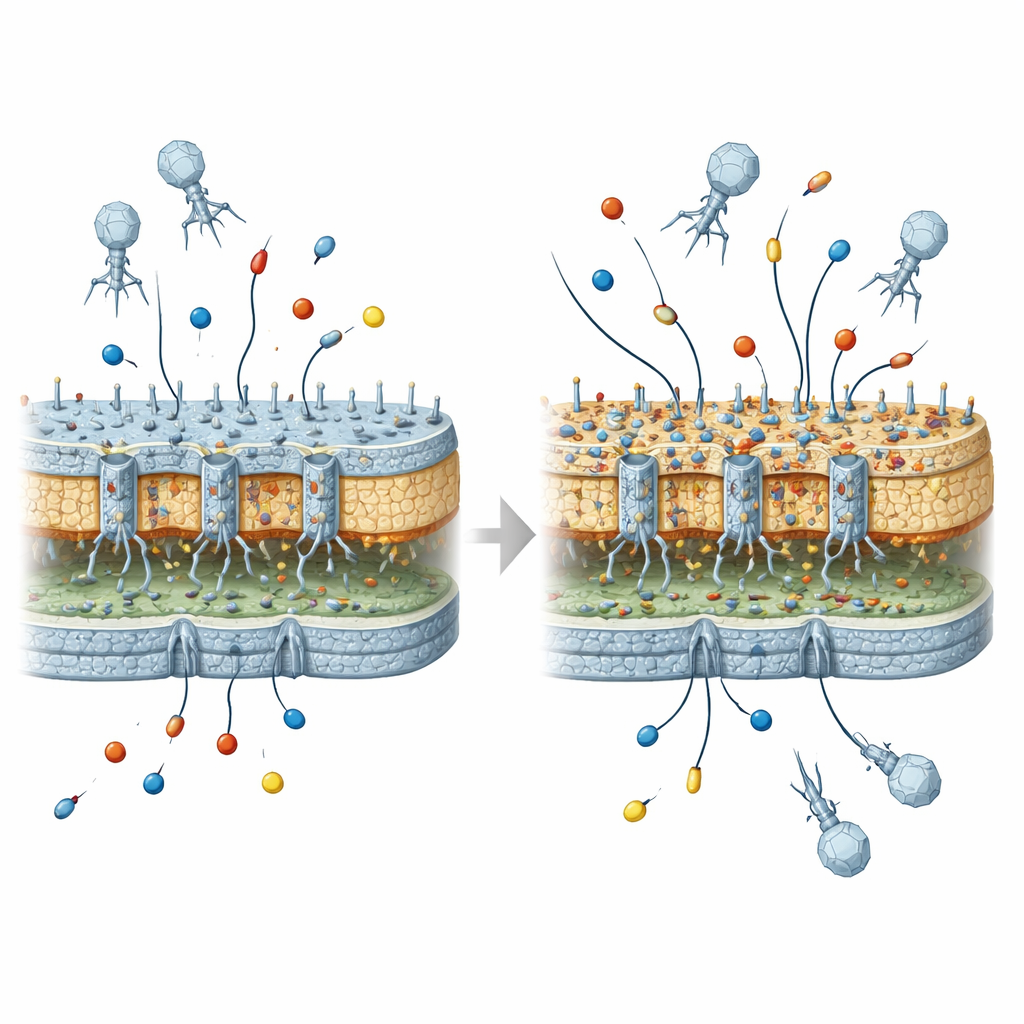
Что это значит для будущих фаговых лечений
Для неспециалиста главный вывод таков: вирусы, используемые для уничтожения бактерий, могут непреднамеренно перестроить их внешнюю «броню» таким образом, что бактерии станут лучше подготовлены выдержать действие некоторых антибиотиков — при условии, что позже они приобретут соответствующие ферменты резистентности. Сами по себе фаг‑индуцированные изменения не создают высоко резистентные штаммы, но формируют «пермиссивный» фон, который может превратить умеренные гены резистентности в более серьёзную клиническую проблему. По мере того как фаговая терапия приближается к рутинному медицинскому применению, эта работа подчёркивает необходимость учитывать такие эволюционные побочные эффекты и проектировать фаговые вмешательства так, чтобы лечить инфекции, минимизируя риск того, что мы поможем бактериям сделать следующий шаг к устойчивости к антибиотикам.
Цитирование: Le-Boulch, J., Charneau, E., Chevallereau, A. et al. Selection of porin and LPS mutants during infection by phage T4 facilitates the emergence of β-lactam resistance in Escherichia coli. npj Antimicrob Resist 4, 21 (2026). https://doi.org/10.1038/s44259-026-00193-9
Ключевые слова: фаговая терапия, резистентность к антибиотикам, Escherichia coli, β‑лактамазы, наружная мембрана бактерий