Clear Sky Science · tr
Faj T4 ile enfeksiyon sırasında porin ve LPS mutasyonlarının seçilmesi, Escherichia coli’de β-laktam direncinin ortaya çıkışını kolaylaştırıyor
Günlük tıp için neden önemli
Doktorların zor öldürülen bakterilerin neden olduğu enfeksiyonları tedavi etmek için seçenekleri azalıyor ve bakterilere saldıran virüsler, yani fajlar, gibi yeni yaklaşımlar ilgi kazanıyor. Bu çalışma basit ama kritik bir soruyu soruyor: Bu tür virüsleri bakterilerle mücadelede kullandığımızda, özellikle son çare olarak sıkça başvurulan karbapenemler gibi güçlü antibiyotiklere karşı bakterilerin direnç kazanmasını istemeden kolaylaştırır mıyız?
Bakterinin dış zırhı
Escherichia coli de dahil olmak üzere birçok sorunlu bakteri sağlam bir dış kabukla çevrilidir. Bu kabuk, besinleri alan ve birçok antibiyotiğin içeri kaymasını sağlayan küçük kanalları ya da gözenekleri içerir. Ayrıca yoğun bir bariyer oluşturmaya yardımcı olan şeker-yağ molekülleri olarak bilinen LPS’leri taşır. Hem gözenekler hem de LPS tabakası bakterinin hayatta kalması için elzemdir—ancak aynı zamanda saldıran fajlar için yapışma noktaları olarak da iş görür. Aynı dış yapılar hem antibiyotikleri hem de fajları içeri alırken kullanıldığından, bakterileri bir tehdide karşı koruyan değişiklikler diğerine karşı tepkilerini de etkileyebilir.
Bakteriyel savunmayı şekillendiren virüsler
Araştırmacılar iyi bilinen bir laboratuvar E. coli suşu ve ona enfekte olan klasik bir virüs olan T4 üzerinde durdular. Bu virüs, tutunup enfeksiyonu başlatmak için belirli bir gözenek (OmpC olarak adlandırılan) ve iç LPS çekirdeğinin bir bölümüne ihtiyaç duyar. Büyük sayıda bakteriyi farklı koşullar altında bu virüse maruz bırakarak ve hayatta kalanların DNA’sını dizileyerek, ekip faj direncinin neredeyse her durumda gözenekte, iç LPS çekirdeğinde veya her ikisinde değişikliklerle ilişkili olduğunu buldu. Bazen gözeneklerin üretimini kontrol eden düzenleyici sistemler de değişiyordu. Tüm durumlarda sonuç, virüsün kolayca tutunmasını artık sağlamayan yeniden düzenlenmiş bir dış kabuktu.
Virüs direnci ilaç direnci için zemin hazırladığında
Sonra ekip, bu virüs-dirençli bakterilerin antibiyotiklere maruz kaldıklarında nasıl davrandığını sordu. Tek başına, fajı engelleyen mutasyonların çoğu, bakterileri karbapenemler veya ileri sefalosporinler gibi önemli β-laktam antibiyotiklere karşı güçlü şekilde dirençli kılmıyordu. Ancak bakterilere yaygın β-laktamaz enzimlerinin genleri verildiğinde—β-laktam antibiyotikleri parçalayabilen moleküller—farklı bir tablo ortaya çıktı. Virüsün seçtiği mutanların küçük ama önemli bir alt kümesi; hem OmpC gözeneklerinin hasarlı olduğu hem de iç LPS çekirdeğinin derinden değiştiği suşlar, meropenem, sefepim ve ertapenem gibi ilaçlara karşı belirgin şekilde daha yüksek hayatta kalma gösterdi. Bu düzeyler tam klinik direncin altında kaldı, ancak aynı enzimleri taşıyan orijinal suşa göre açıkça daha yüksekti.
Mekanizmayı baştan inşa etmek
Bunun tesadüf olmadığından emin olmak için bilim insanları gözenek geninde ve seçilmiş LPS çekirdek genlerinde tanımlı silinmeler içeren hassas bakteriyel mutanlar tasarladılar ve ardından bu arka planlarda karbapenemlerin β-laktamazlarla ve β-laktamazlar olmadan nasıl çalıştığını ölçtüler. OmpC gözenek kaybının, aynı zamanda kritik iç LPS genlerinin bozulmasının, virüs maruziyetinden sonra görülen direnç desenini taklit etmek için yeterli olduğunu doğruladılar. Dış süslemeler değil, iç çekirdek değişiklikleri belirleyiciydi. Yazarlar, bu iç-çekirdek kusurlarının muhtemelen kalan gözeneklerin montajını veya işlevini bozduğunu ve hücre zarfında stres tepkilerini tetikleyerek dış kabuğun antibiyotiklere karşı genel geçirgenliğini düşürdüğünü öne sürüyorlar.
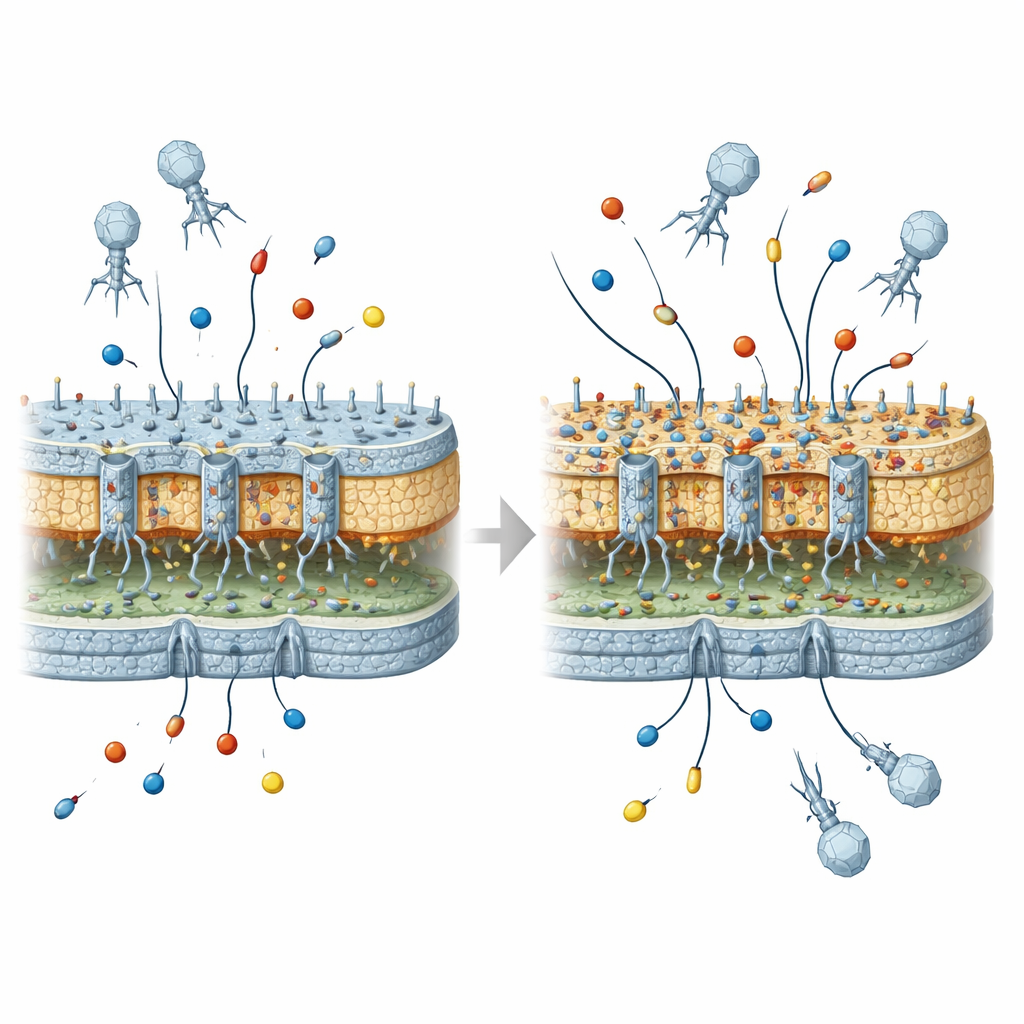
Gelecekteki faj tedavileri için anlamı
Bir meraklı okuyucu için merkezî mesaj, bakterileri öldürmek için kullanılan virüslerin, daha sonra doğru direnç enzimlerini kazandıklarında belirli antibiyotiklere karşı dayanıklılıklarını artırabilecek şekilde bakterinin dış zırhını istemeden yeniden şekillendirebileceğidir. Tek başına fajla seçilen değişiklikler yüksek derecede ilaç dirençli suşlar yaratmıyor, ancak mütevazı direnç genlerini daha ciddi klinik sorunlara dönüştürebilecek “izin verici” bir zemin oluşturuyorlar. Faj terapisi rutin tıbbi kullanımına yaklaşırken bu çalışma, enfeksiyonları iyileştirirken bakterilerin antibiyotik direncine bir sonraki adımı atmasına yardımcı olma riskini en aza indirecek şekilde virus tedavilerini dikkatle tasarlamamız gerektiğini savunuyor.
Atıf: Le-Boulch, J., Charneau, E., Chevallereau, A. et al. Selection of porin and LPS mutants during infection by phage T4 facilitates the emergence of β-lactam resistance in Escherichia coli. npj Antimicrob Resist 4, 21 (2026). https://doi.org/10.1038/s44259-026-00193-9
Anahtar kelimeler: faj terapisi, antibiyotik direnci, Escherichia coli, beta-laktamazlar, bakteriyel dış zar