Clear Sky Science · it
Selezione di mutanti delle porine e del LPS durante l’infezione da fago T4 facilita l’emergere della resistenza ai β-lattamici in Escherichia coli
Perché questo è importante per la medicina di tutti i giorni
I medici stanno esaurendo le opzioni per trattare infezioni causate da batteri difficili da eliminare, e nuove idee come l’uso di virus che attaccano i batteri, detti fagi, stanno attirando attenzione. Questo studio pone una domanda semplice ma cruciale: quando usiamo questi virus per combattere i batteri, potremmo per errore facilitare la comparsa di resistenza agli antibiotici, in particolare a farmaci potenti come i carbapenemi spesso impiegati come ultima risorsa?
La corazza esterna dei batteri
Molti batteri problematici, compreso Escherichia coli, sono avvolti da un involucro esterno robusto. Questo strato contiene minuscoli canali, o pori, che lasciano entrare nutrienti e permettono anche a molti antibiotici di penetrare. Vi sono inoltre molecole zucchero-grasse note come LPS che contribuiscono a formare una barriera densa. Sia i pori sia lo strato di LPS sono essenziali per la sopravvivenza del batterio—ma fungono anche da punti di aggancio per i fagi invasori. Poiché le stesse strutture esterne servono sia per ammettere gli antibiotici sia per consentire l’ingresso dei fagi, qualsiasi modifica che protegga i batteri da una minaccia può influenzare la loro risposta all’altra.
Virus che modellano le difese batteriche
I ricercatori si sono concentrati su un ceppo di laboratorio ben noto di E. coli e su un classico virus che lo infetta, chiamato T4. Questo virus richiede un poro specifico (chiamato OmpC) e una parte del nucleo interno del LPS per agganciarsi e iniziare l’infezione. Esponendo grandi popolazioni di batteri a questo virus in condizioni diverse, e sequenziando il DNA dei sopravvissuti, il team ha scoperto che la resistenza al virus implicava quasi sempre modifiche nel poro, nel nucleo interno del LPS, o in entrambi. Talvolta risultavano alterati anche sistemi regolatori che controllano la produzione delle porine. In tutti i casi, il risultato finale era una rimodellata corazza esterna che non permetteva più al virus di agganciarsi facilmente.
Quando la resistenza al virus prepara il terreno per la resistenza ai farmaci
Successivamente il gruppo ha chiesto come si comportassero questi batteri resistenti al virus quando esposti agli antibiotici. Da sole, la maggior parte delle mutazioni che bloccavano il fago non rendevano i batteri fortemente resistenti ai principali antibiotici β-lattamici come i carbapenemi o le cefalosporine di ultima generazione. Ma quando i batteri ricevevano geni per comuni enzimi β-lattamasi—molecole che degradano gli antibiotici β-lattamici—emerse un quadro diverso. Un piccolo ma significativo sottoinsieme di mutanti selezionati dal virus, quelli con sia il poro OmpC compromesso sia un nucleo interno del LPS fortemente alterato, mostrò una sopravvivenza visibilmente maggiore contro farmaci come meropenem, cefepime ed ertapenem. Questi livelli restavano comunque al di sotto della piena resistenza clinica, ma risultavano chiaramente più alti rispetto al ceppo originale che portava gli stessi enzimi.
Ricostruire il meccanismo da zero
Per verificare che non fosse una coincidenza, gli scienziati hanno ingegnerizzato mutanti batterici precisi con delezioni definite nel gene della porina e in geni selezionati del nucleo del LPS, quindi hanno misurato l’efficacia dei carbapenemi in questi contesti con e senza β-lattamasi. Hanno confermato che la perdita della porina OmpC insieme alla disgregazione di geni chiave del nucleo interno del LPS era sufficiente a imitare il profilo di resistenza osservato dopo l’esposizione al virus. Le alterazioni del nucleo interno, non le decorazioni esterne, risultarono critiche. Gli autori suggeriscono che questi difetti del nucleo interno disturbano probabilmente l’assemblaggio o la funzione delle porine rimanenti e attivano risposte di stress nell’involucro cellulare, riducendo complessivamente la permeabilità della corazza esterna agli antibiotici.
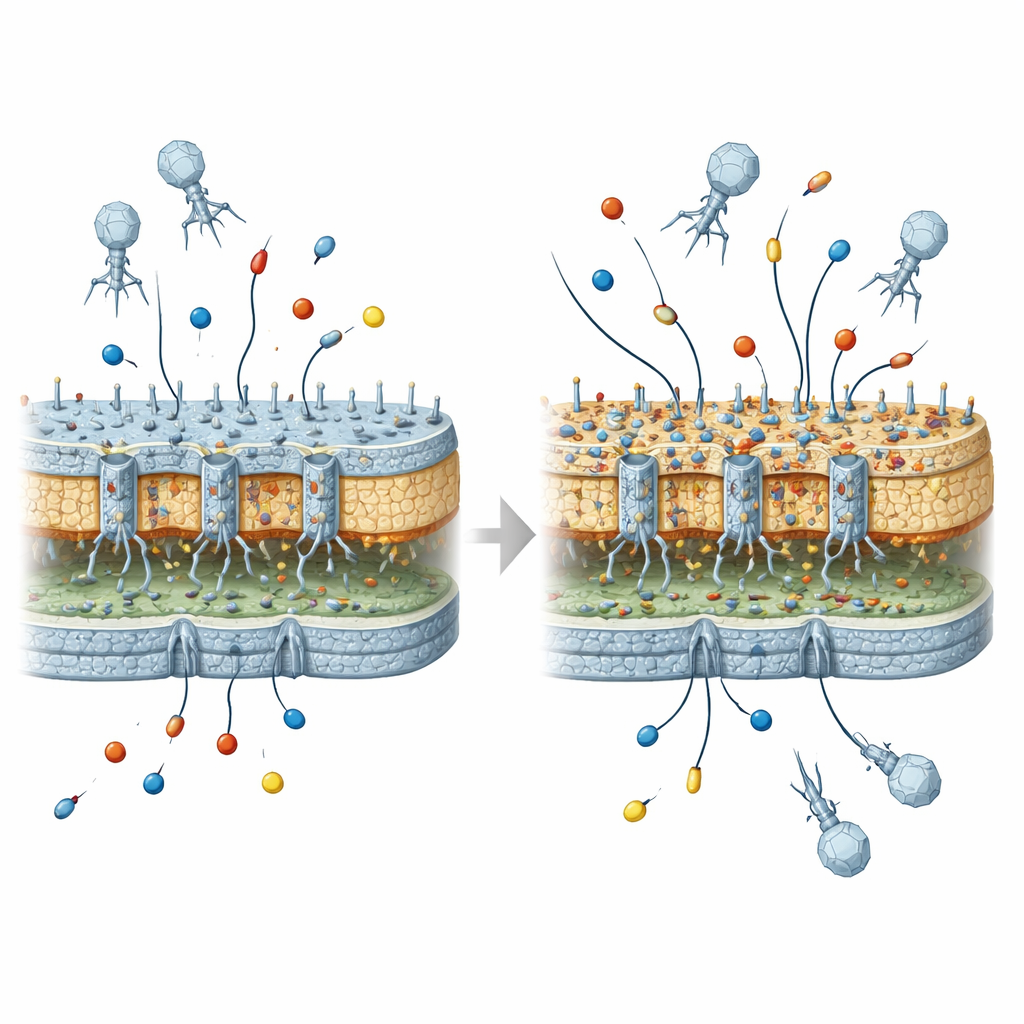
Cosa significa per i futuri trattamenti con fagi
Per un lettore non specialista, il messaggio centrale è che i virus usati per uccidere i batteri possono involontariamente rimodellare la corazza esterna dei batteri in modi che li rendono più preparati a sopportare certi antibiotici—a patto che in seguito acquisiscano i giusti enzimi di resistenza. Da soli, i cambi selezionati dal virus non generano ceppi altamente resistenti ai farmaci, ma creano un contesto “permissivo” che può trasformare geni di resistenza modesta in problemi clinici più seri. Con l’avvicinarsi della terapia con fagi a un uso medico routinario, questo lavoro sostiene la necessità di considerare attentamente questi effetti evolutivi collaterali, progettando trattamenti virali che curino le infezioni minimizzando il rischio di agevolare il passo successivo verso la resistenza agli antibiotici.
Citazione: Le-Boulch, J., Charneau, E., Chevallereau, A. et al. Selection of porin and LPS mutants during infection by phage T4 facilitates the emergence of β-lactam resistance in Escherichia coli. npj Antimicrob Resist 4, 21 (2026). https://doi.org/10.1038/s44259-026-00193-9
Parole chiave: terapia con fagi, resistenza agli antibiotici, Escherichia coli, beta-lattamasi, membrana esterna batterica