Clear Sky Science · fr
Sélection de mutants de porine et du LPS pendant l’infection par le phage T4 favorise l’émergence de la résistance aux β-lactamines chez Escherichia coli
Pourquoi cela importe en médecine courante
Les médecins manquent d’options pour traiter les infections causées par des bactéries difficiles à éliminer, et des approches nouvelles comme l’utilisation de virus qui attaquent les bactéries, appelés phages, suscitent de l’intérêt. Cette étude pose une question simple mais cruciale : lorsque nous utilisons ces virus pour combattre les bactéries, risquons‑nous, par inadvertance, de faciliter chez ces bactéries l’apparition d’une résistance aux antibiotiques, en particulier à des médicaments puissants comme les carbapénèmes, souvent réservés au dernier recours ?
L’armure externe des bactéries
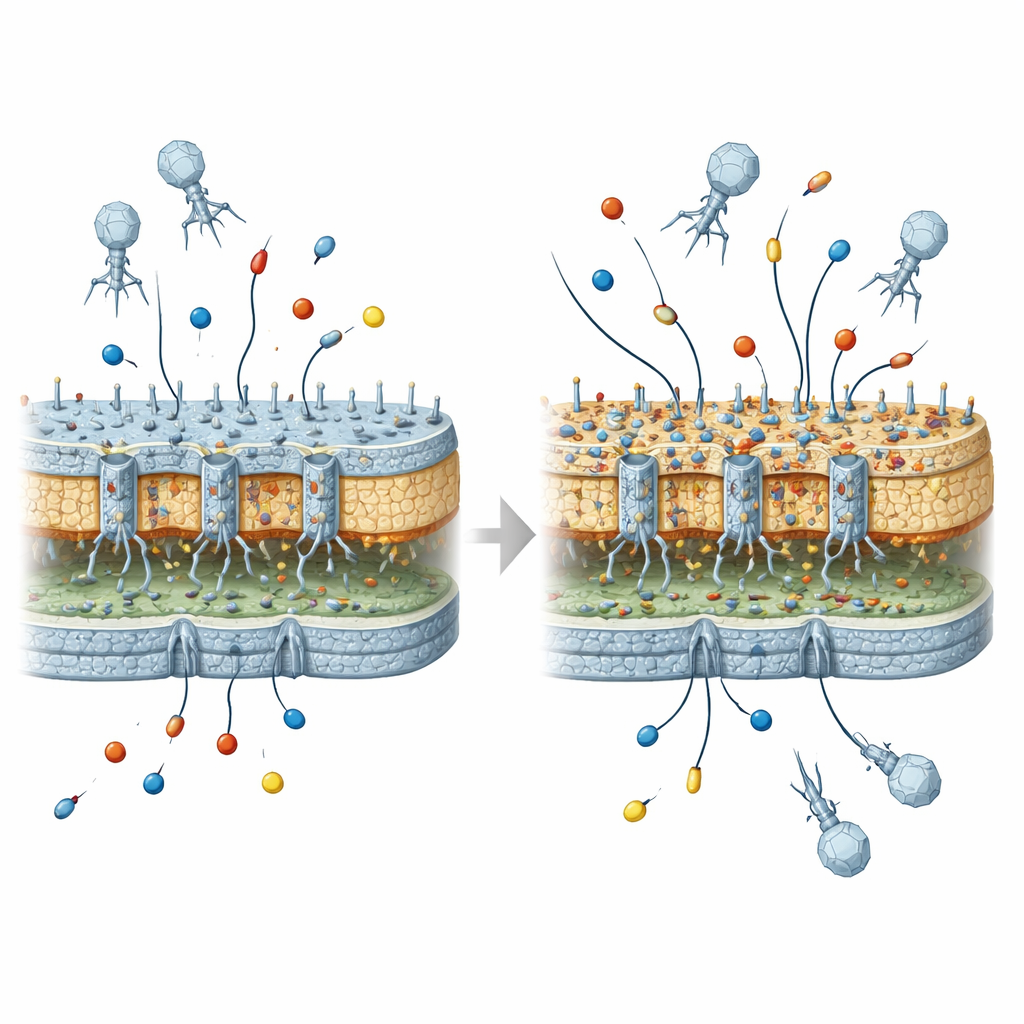
De nombreuses bactéries problématiques, dont Escherichia coli, sont enveloppées d’une coque externe résistante. Cette couche contient de minuscules canaux, ou pores, qui laissent entrer les nutriments et permettent aussi à de nombreux antibiotiques de pénétrer. Elle porte également des molécules sucre‑lipides connues sous le nom de LPS qui contribuent à former une barrière dense. Les pores et la couche de LPS sont essentiels à la survie bactérienne — mais servent aussi d’ancrage aux phages attaquants. Parce que ces mêmes structures externes permettent l’accès aux antibiotiques et aux phages, toute modification qui protège les bactéries contre une menace peut modifier leur réponse à l’autre.
Des virus qui façonnent les défenses bactériennes
Les chercheurs se sont concentrés sur une souche de laboratoire bien caractérisée d’E. coli et sur un virus classique qui l’infecte, appelé T4. Ce virus nécessite une porine spécifique (nommée OmpC) et une partie du cœur interne du LPS pour s’attacher et initier l’infection. En exposant de grands nombres de bactéries à ce virus dans différentes conditions, puis en séquençant l’ADN des survivants, l’équipe a constaté que la résistance au virus impliquait presque toujours des modifications de la porine, du cœur interne du LPS, ou des deux. Parfois, des systèmes régulateurs contrôlant la production des pores étaient aussi altérés. Dans tous les cas, le résultat final était une coque externe remodelée qui n’autorisait plus facilement l’attachement du virus.
Quand la résistance au virus prépare le terrain pour la résistance aux médicaments
Puis l’équipe a examiné le comportement de ces bactéries résistantes au virus lorsqu’elles étaient exposées aux antibiotiques. Pris isolément, la plupart des mutations qui bloquaient le phage ne conféraient pas aux bactéries une résistance marquée aux β‑lactamines importantes comme les carbapénèmes ou les céphalosporines avancées. Mais lorsqu’on équipait les bactéries de gènes codant pour des β‑lactamases courantes — des enzymes qui dégradent les β‑lactamines — un autre tableau apparaissait. Un petit mais significatif sous‑ensemble de mutants sélectionnés par le virus, ceux présentant à la fois une porine OmpC endommagée et un cœur interne du LPS profondément altéré, montraient une survie sensiblement plus élevée face à des médicaments comme le méropénem, le céfépime et l’ertapénem. Ces niveaux restaient inférieurs à une résistance clinique complète, mais étaient nettement plus élevés que chez la souche d’origine portant les mêmes enzymes.
Reconstruire le mécanisme depuis la base
Pour vérifier que ce n’était pas un hasard, les scientifiques ont conçu des mutants bactériens précis avec des délétions définies dans le gène de la porine et dans certains gènes du cœur du LPS, puis ont mesuré l’efficacité des carbapénèmes dans ces contextes avec et sans β‑lactamases. Ils ont confirmé que la perte de la porine OmpC combinée à la perturbation de gènes clés du cœur interne du LPS suffisait à reproduire le schéma de résistance observé après exposition au virus. Ce sont les altérations du cœur interne, et non les décorations externes, qui étaient déterminantes. Les auteurs suggèrent que ces défauts du cœur interne perturbent probablement l’assemblage ou la fonction des pores restants et déclenchent des réponses au stress de l’enveloppe cellulaire, réduisant ensemble la perméabilité globale de la coque externe aux antibiotiques.
Ce que cela signifie pour les traitements futurs par phages
Pour un lecteur non spécialiste, le message central est que les virus utilisés pour tuer les bactéries peuvent involontairement remodeler leur armure externe de manière à les préparer mieux à résister à certains antibiotiques — à condition qu’elles acquièrent ensuite les enzymes de résistance appropriées. Pris seuls, les changements sélectionnés par le virus ne créent pas de souches hautement résistantes, mais ils établissent un contexte « permissif » qui peut transformer des gènes de résistance modestes en problèmes cliniques plus sérieux. À mesure que la thérapie par phages se rapproche d’une utilisation médicale courante, ce travail plaide pour une réflexion attentive sur ces effets évolutifs secondaires, et pour concevoir des traitements viraux qui guérissent les infections tout en minimisant le risque d’aider les bactéries à franchir l’étape suivante vers la résistance aux antibiotiques.
Citation: Le-Boulch, J., Charneau, E., Chevallereau, A. et al. Selection of porin and LPS mutants during infection by phage T4 facilitates the emergence of β-lactam resistance in Escherichia coli. npj Antimicrob Resist 4, 21 (2026). https://doi.org/10.1038/s44259-026-00193-9
Mots-clés: thérapie par des phages, résistance aux antibiotiques, Escherichia coli, β-lactamases, membrane externe bactérienne