Clear Sky Science · nl
Selectie van porine- en LPS-mutanten tijdens infectie door fage T4 bevordert het ontstaan van β-lactamresistentie in Escherichia coli
Waarom dit van belang is voor de dagelijkse geneeskunde
Artsen raken uitgeput wat betreft behandelopties voor infecties veroorzaakt door moeilijk te doden bacteriën, en nieuwe ideeën zoals het gebruik van virussen die bacteriën aanvallen, zogenaamde fagen, krijgen steeds meer aandacht. Deze studie stelt een eenvoudige maar cruciale vraag: wanneer we zulke virussen gebruiken om bacteriën te bestrijden, kunnen we dan per ongeluk het voor die bacteriën makkelijker maken om resistentie tegen antibiotica te ontwikkelen, vooral tegen krachtige middelen zoals carbapenems die vaak als laatste redmiddel worden ingezet?
Het buitenschild van bacteriën
Veel problematische bacteriën, waaronder Escherichia coli, zijn omgeven door een robuuste buitenlaag. Deze laag bevat kleine kanalen of poriën die voedingsstoffen binnenlaten en ook veel antibiotica toelaten. Ze bevat ook suikervetzuren, bekend als LPS, die helpen een dichte barrière te vormen. Zowel de poriën als de LPS-laag zijn essentieel voor het overleven van de bacterie—maar ze dienen ook als aanhechtingspunten voor aanvallende fagen. Omdat dezelfde buitenstructuren zowel gebruikt worden om antibiotica binnen te laten als om fagen binnen te laten, kunnen veranderingen die bescherming bieden tegen de ene bedreiging het antwoord op de andere beïnvloeden.
Virussen die bacteriële verdedigingen vormen
De onderzoekers concentreerden zich op een bekende laboratoriumstam van E. coli en een klassieke virus dat deze infecteert, genaamd T4. Dit virus heeft een specifieke porie (OmpC genoemd) en een deel van de binnenste LPS-kern nodig om zich vast te hechten en een infectie te starten. Door grote aantallen bacteriën onder verschillende condities aan dit virus bloot te stellen en vervolgens het DNA van overlevenden te sequencen, vonden de onderzoekers dat resistentie tegen het virus bijna altijd veranderingen in de porie, de binnenste LPS-kern of beide inhield. Soms werden ook regulerende systemen die de productie van poriën aansturen gewijzigd. In alle gevallen was het eindresultaat een herbouwde buitenlaag die het virus niet langer gemakkelijk liet aanhechten.
Wanneer virusresistentie het toneel vormt voor medicijnresistentie
Vervolgens onderzochten de onderzoekers hoe deze virusresistente bacteriën zich gedroegen bij blootstelling aan antibiotica. Op zichzelf maakten de meeste mutaties die de faag blokkeerden de bacteriën niet sterk resistent tegen belangrijke β-lactamantibiotica zoals carbapenems of geavanceerde cefalosporines. Maar wanneer de bacteriën genen kregen voor veelvoorkomende β-lactamase-enzymen—moleculen die β-lactamantibiotica afbreken—ontstond een ander beeld. Een kleine maar belangrijke subset van virus-geselecteerde mutanten, die zowel een beschadigde OmpC-porie als een sterk veranderde binnenste LPS-kern hadden, vertoonde duidelijk hogere overleving tegen middelen als meropenem, cefepime en ertapenem. Deze niveaus lagen nog onder volledige klinische resistentie, maar waren duidelijk hoger dan bij de oorspronkelijke stam met dezelfde enzymen.
Het mechanisme vanaf de basis herbouwen
Om zeker te zijn dat dit geen toeval was, bouwden de wetenschappers nauwkeurig gedefinieerde bacteriële mutanten met deleties in het poriegen en in geselecteerde LPS-kerngenen en maten ze hoe goed carbapenems werkten in deze achtergronden, met en zonder β-lactamases. Ze bevestigden dat het verlies van de OmpC-porie in combinatie met verstoring van sleutelgenen van de binnenste LPS-kern voldoende was om het resistentiepatroon na faagblootstelling na te bootsen. Veranderingen in de binnenkern, niet in de uiterlijke versieringen, waren doorslaggevend. De auteurs suggereren dat deze defecten in de binnenkern waarschijnlijk de assemblage of functie van de overgebleven poriën verstoren en stressresponsen in de celwand activeren, waardoor de totale permeabiliteit van het buitenschild voor antibiotica afneemt.
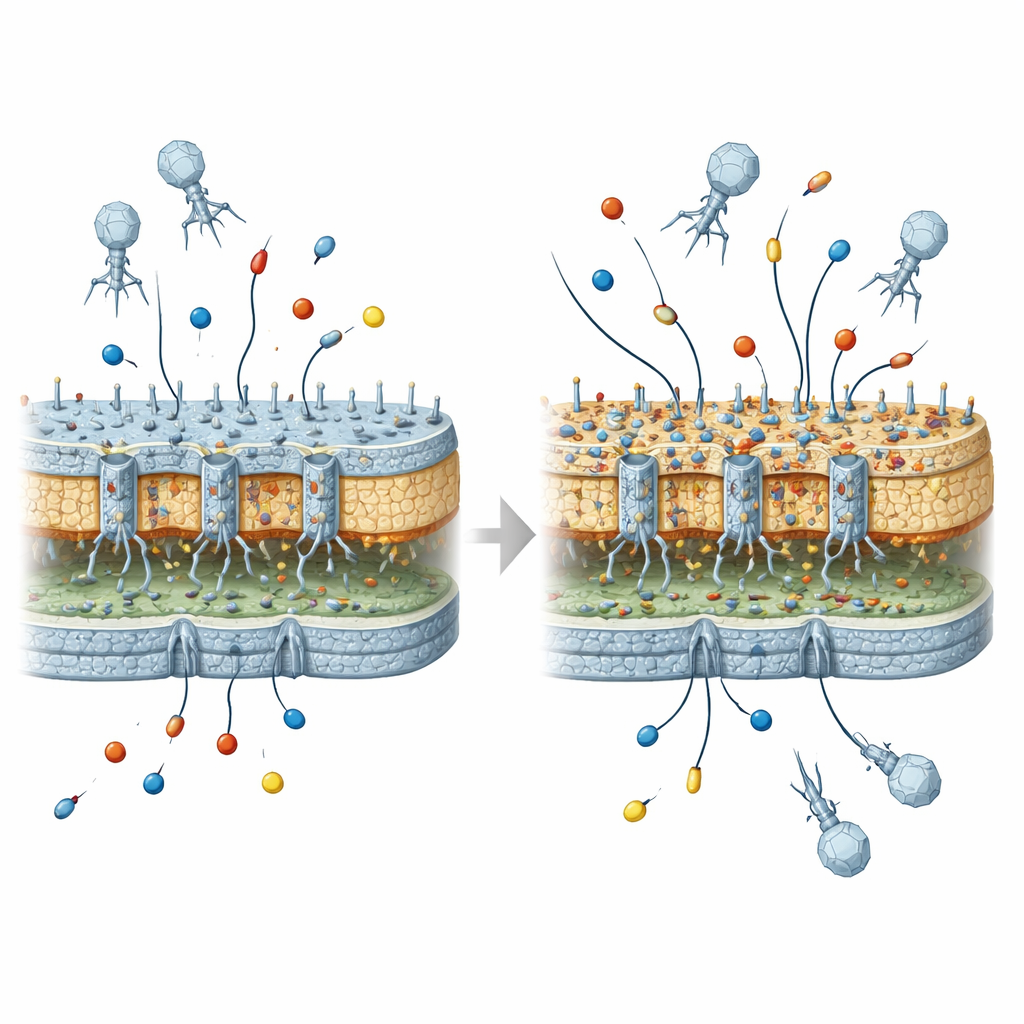
Wat dit betekent voor toekomstige faagbehandelingen
Voor een niet-specialistische lezer is de kernboodschap dat virussen die worden gebruikt om bacteriën te doden onbedoeld het buitenschild van bacteriën kunnen herinrichten op manieren die hen beter voorbereiden om bepaalde antibiotica te weerstaan—mits ze later de juiste resistentie-enzymen opnemen. Op zichzelf creëren de door fagen geselecteerde veranderingen geen sterk medicijnresistente stammen, maar ze vormen een "permissieve" achtergrond die bescheiden resistentiegenen kan omzetten in ernstigere klinische problemen. Nu fagetherapie dichter bij routinematig medisch gebruik komt, pleit dit werk ervoor deze evolutionaire bijeffecten zorgvuldig te overwegen en virale behandelingen te ontwerpen die infecties genezen terwijl het risico dat bacteriën de volgende stap naar antibioticaresistentie zetten tot een minimum wordt beperkt.
Bronvermelding: Le-Boulch, J., Charneau, E., Chevallereau, A. et al. Selection of porin and LPS mutants during infection by phage T4 facilitates the emergence of β-lactam resistance in Escherichia coli. npj Antimicrob Resist 4, 21 (2026). https://doi.org/10.1038/s44259-026-00193-9
Trefwoorden: fagetherapie, antibioticaresistentie, Escherichia coli, beta-lactamases, bacterieel buitenmembraan