Clear Sky Science · es
Selección de mutantes de porina y LPS durante la infección por el fago T4 facilita la aparición de resistencia a β-lactámicos en Escherichia coli
Por qué esto importa en la medicina cotidiana
Los médicos se están quedando sin opciones para tratar infecciones causadas por bacterias difíciles de eliminar, y nuevas ideas como el uso de virus que atacan bacterias, llamados fagos, están ganando atención. Este estudio plantea una pregunta simple pero crucial: cuando usamos estos virus para combatir bacterias, ¿podríamos sin querer facilitar que esas bacterias desarrollen resistencia a los antibióticos, en especial a fármacos potentes como los carbapenémicos que a menudo se usan como último recurso?
La armadura exterior de las bacterias
Muchas bacterias problemáticas, incluida Escherichia coli, están envueltas en una resistente capa externa. Esta cubierta contiene diminutos canales, o poros, que permiten la entrada de nutrientes y también permiten que muchos antibióticos se filtren hacia el interior. Además contiene moléculas azucaradas-grasas conocidas como LPS que ayudan a formar una barrera densa. Tanto los poros como la capa de LPS son esenciales para la supervivencia de la bacteria, pero también sirven como puntos de anclaje para los fagos que las atacan. Dado que las mismas estructuras externas se usan tanto para admitir antibióticos como para admitir fagos, cualquier cambio que proteja a la bacteria de una amenaza puede afectar cómo responde a la otra.
Virus que moldean las defensas bacterianas
Los investigadores se centraron en una cepa de laboratorio bien conocida de E. coli y en un virus clásico que la infecta, llamado T4. Este virus necesita un poro específico (llamado OmpC) y parte del núcleo interno del LPS para adherirse e iniciar la infección. Al exponer grandes poblaciones de bacterias a este virus en distintas condiciones y luego secuenciar el ADN de los supervivientes, el equipo encontró que la resistencia al virus casi siempre implicaba cambios en el poro, en el núcleo interno del LPS o en ambos. A veces también se alteraban sistemas reguladores que controlan la producción de porinas. En todos los casos, el resultado final fue una capa externa remodelada que ya no permitía que el virus se adhiriera con facilidad.
Cuando la resistencia al virus prepara el terreno para la resistencia a fármacos
A continuación, el equipo preguntó cómo se comportaban estas bacterias resistentes al virus cuando se exponían a antibióticos. Por sí solas, la mayoría de las mutaciones que bloqueaban el fago no conferían a las bacterias una resistencia fuerte a β-lactámicos importantes como los carbapenémicos o las cefalosporinas avanzadas. Pero cuando a las bacterias se les dotó de genes para β-lactamasas comunes —moléculas que degradan antibióticos β-lactámicos— surgió un panorama distinto. Un pequeño pero importante subconjunto de mutantes seleccionados por el virus, aquellos con un poro OmpC dañado y un núcleo interno de LPS profundamente alterado, mostraron una supervivencia notablemente mayor frente a fármacos como meropenem, cefepima y ertapenem. Estos niveles seguían por debajo de la resistencia clínica total, pero eran claramente superiores a los de la cepa original que portaba las mismas enzimas.
Reconstruir el mecanismo desde sus cimientos
Para asegurarse de que no se tratara de una coincidencia, los científicos diseñaron mutantes bacterianos precisos con deleciones definidas en el gen de la porina y en genes seleccionados del núcleo del LPS, y luego midieron la eficacia de los carbapenémicos en estos fondos con y sin β-lactamasas. Confirmaron que la pérdida de la porina OmpC junto con la alteración de genes clave del núcleo interno del LPS era suficiente para reproducir el patrón de resistencia observado tras la exposición al virus. Los cambios en el núcleo interno, no las decoraciones externas, fueron críticos. Los autores sugieren que estos defectos del núcleo interno probablemente alteran el ensamblaje o la función de las porinas restantes y desencadenan respuestas de estrés en la envoltura celular, reduciendo en conjunto la permeabilidad de la capa externa a los antibióticos.
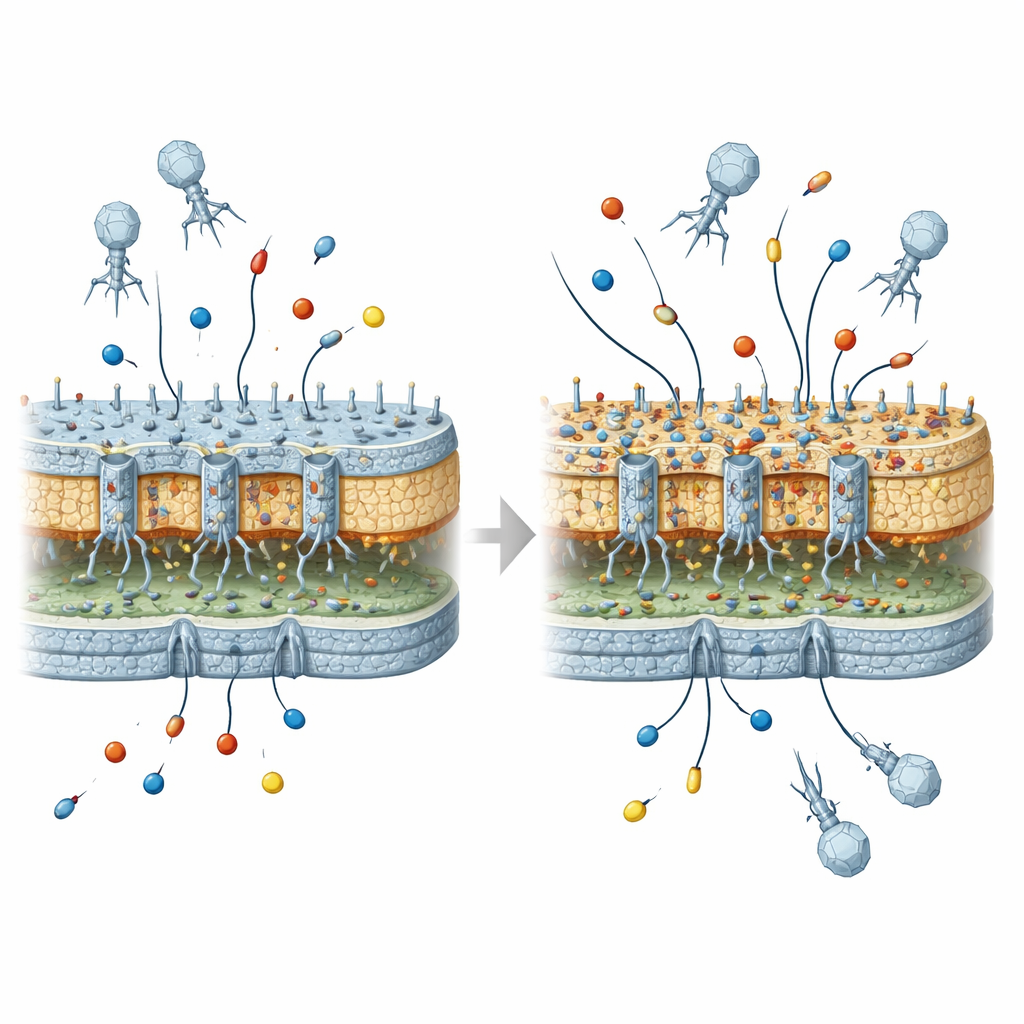
Qué implica esto para futuros tratamientos con fagos
Para un lector no especializado, el mensaje central es que los virus usados para matar bacterias pueden, sin querer, remodelar la armadura externa de las bacterias de maneras que las preparan mejor para resistir ciertos antibióticos, siempre que luego adquieran las enzimas de resistencia adecuadas. Por sí solos, los cambios seleccionados por el virus no crean cepas altamente resistentes a los fármacos, pero generan un trasfondo “permisivo” que puede convertir genes de resistencia modestos en problemas clínicos más serios. A medida que la terapia con fagos se acerca a un uso médico más rutinario, este trabajo sostiene que debemos considerar cuidadosamente estos efectos evolutivos secundarios y diseñar tratamientos con virus que curen infecciones minimizando el riesgo de ayudar a las bacterias a dar el siguiente paso hacia la resistencia a antibióticos.
Cita: Le-Boulch, J., Charneau, E., Chevallereau, A. et al. Selection of porin and LPS mutants during infection by phage T4 facilitates the emergence of β-lactam resistance in Escherichia coli. npj Antimicrob Resist 4, 21 (2026). https://doi.org/10.1038/s44259-026-00193-9
Palabras clave: terapia con fagos, resistencia a antibióticos, Escherichia coli, beta-lactamasas, membrana externa bacteriana