Clear Sky Science · he
בחירה במוטנטים של פורין ו-LPS במהלך זיהום על ידי הפאג T4 מקלה על הופעת עמידות לבטא-לקטמים ב-Escherichia coli
מדוע זה חשוב לרפואה היומיומית
הרופאים מתקרבים למחסור באופציות לטיפול בזיהומים הנגרמים על ידי חיידקים שקשה להשמיד, ורעיונות חדשים כמו שימוש בנגיפים התוקפים חיידקים — פאגים — זוכים לתשומת לב. המחקר הזה שואל שאלה פשוטה אך קריטית: כאשר אנו משתמשים בנגיפים כאלה כדי להילחם בחיידקים, האם באפשרותנו בשוגג להקל על הפיכת החיידקים לעמידים לאנטיביוטיקות, במיוחד תרופות חזקות כמו קרבאפנים המשמשות לעתים קרובות כקו אחרון?
שריון החיצוני של החיידקים
רבים מהחיידקים הבעייתיים, כולל Escherichia coli, עטופים במעטפת חיצונית חזקה. מעטפת זו מכילה ערוצי מיקרו, או נקבים, שמאפשרים כניסת מזון וגם מאפשרים לכניסתן של אנטיביוטיקות רבות. היא כוללת גם מולקולות סוכר-שומן הנקראות LPS שתורמות ליצירת מחסום צפוף. גם הנקבים וגם שכבת ה-LPS חיוניים להישרדות החיידק — אך בו בזמן משמשים גם כאתרי ניחוש לפאגים התוקפים. מכיוון שהמבנים החיצוניים האלה משמשים הן לכניסת אנטיביוטיקות והן לכניסת פאגים, כל שינוי שמגן על החיידקים מפני איום אחד עלול להשפיע על תגובתם לאחר.
נגיפים שמעצבים את ההגנות החיידקיות
החוקרים התמקדו בזן מעבדה ידוע של E. coli ובנגיף קלאסי המדביק אותו, שנקרא T4. נגיף זה זקוק לנקב ספציפי (OmpC) ולחלק מהליבה הפנימית של ה-LPS כדי להיצמד ולהשיק זיהום. על ידי חשיפת כמות גדולה של חיידקים לנגיף בתנאים שונים ולאחר רצף של דגימת ה-DNA של שורדים, מצאו החוקרים כי עמידות לנגיף כמעט תמיד כללה שינויים בנקב, בליבת ה-LPS הפנימית, או בשניהם. לעתים שונו גם מערכות רגולטוריות השולטות בייצור הנקבים. בכל המקרים, התוצאה הייתה עיצוב מחדש של המעטפת החיצונית שחוסמת כיום את היצמדות הנגיף בקלות.
כשעמידות לנגיף מציתה את הבסיס לעמידות לתרופות
בהמשך שאלו החוקרים כיצד החיידקים העמידים לנגיף מתנהגים מול אנטיביוטיקות. בפני עצמן, רוב המוטציות שחסמו את הפאג לא הפכו את החיידקים לעמידים באופן חזק לאנטיביוטיקות בסדרת ה-β-לקטמים כגון קרבאפנים או צפלוספורינים מתקדמים. אך כשהחיידקים קיבלו גנים המקודדים לבטא-לקטמאזות שכיחות — אנזימים שמפרקים אנטיביוטיקות β-לקטמיות — התמונה השתנתה. תת-קבוצה קטנה אך חשובה של מוטנטים שנבחרו על ידי הנגיף, אלה שסבלו גם מנקב OmpC פגום וגם מליבת LPS פנימית מועדת לשינוי עמוק, הראתה הישרדות גבוהה במידה ניכרת מול תרופות כמו מרופנאם, צפפימם וארטפנאם. רמות אלה עדיין היו מתחת לסף עמידות קלינית מלאה, אך היו בולטות יותר מהזן המקורי הנושא את אותם אנזימים.
שחזור המנגנון מאפס
כדי לוודא שמדובר לא במקרה, המדענים הנדסו מוטנטים חיידקיים מדויקים עם מחיקות מוגדרות בגן הנקב ובגנים נבחרים של ליבת ה-LPS, ואז מדדו עד כמה קרבאפנים יעילים ברקעים אלה עם ובלי בטא-לקטמאזות. הם אישרו שאיבוד נקב OmpC יחד עם פגיעה בגנים פנימיים מרכזיים של ה-LPS מספיקים כדי לחקות את דפוס העמידות שנצפה לאחר חשיפה לנגיף. שינויים בליבת ה-LPS, ולא בקישוטים החיצוניים, היו קריטיים. המחברים מציעים כי פגמים בליבה הפנימית ככל הנראה מחריגים את ההרכבה או את תפקוד הנקבים שנותרו ומפעילים תגובות לחץ במעטפת התאית, הכוללות הפחתת חדירות כללית של המעטפת החיצונית לאנטיביוטיקה.
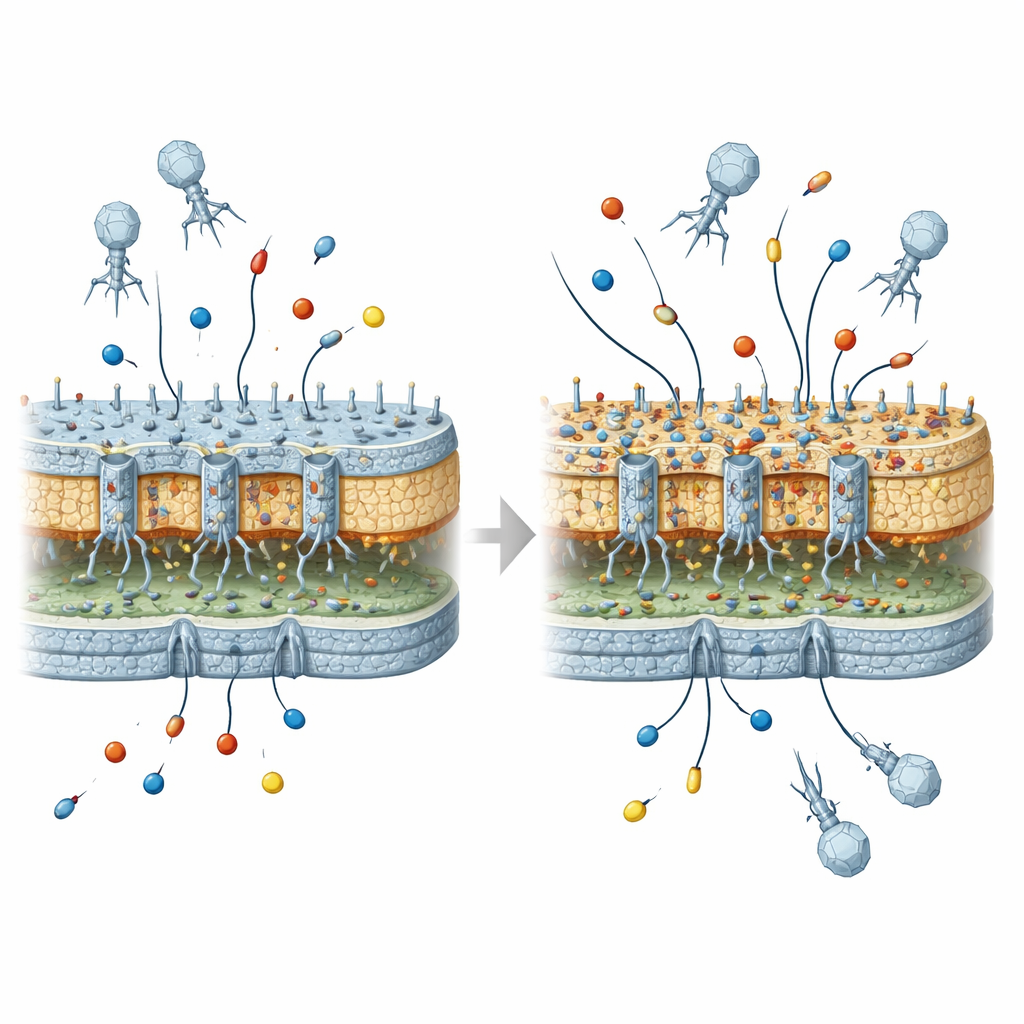
מה משמעות הדבר לטיפולי פאג בעתיד
לקריאה שאינה מקצועית, המסר המרכזי הוא שנגיפים המשמשים להריגת חיידקים יכולים, בלי משים, לעצב מחדש את שריון החיידקים בדרכים שעוזרות להם לעמוד מול אנטיביוטיקות מסוימות — בתנאי שאחר כך הם רוכשים את האנזימים המתאימים לעמידות. כשלעצמם, השינויים שנבחרו על ידי הנגיף אינם יוצרים זנים בעלי עמידות תרופתית גבוהה, אך הם יוצרים רקע "מאפשר" שיכול להפוך גני עמידות צנועים לבעיה קלינית משמעותית יותר. ככל שטיפול בפאגים מתקדם לשימוש שגרתי במרפאות, עבודה זו טוענת שעלינו לשקול בקפידה את התופעות האבולוציוניות הללו, ולעצב טיפולי נגיפים שמרפאים זיהומים תוך הפחתת הסיכון שנעזור לחיידקים לעשות את הצעד הבא לעמידות לאנטיביוטיקה.
ציטוט: Le-Boulch, J., Charneau, E., Chevallereau, A. et al. Selection of porin and LPS mutants during infection by phage T4 facilitates the emergence of β-lactam resistance in Escherichia coli. npj Antimicrob Resist 4, 21 (2026). https://doi.org/10.1038/s44259-026-00193-9
מילות מפתח: טיפולי פאגים, עמידות לאנטיביוטיקה, Escherichia coli, בטא-לקטמאזות, ממברנת החיידק החיצונית