Clear Sky Science · zh
肝细胞表观遗传学在代谢功能障碍相关脂肪性肝病发病中的作用
这个肝脏故事为何与你相关
代谢功能障碍相关脂肪性肝病(MASLD)影响了全球近三分之一的人口,并与肥胖、2 型糖尿病和心脏病密切相关。大多数人在明显症状出现之前不会察觉,往往等到严重损伤已发生才被发现。本文综述了一个快速发展的研究领域,提出了一个简单而有力的问题:肝细胞内基因上的化学“开关”如何推动脂肪肝的发生,这些开关能否被重置以预防或治疗该病?
从简单脂肪堆积到严重肝纤维化
MASLD 是一个广泛的术语,涵盖从肝脏轻度脂肪堆积到炎症、瘢痕形成、肝硬化乃至肝癌的一系列病况。该病通过遗传易感、饮食、肠道微生物以及胰岛素抵抗等代谢问题的综合作用发展而来。经典模型描述了最初的“打击”,即过量热量和激素促使脂肪进入肝细胞,随后发生额外的“打击”,如氧化应激和慢性炎症,导致这些细胞受损和死亡。更新的“多重打击”思路增加了更多层面,包括肝细胞与免疫细胞及成纤维细胞之间的通信。在这些影响因素中,表观遗传学已成为连接环境与生活方式与肝细胞行为之间的关键桥梁。
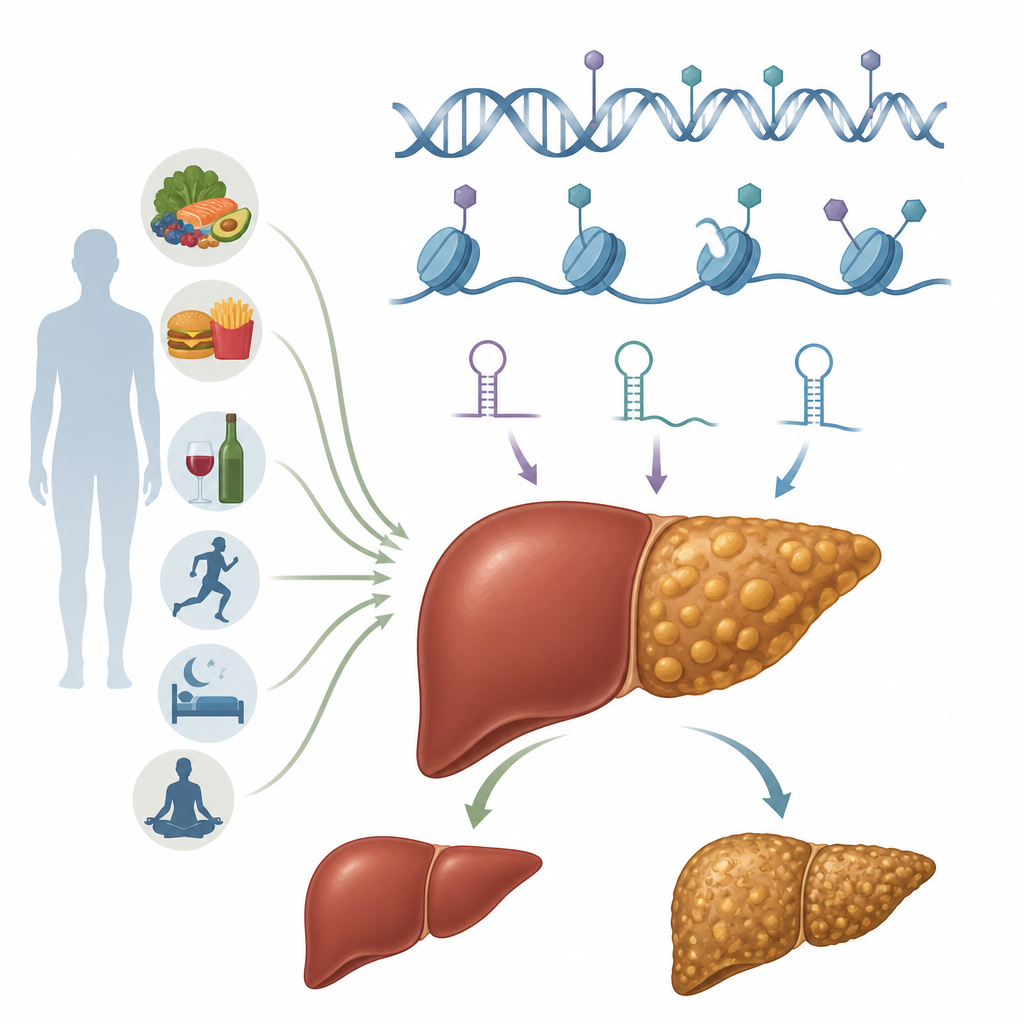
肝细胞中的表观遗传开关
表观遗传学指的是在不改变 DNA 序列的情况下,调整基因使用方式的化学标记和结构性变化。这些标记是可逆的,并可受饮食、代谢状态和毒素影响。在肝细胞这一肝脏主力细胞中,多个表观遗传系统协同工作。DNA 甲基化通过在特定 DNA 位点添加小的化学标签来抑或激活基因。组蛋白修饰改变 DNA 绕组蛋白的缠绕状态,使基因组的某些区域更开放或更紧闭。非编码 RNA(包括微小 RNA 和长链 RNA)则对哪些信息被翻译成蛋白质进行精细调控。额外的层面包括 RNA 自身的化学修饰以及染色质——将遗传物质打包的 DNA–蛋白复合体——的大规模重排。综合起来,这些系统影响肝细胞如何处理脂肪、糖和炎症信号。
这些变化如何推动肝脏走向疾病
综述汇集的证据显示,肝细胞中的特定表观遗传模式倾向于促进脂肪储存、抑制脂肪消耗并加剧炎症。例如,异常的 DNA 甲基化可沉默那些通常支持健康脂肪分解或线粒体功能的基因,同时增强促进脂肪堆积的基因。在实验模型中,高糖和高胆固醇水平会引起跨越数千个基因的 DNA 甲基化变化,从而转移参与脂质代谢的整个网络。组蛋白修饰酶可打开驱动脂肪合成或炎症通路的 DNA 区段,而另一些酶则促进如禁食诱导的脂肪燃烧和细胞清理等保护性程序。非编码 RNA 作为快速响应的调节因子发挥作用:某些微小 RNA 和长链 RNA 促进脂肪积聚和胰岛素抵抗,而另一些则通过抑制脂质生成酶或减弱炎症信号来保护免受脂肪肝影响。
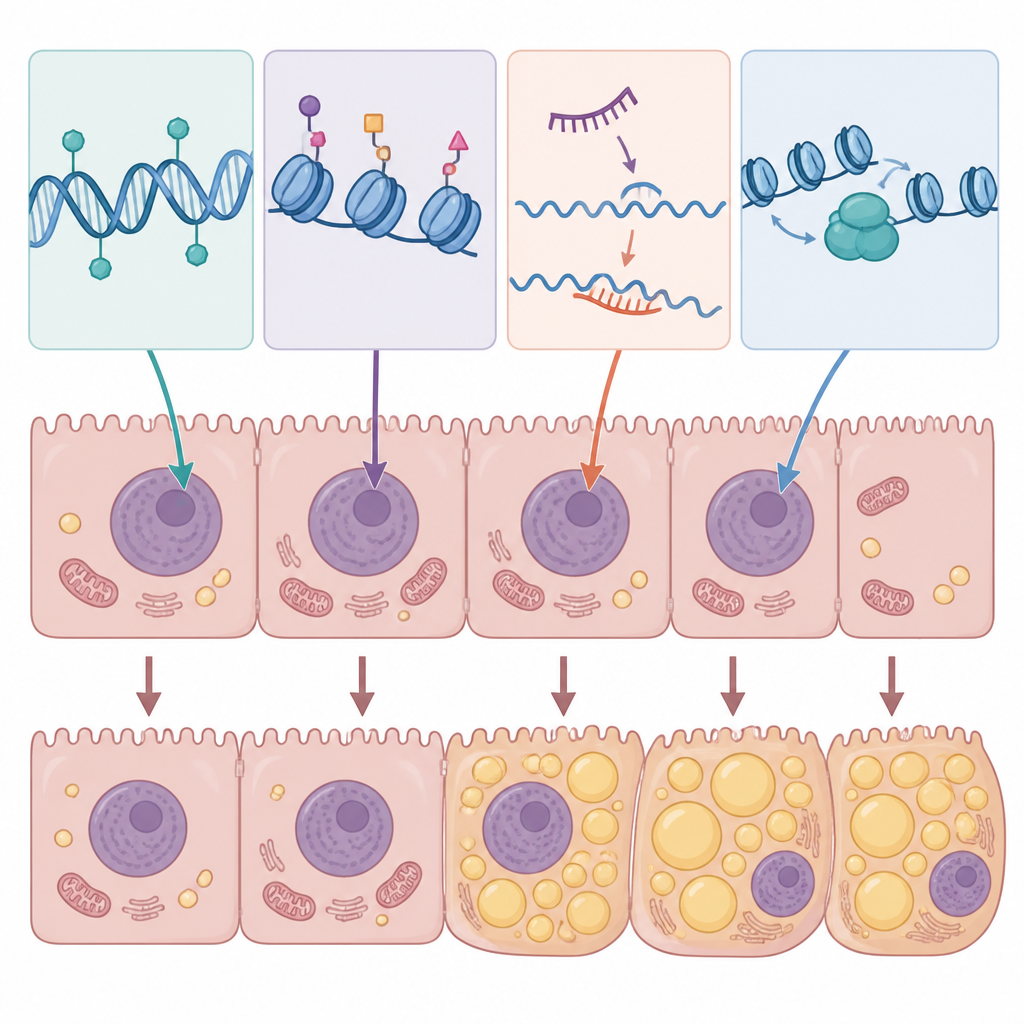
从机制到检测与治疗
由于表观遗传标记既稳定又可逆,它们作为未来诊断工具和药物靶点具有吸引力。一些 DNA 甲基化模式和微RNA 指纹已可在血液中检测到,并且似乎与 MASLD 的严重程度有关,这提出了可能通过简单血检替代部分肝活检的设想。在治疗方面,一些在细胞和动物模型中测试的药物与天然化合物(如白藜芦醇、甜菜碱、黄连素以及某些治疗糖尿病的药物)似乎通过调节肝细胞的表观遗传调控因子而部分改善脂肪肝。与此同时,作者提醒这些“开关”控制着许多器官中的大量基因,因此如果不能精确靶向,广泛作用的药物可能会引发不良副作用。
这项研究可能引向何方
文章的结论是,肝细胞的表观遗传调控在 MASLD 的启动、进展乃至可能的逆转中处于核心地位。通过利用现代单细胞与“组学”工具描绘细胞特异的表观遗传变化,科学家希望确定哪些开关最能预测疾病风险、哪些标志着危险的进展,以及哪些可以被安全地调控。对非专业读者而言,关键的信息是肝脏健康并非由基因单独决定。日常因素如饮食和代谢状态会在肝细胞的 DNA 与 RNA 上留下化学指纹,能够将器官推向健康或疾病。理解并最终调控这些指纹,可能为更早的诊断以及更精准、创伤更小的脂肪肝治疗开辟道路。
引用: Zhu, G., Zhao, Q., Ran, J. et al. The role of hepatocyte epigenetics in the pathogenesis of metabolic dysfunction-associated steatotic liver disease. Commun Med 6, 276 (2026). https://doi.org/10.1038/s43856-026-01651-1
关键词: 脂肪性肝病, 表观遗传学, 肝细胞, DNA 甲基化, 非编码 RNA