Clear Sky Science · fr
Le rôle de l’épigénétique des hépatocytes dans la pathogenèse de la maladie du foie stéatosique associée à un dysfonctionnement métabolique
Pourquoi cette histoire du foie vous concerne
La maladie du foie stéatosique associée à un dysfonctionnement métabolique, ou MASLD, touche près d’une personne sur trois dans le monde et est étroitement liée à l’obésité, au diabète de type 2 et aux maladies cardiovasculaires. La plupart des personnes ne ressentent pas de symptômes évidents avant qu’un dommage sérieux ne se soit déjà produit. Cet article de revue explore un domaine de recherche en plein essor qui pose une question simple mais puissante : comment les « interrupteurs » chimiques appliqués sur nos gènes à l’intérieur des cellules hépatiques contribuent-ils à la stéatose hépatique, et ces interrupteurs peuvent‑ils être réinitialisés pour prévenir ou traiter la maladie ?
De l’accumulation simple de graisses à la cicatrisation sévère du foie
MASLD est un terme large couvrant des états allant d’une accumulation de graisses légère dans le foie à l’inflammation, la fibrose, la cirrhose et même le cancer du foie. La maladie se développe par un mélange de prédispositions héréditaires, d’alimentation, du microbiote intestinal et de troubles métaboliques tels que la résistance à l’insuline. Les modèles classiques décrivent un « premier coup » où l’excès de calories et d’hormones pousse les graisses dans les cellules hépatiques, suivi d’autres « coups » tels que le stress oxydatif et l’inflammation chronique qui blessent et tuent ces cellules. Les approches récentes de type « coups multiples » ajoutent des niveaux supplémentaires, notamment la façon dont les cellules hépatiques communiquent avec les cellules immunitaires et les cellules productrices de tissu cicatriciel. Parmi ces influences, l’épigénétique est apparue comme un pont central reliant l’environnement et le mode de vie au comportement des cellules hépatiques.
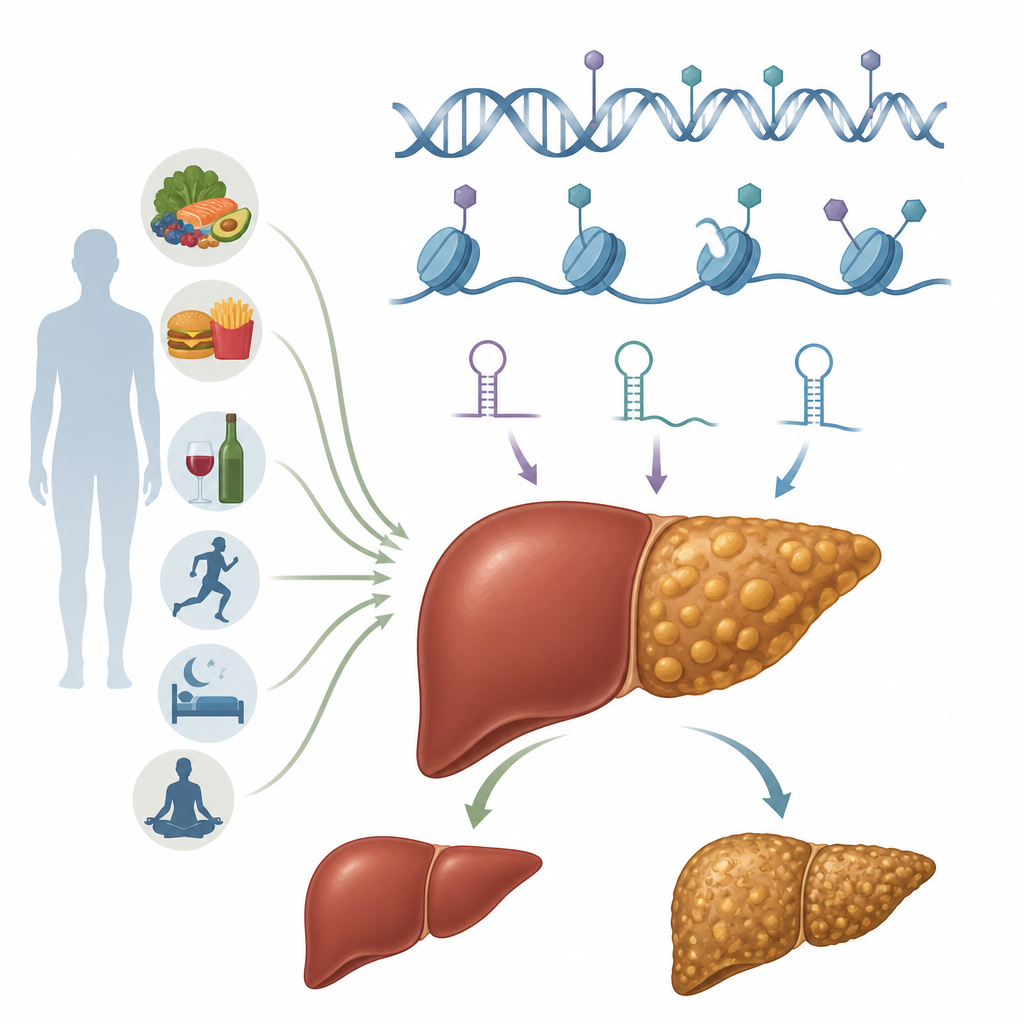
Les interrupteurs épigénétiques dans les cellules hépatiques
L’épigénétique désigne des marques chimiques et des modifications structurelles qui ajustent l’utilisation des gènes sans altérer le code ADN lui‑même. Ces marques sont réversibles et peuvent être modelées par l’alimentation, l’état métabolique et les toxines. Dans les hépatocytes, les cellules actives du foie, plusieurs systèmes épigénétiques agissent de concert. La méthylation de l’ADN peut augmenter ou diminuer l’expression des gènes en ajoutant de petites étiquettes chimiques sur des sites d’ADN spécifiques. Les modifications des histones modifient les « bobines » protéiques autour desquelles l’ADN est enroulé, rendant des régions du génome plus accessibles ou plus compactes. Les ARN non codants, y compris les microARN et les ARN longs, règlent finement quels messages sont traduits en protéines. Des couches supplémentaires comprennent des modifications chimiques de l’ARN lui‑même et des réarrangements à grande échelle de la chromatine, le complexe ADN–protéine qui emballe le matériel génétique. Ensemble, ces systèmes déterminent la façon dont les hépatocytes gèrent les lipides, les sucres et les signaux inflammatoires.
Comment ces changements poussent le foie vers la maladie
La revue compile des preuves selon lesquelles des profils épigénétiques spécifiques dans les hépatocytes favorisent le stockage des graisses, altèrent la combustion des lipides et attisent l’inflammation. Par exemple, une méthylation altérée de l’ADN peut réprimer des gènes qui soutiennent normalement la dégradation saine des graisses ou la fonction mitochondriale, tout en amplifiant des gènes qui encouragent l’accumulation lipidique. Des taux élevés de sucre et de cholestérol dans des modèles expérimentaux entraînent des modifications de la méthylation de l’ADN sur des milliers de gènes, faisant basculer des réseaux entiers impliqués dans le métabolisme lipidique. Les enzymes modifiant les histones peuvent ouvrir des segments d’ADN qui stimulent la synthèse des lipides ou des voies inflammatoires, tandis que d’autres favorisent des programmes protecteurs comme l’oxydation des graisses induite par le jeûne et le nettoyage cellulaire. Les ARN non codants agissent comme des régulateurs à réponse rapide : certains microARN et ARN longs favorisent l’accumulation de graisses et la résistance à l’insuline, tandis que d’autres semblent protéger contre la stéatose en contrôlant les enzymes lipogéniques ou en atténuant la signalisation inflammatoire.
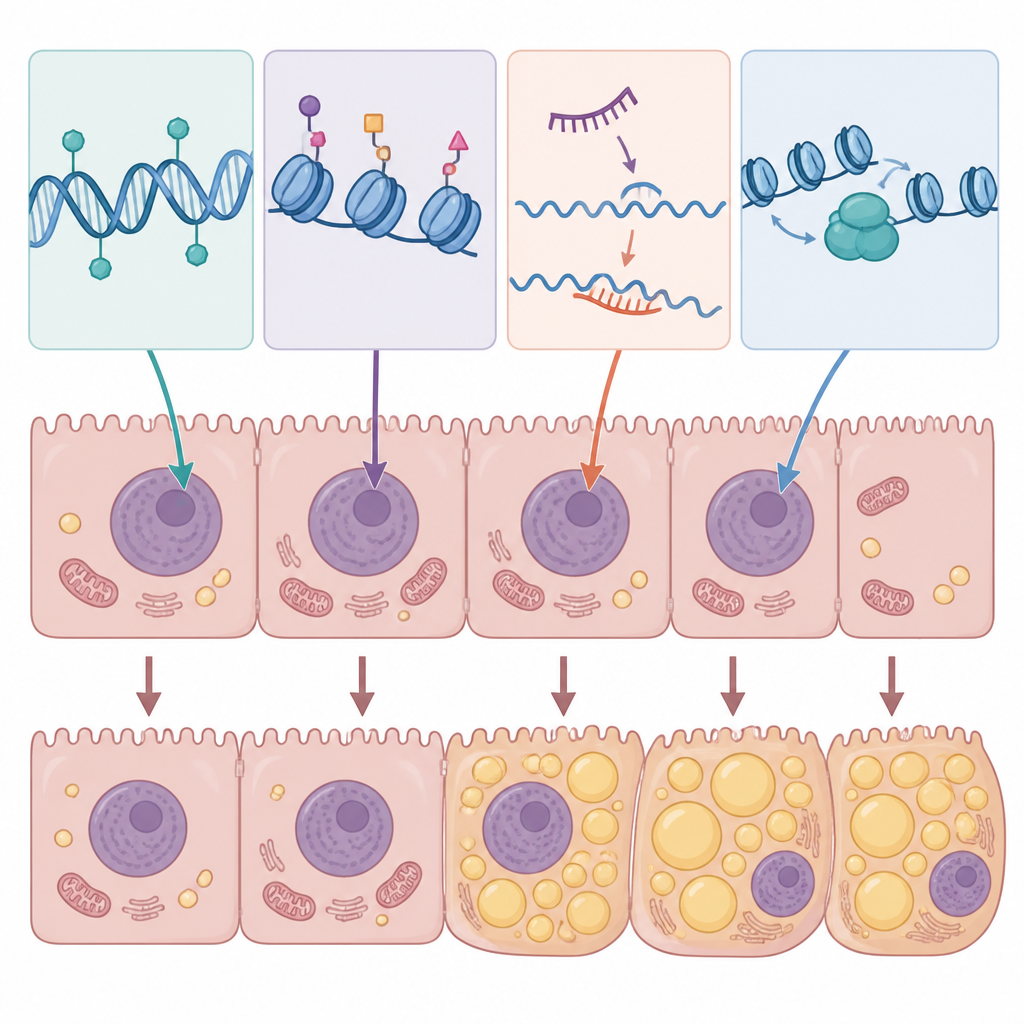
Des mécanismes aux tests et traitements
Parce que les marques épigénétiques sont à la fois stables et réversibles, elles représentent des outils diagnostics et des cibles médicamenteuses prometteuses. Certains profils de méthylation de l’ADN et signatures de microARN peuvent déjà être détectés dans le sang et semblent corréler avec la gravité de la MASLD, ouvrant la possibilité de tests sanguins simples qui éviteraient à certains patients une biopsie hépatique. Côté traitement, plusieurs médicaments et composés naturels testés in vitro et chez l’animal, tels que le resvératrol, la bétaïne, la berbérine et certains antidiabétiques, semblent améliorer partiellement la stéatose en modulant les régulateurs épigénétiques dans les hépatocytes. Les auteurs soulignent toutefois que ces interrupteurs contrôlent de nombreux gènes dans plusieurs organes, si bien que des médicaments à large spectre pourraient provoquer des effets indésirables non souhaités s’ils ne sont pas ciblés avec précision.
Vers où cette recherche peut conduire
L’article conclut que la régulation épigénétique dans les hépatocytes est centrale pour le déclenchement, la progression et éventuellement la réversibilité de la MASLD. En cartographiant les changements épigénétiques spécifiques aux cellules grâce aux outils modernes d’analyse single‑cell et « omics », les chercheurs espèrent identifier quels interrupteurs prédisent le mieux le risque de maladie, lesquels marquent une progression dangereuse et lesquels peuvent être manipulés en toute sécurité. Pour le grand public, le message clé est que la santé du foie n’est pas déterminée par les gènes seuls. Des facteurs quotidiens comme l’alimentation et l’état métabolique laissent des empreintes chimiques sur l’ADN et l’ARN des cellules hépatiques qui peuvent pousser l’organe vers la santé ou la maladie. Comprendre et, à terme, orienter ces empreintes pourrait ouvrir la voie à un diagnostic plus précoce et à des traitements plus précis et moins invasifs pour la maladie du foie gras.
Citation: Zhu, G., Zhao, Q., Ran, J. et al. The role of hepatocyte epigenetics in the pathogenesis of metabolic dysfunction-associated steatotic liver disease. Commun Med 6, 276 (2026). https://doi.org/10.1038/s43856-026-01651-1
Mots-clés: stéatose hépatique, épigénétique, hépatocytes, méthylation de l’ADN, ARN non codants