Clear Sky Science · sv
Hepatocytens epigenetik i patogenesen av metaboliskt dysfunktionsassocierad steatisk leversjukdom
Varför den här leverberättelsen är viktig för dig
Metaboliskt dysfunktionsassocierad steatisk leversjukdom, eller MASLD, drabbar nästan en av tre personer globalt och är starkt kopplad till fetma, typ 2-diabetes och hjärtsjukdomar. De flesta känner inga tydliga symtom förrän allvarliga skador redan har uppstått. Denna översiktsartikel granskar ett snabbt växande forskningsfält som ställer en enkel men kraftfull fråga: hur hjälper kemiska ”strömbrytare” som ligger ovanpå våra gener i leverceller till att driva fettlever, och kan dessa strömbrytare återställas för att förebygga eller behandla sjukdomen?
Från enkel fettansamling till allvarlig leverskada
MASLD är en vid term som täcker tillstånd från lindrig fettansamling i levern till inflammation, ärrbildning, cirros och till och med levercancer. Sjukdomen utvecklas genom en blandning av ärftlig risk, kost, tarmmikrobiota och metabola problem såsom insulinresistens. Klassiska modeller beskriver en initial ”träff” där överskott av kalorier och hormoner skjuter in fett i levercellerna, följt av ytterligare ”träffar” som oxidativ stress och kronisk inflammation som skadar och dödar dessa celler. Nyare tankesätt om flera påfrestningar lägger till fler lager, inklusive hur leverceller kommunicerar med immunceller och ärrbildande celler. Bland dessa influenser har epigenetiken framträtt som en viktig bro som kopplar miljö och livsstil till levercellernas beteende.
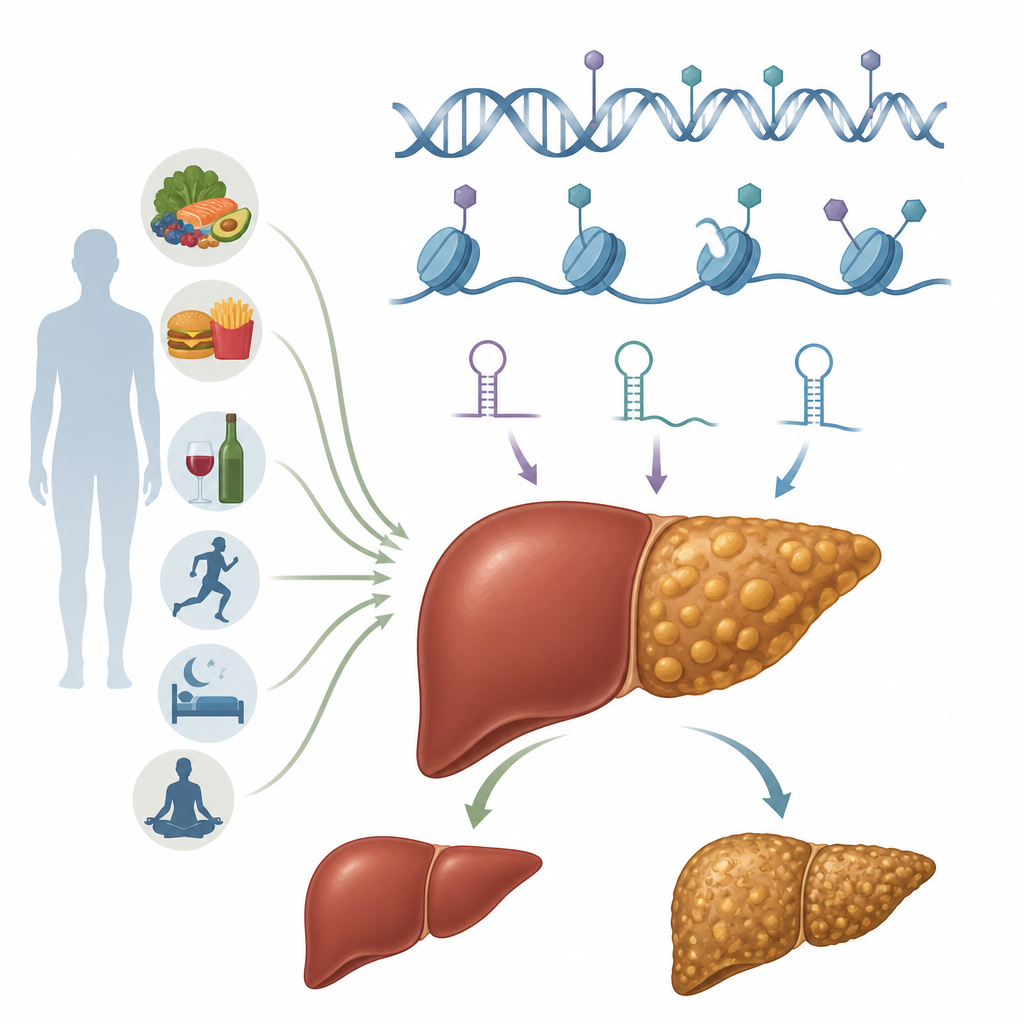
Epigenetiska strömbrytare i leverceller
Epigenetik avser kemiska markörer och strukturella förändringar som justerar hur gener används utan att ändra DNA-koden i sig. Dessa markörer är reversibla och kan formas av kost, metabol status och toxiner. I hepatocyter, leverns arbetsmyror, samarbetar flera epigenetiska system. DNA-metylering kan öka eller minska geners aktivitet genom att placera små kemiska etiketter på specifika DNA-ställen. Histonmodifiering ändrar de proteinnystan kring vilka DNA är lindat och gör delar av genomet mer öppna eller mer slutna. Icke-kodande RNA, inklusive mikroRNA och långa RNA, finjusterar vilka budskap som översätts till proteiner. Ytterligare lager innefattar kemiska förändringar på själva RNA:t och storskaliga omarrangemang av kromatin, DNA–proteinkomplexet som paketerar det genetiska materialet. Tillsammans formar dessa system hur hepatocyter hanterar fett, socker och inflammatoriska signaler.
Hur dessa förändringar driver levern mot sjukdom
Översikten samlar bevis för att specifika epigenetiska mönster i hepatocyter gynnar fettlagring, försämrar fettförbränning och eldar på inflammationen. Till exempel kan förändrad DNA-metylering tysta gener som normalt stödjer hälsosam fettnedbrytning eller mitokondriefunktion, samtidigt som gener som främjar fettansamling stärks. Höga nivåer av socker och kolesterol i experimentella modeller leder till metyleringsförändringar i tusentals gener, vilket förskjuter hela nätverk involverade i lipidmetabolism. Enzymer som modifierar histoner kan öppna upp DNA-avsnitt som driver fettsyntes eller inflammatoriska banor, medan andra främjar skyddande program som fastainducerad fettoxidation och cellulär städning. Icke-kodande RNA fungerar som snabba regulatorer: vissa mikroRNA och långa RNA främjar fettansamling och insulinresistens, medan andra tycks skydda mot steatos genom att begränsa lipogena enzymer eller dämpa inflammatoriska signaler.
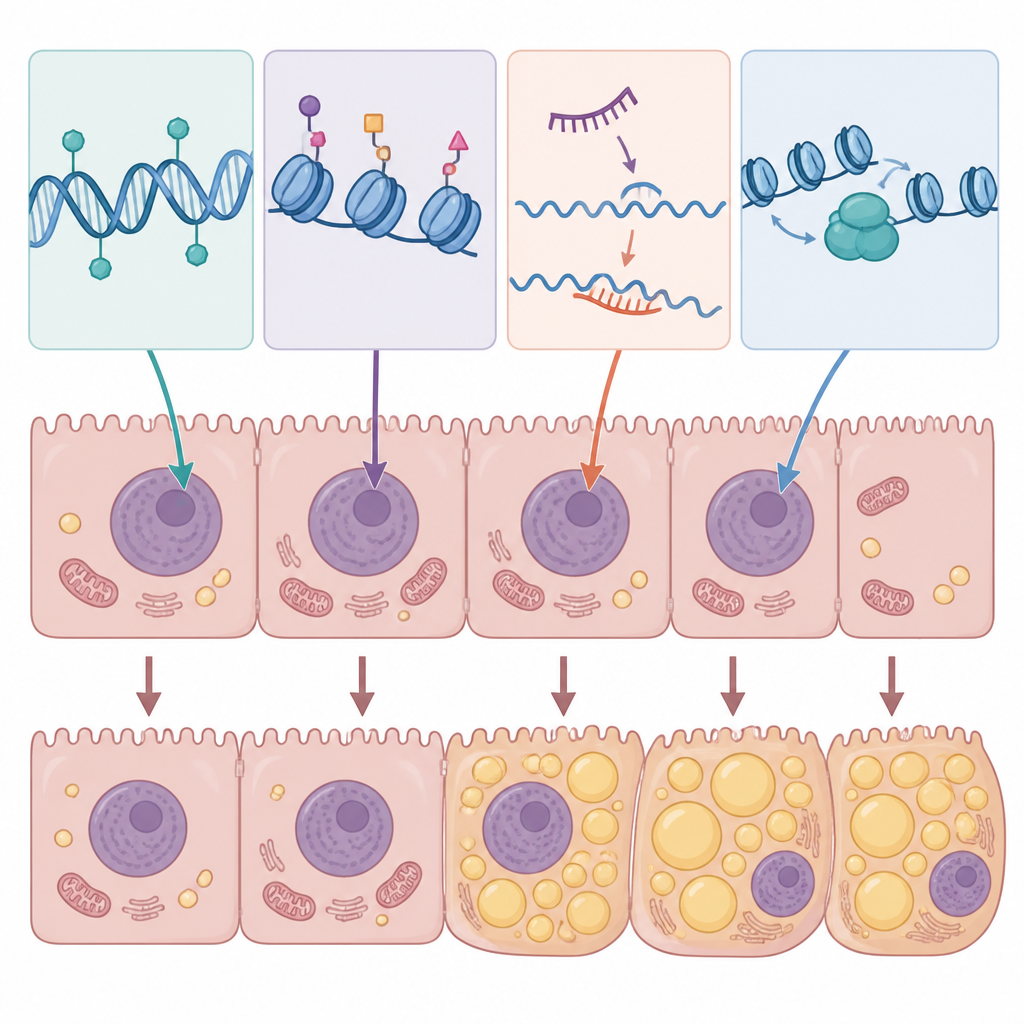
Från mekanismer till tester och behandlingar
Eftersom epigenetiska markörer är både stabila och reversibla är de attraktiva som framtida diagnostiska verktyg och läkemedelsmål. Vissa DNA-metyleringsmönster och mikroRNA-signaturer kan redan upptäckas i blod och verkar korrelera med MASLD:s svårighetsgrad, vilket öppnar för möjligheten till enkla blodprov som kan skona vissa patienter från leverbiopsi. På behandlingssidan tyder flera läkemedel och naturliga föreningar som testats i celler och djurmodeller — såsom resveratrol, betain, berberin och vissa diabetesläkemedel — på att de delvis kan förbättra fettlever genom att påverka epigenetiska regulatorer i hepatocyter. Samtidigt varnar författarna för att dessa strömbrytare styr många gener i flera organ, så bredverkande läkemedel kan ge oönskade biverkningar om de inte riktas noggrant.
Vart denna forskning kan leda
Artikeln avslutar att epigenetisk reglering i hepatocyter är central för hur MASLD börjar, fortskrider och eventuellt kan vändas. Genom att kartlägga cellspecifika epigenetiska förändringar med moderna single-cell- och ”omik”-verktyg hoppas forskare kunna peka ut vilka strömbrytare som bäst förutsäger sjukdomsrisk, vilka som markerar farlig progression och vilka som kan manipuleras säkert. För icke-specialister är huvudbudskapet att leverhälsa inte är fixerad av generna ensam. Vardagliga faktorer såsom kost och metabol status lämnar kemiska fingeravtryck på levercellers DNA och RNA som kan föra organet mot hälsa eller sjukdom. Att förstå och så småningom styra dessa fingeravtryck kan öppna dörren till tidigare diagnos och mer precisa, mindre invasiva behandlingar för fettleversjukdom.
Citering: Zhu, G., Zhao, Q., Ran, J. et al. The role of hepatocyte epigenetics in the pathogenesis of metabolic dysfunction-associated steatotic liver disease. Commun Med 6, 276 (2026). https://doi.org/10.1038/s43856-026-01651-1
Nyckelord: fettleversjukdom, epigenetik, hepatocyter, DNA-metylering, icke-kodande RNA