Clear Sky Science · he
תפקיד האפיגנטיקה של ההפטוציטים בפתוגנזה של מחלת הכבד השומני הקשורה לבלגן מטבולי
למה הסיפור של הכבד הזה חשוב בשבילכם
מחלת הכבד השומני הקשורה לבלגן מטבולי, או MASLD, משפיעה כמעט על אחד מכל שלושה אנשים בעולם והיא קשורה קשר הדוק להשמנת יתר, סוכרת סוג 2 ומחלות לב. רוב האנשים אינם חשים תסמינים ברורים עד שנגרם כבר נזק חמור. מאמר סקירה זה חוקר תחום מחקר המתפתח במהירות ושואל שאלה פשוטה אך חשובה: כיצד "מפסקים" כימיים המצטברים על הגנים בתוך תאי הכבד מסייעים לקידום מחלת הכבד השומני, והאם ניתן לאפס מפסקים אלה כדי למנוע או לטפל בה?
מצטברות שומנית פשוטה לצלקות כבד חמורות
MASLD הוא מונח רחב הכולל מצבים הנעים מהצטברות שומן קלה בכבד עד דלקת, הצטלקות, שחמת ואפילו סרטן כבד. המחלה מתפתחת משילוב של סיכון תורשתי, תזונה, חיידקי מעי ובעיות מטבוליות כגון עמידות לאינסולין. מודלים קלאסיים מתארים "מכה" ראשונית שבה עודפי קלוריות והורמונים דוחפים שומן לתאי הכבד, ואחריה "מכות" נוספות כגון מתח חמצוני ודלקת כרונית שפוגעות בתאים ומובילות למותם. גישות עדכניות של "פגיעות מרובות" מוסיפות שכבות נוספות, כולל האופן שבו תאי הכבד מתקשרים עם תאי חיסון ותאי יצירת צלקת. בין ההשפעות הללו, האפיגנטיקה התגלתה כגשר מרכזי שמקשר בין סביבה ואורח חיים להתנהגות תאי הכבד.
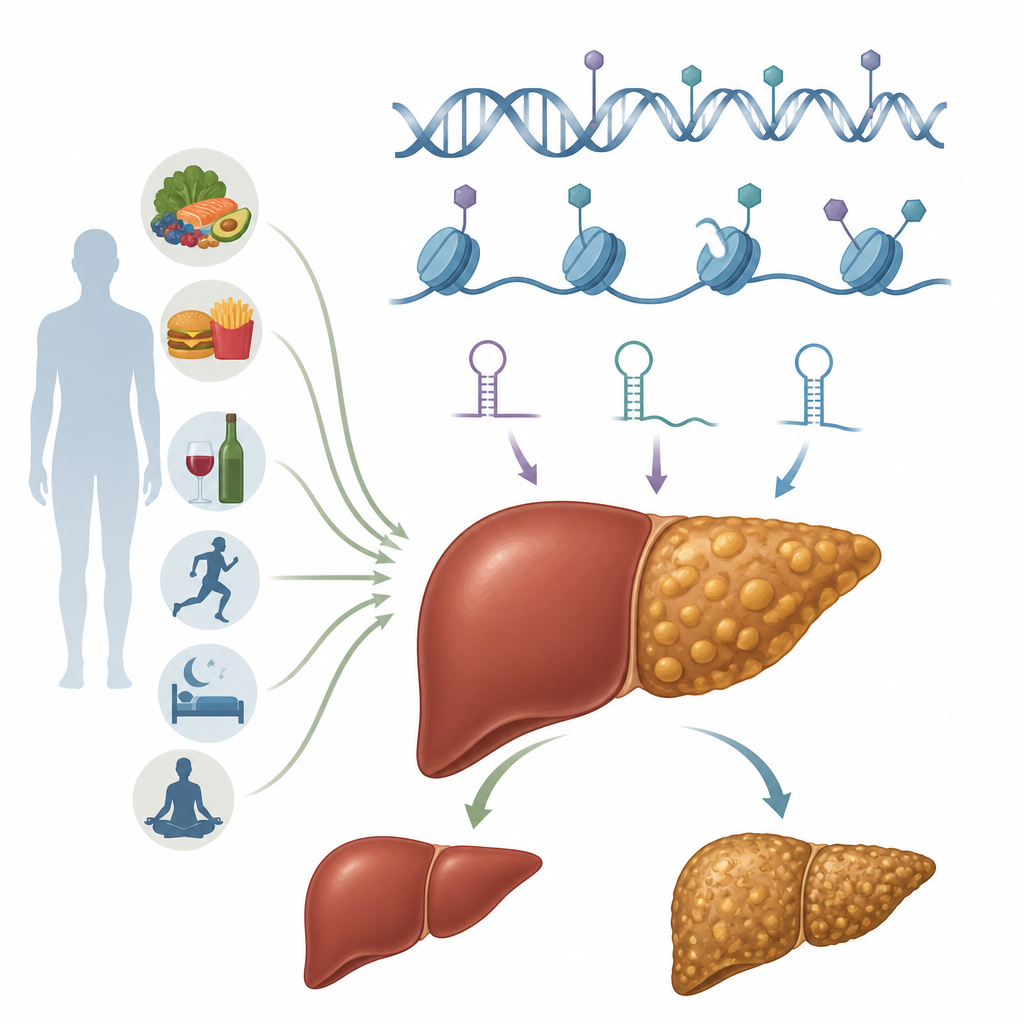
מפסקים אפיגנטיים בתאי הכבד
אפיגנטיקה מתייחסת לסימנים כימיים ושינויים מבניים שמכוונים איך גנים מנוצלים בלי לשנות את רצף ה‑DNA עצמו. סימנים אלה הפיכים ויכולים להיות מעוצבים על ידי תזונה, מצב מטבולי ורעלנים. בהפטוציטים, תאי העבודה של הכבד, פועלים יחד כמה מערכות אפיגנטיות. מתילציה של DNA יכולה להפעיל או לשתק גנים על ידי הצבת תגים כימיים קטנים באתרים ספציפיים ב‑DNA. שינויי היסטונים משנים את גלגלי החלבון סביבם עטוף ה‑DNA, מה שעושה אזורים בגנום פתוחים או סגורים יותר. RNA לא מקודדים, כולל מיקרו‑RNA ו‑long RNA, מווסתים בעדינות אילו מסרים יתורגמו לחלבונים. שכבות נוספות כוללות שינויים כימיים על ה‑RNA עצמו ואתארגנויות בקנה מידה גדול של הכרומטין, קומפלקס ה‑DNA‑חלבון שמארז את החומר הגנטי. יחד מערכות אלה מעצבות כיצד ההפטוציטים מטפלים בשומן, בסוכר ובאותות דלקתיים.
כיצד שינויים אלה דוחפים את הכבד לכיוון מחלה
הסקירה אוספת עדויות שהדפוסים האפיגנטיים הספציפיים בהפטוציטים מעודדים אגירה של שומן, פוגעים בשריפת שומן ומלהיטים דלקת. לדוגמה, מתילציה שונה של DNA יכולה להשתיק גנים שתומכים בדרך כלל בפירוק שומנים בריא או בתפקוד מיטוכונדריאלי, בעוד שהיא מחזקת גנים המעודדים הצטברות שומן. רמות סוכר וכולסטרול גבוהות במודלים ניסיוניים מובילות לשינויים במתילציה של DNA על פני אלפי גנים, ומזיזות רשתות שלמות המעורבות בחילוף חומרים של ליפידים. אנזימי שינוּי היסטונים יכולים לפתוח מקטעים של DNA שמניעים סינתזת שומנים או מסלולי דלקת, בעוד אחרים מקדמים תכניות מגן כגון שריפת שומן בזמן צום וניקוי תאי. RNA לא מקודדים פועלים כמווסתי תגובה מהירה: מיקרו‑RNA ו‑long RNA מסוימים מקדמים הצטברות שומן ועמידות לאינסולין, בעוד שאחרים נראים כמגינים מפני סטטוזיס על ידי עיכוב אנזימי ליפוגנזה או השתקת אותות דלקתיים.
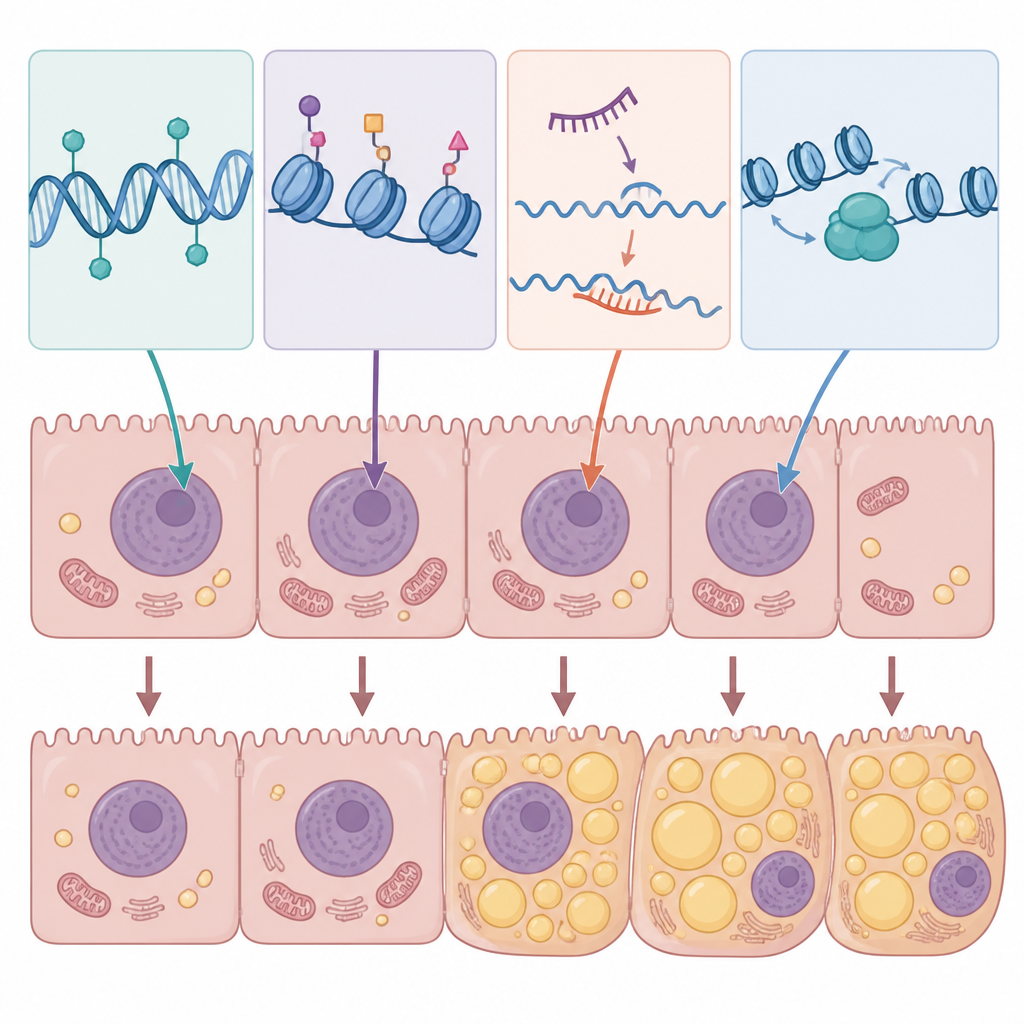
ממנגנונים למבחנים וטיפולים
כיוון שסימנים אפיגנטיים יציבים אך גם הפיכים, הם מושכים בתור כלים אבחוניים עתידיים ויעדים תרופתיים. דפוסי מתילציה של DNA וחתימות מיקרו‑RNA מסוימים כבר ניתנים לזיהוי בדם ונראים כמסתנכרנים עם חומרת MASLD, מה שמעלה את האפשרות למבחני דם פשוטים שעשויים לחסוך לחלק מהמטופלים ביופסיית כבד. בתחום הטיפול, מספר תרופות ומרכיבים טבעיים שנבדקו בתאים ובמודלים של בעלי חיים — כגון רזברטרול, בטאין, ברברין וחלק מתרופות הסוכרת — נראים משפרים חלקית את הכבד השומני על ידי התאמת מבקרי אפיגנטיקה בהפטוציטים. עם זאת, המחברים מזהירים שמפסקים אלה שולטים בהרבה גנים במספר איברים, ולכן תרופות בעלות יעילות רחבה עלולות לגרום לתופעות לוואי בלתי רצויות אם לא יופנו במדויק.
לאן מחקר זה עשוי להוביל
המאמר מסכם שהוויסות האפיגנטי בהפטוציטים הוא מרכזי לאופן שבו MASLD מתחילה, מתקדמת ואולי גם יכולה להתהפך. על ידי מיפוי שינויים אפיגנטיים ספציפיים לתא בעזרת כלים מודרניים של סינגל‑סל והום‑אומיקס, מדענים מקווים לזהות אילו מפסקים מנבאים הכי טוב את סיכון המחלה, אילו מהם מסמנים התקדמות מסוכנת ואילו אפשר לתמרן בבטחה. עבור הלא‑מומחים, המסר המרכזי הוא שכבר לא רק הגנים מחליטים על בריאות הכבד. גורמים יומיומיים כגון תזונה ומצב מטבולי משאירים טביעות כימיות על DNA ו‑RNA של תאי הכבד שיכולות לדחוף את האיבר לכיוון בריאות או מחלה. הבנת טביעות אלה ובהמשך היכולת להנחות אותן עשויות לפתוח דלת לאבחון מוקדם וטיפולים מדויקים, פחות פולשניים למחלת הכבד השומני.
ציטוט: Zhu, G., Zhao, Q., Ran, J. et al. The role of hepatocyte epigenetics in the pathogenesis of metabolic dysfunction-associated steatotic liver disease. Commun Med 6, 276 (2026). https://doi.org/10.1038/s43856-026-01651-1
מילות מפתח: מחלת כבד שומני, אפיגנטיקה, הפטוציטים, מתילציה של DNA, RNA לא מקודד