Clear Sky Science · de
Die Rolle der Hepatozyten-Epigenetik in der Pathogenese der metabolisch-dysfunktionsassoziierten steatotischen Lebererkrankung
Warum diese Lebergeschichte für Sie wichtig ist
Die metabolisch-dysfunktionsassoziierte steatotische Lebererkrankung (MASLD) betrifft weltweit fast eine von drei Personen und steht in engem Zusammenhang mit Adipositas, Typ-2-Diabetes und Herz-Kreislauf-Erkrankungen. Die meisten Betroffenen zeigen lange keine deutlichen Symptome, bis bereits erheblicher Schaden entstanden ist. Dieser Übersichtsartikel beleuchtet ein schnell wachsendes Forschungsfeld, das eine einfache, aber wirkungsvolle Frage stellt: Wie tragen chemische "Schalter", die auf unseren Genen in Leberzellen liegen, zur Entstehung der Fettleber bei — und lassen sich diese Schalter zurücksetzen, um die Erkrankung zu verhindern oder zu behandeln?
Von einfacher Fettansammlung bis zur schweren Lebervernarbung
MASLD ist ein Sammelbegriff für Zustände von milder Fettablagerung in der Leber über Entzündung, Vernarbung, Zirrhose bis hin zu Leberkrebs. Die Erkrankung entsteht aus einer Mischung von erblichen Risiken, Ernährung, Darmmikrobiota und Stoffwechselstörungen wie Insulinresistenz. Klassische Modelle beschreiben einen anfänglichen "Treffer", bei dem überschüssige Kalorien und Hormone Fett in Hepatozyten drücken, gefolgt von weiteren "Treffern" wie oxidativem Stress und chronischer Entzündung, die diese Zellen schädigen und abtöten. Neuere Konzepte mit mehreren Schlaglichtern fügen weitere Ebenen hinzu, etwa wie Leberzellen mit Immunzellen und narbenbildenden Zellen kommunizieren. Unter diesen Einflüssen hat sich die Epigenetik als wichtige Brücke herauskristallisiert, die Umwelt und Lebensstil mit dem Verhalten der Leberzellen verbindet.
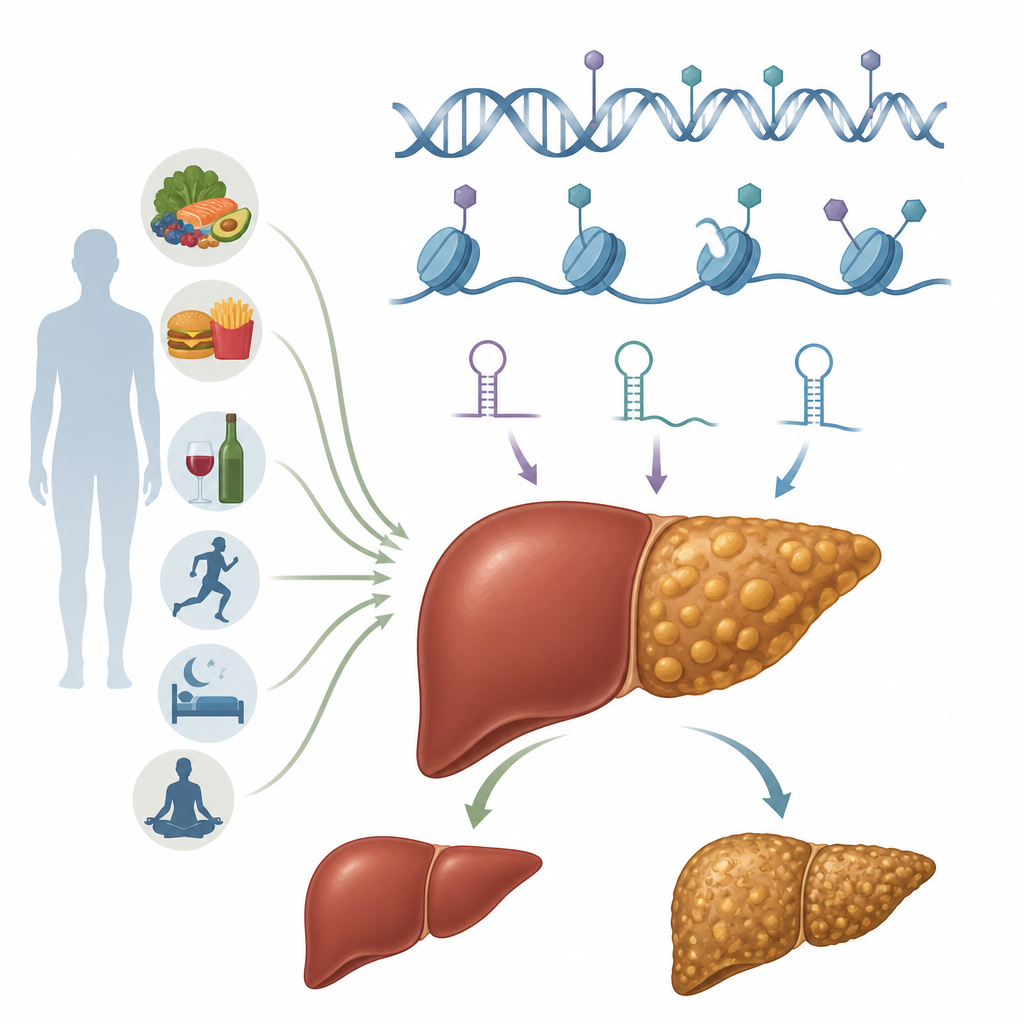
Epigenetische Schalter in Leberzellen
Epigenetik bezeichnet chemische Markierungen und strukturelle Veränderungen, die steuern, wie Gene genutzt werden, ohne die DNA-Sequenz selbst zu verändern. Diese Markierungen sind reversibel und können durch Ernährung, Stoffwechselstatus und Toxine beeinflusst werden. In Hepatozyten, den Arbeitspferden der Leber, greifen mehrere epigenetische Systeme ineinander. DNA-Methylierung kann Gene an- oder abschalten, indem kleine chemische Gruppen an bestimmte DNA-Stellen angefügt werden. Histonmodifikationen verändern die Proteinspulen, um die herum die DNA gewickelt ist, und machen Genomregionen offener oder geschlossener. Nicht-kodierende RNAs, darunter MicroRNAs und lange nicht-kodierende RNAs, justieren fein, welche Botschaften in Proteine übersetzt werden. Weitere Ebenen umfassen chemische Veränderungen an RNA selbst und großskalige Umordnungen des Chromatins, des DNA–Protein-Komplexes, der das genetische Material verpackt. Zusammen formen diese Systeme, wie Hepatozyten mit Fett, Zucker und Entzündungssignalen umgehen.
Wie diese Veränderungen die Leber in Richtung Krankheit treiben
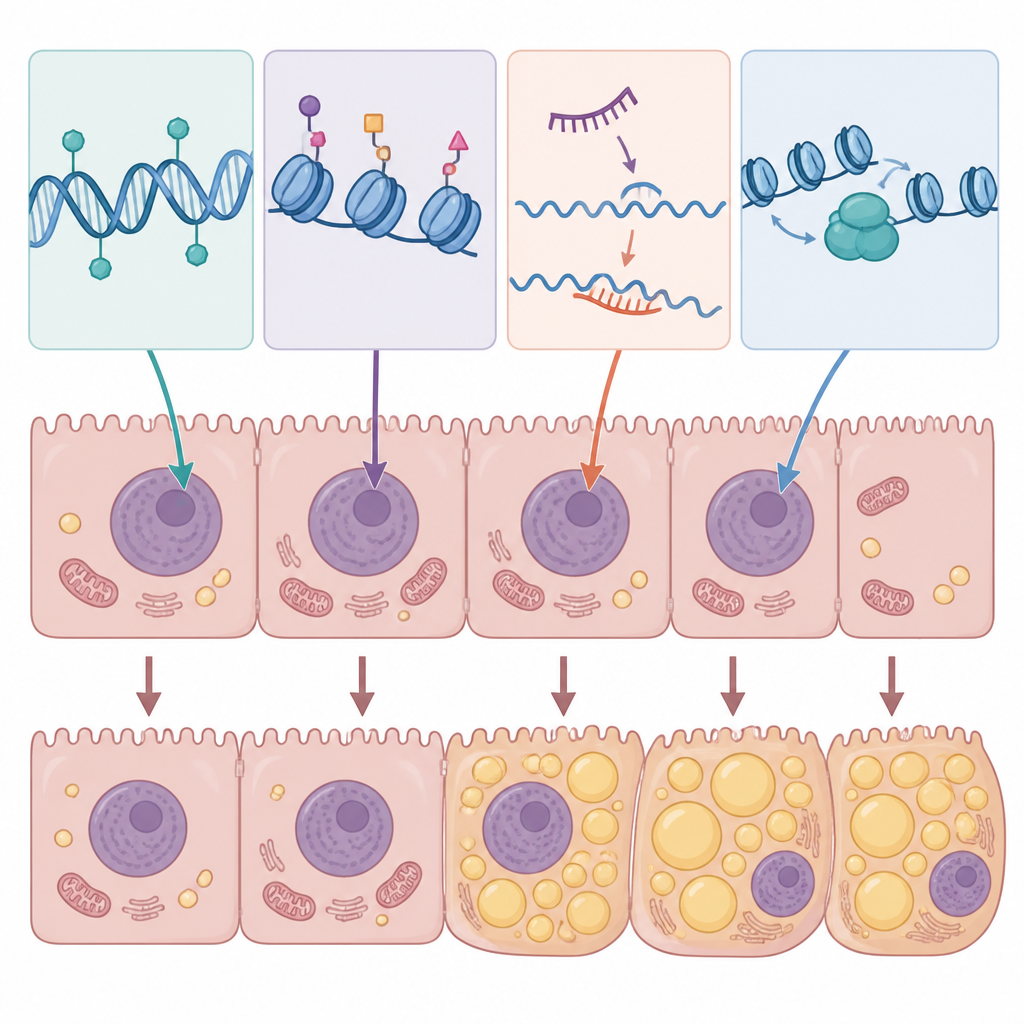
Die Übersicht fasst Hinweise zusammen, dass spezifische epigenetische Muster in Hepatozyten Fettablagerung begünstigen, die Fettverbrennung behindern und Entzündungen anheizen. Beispielsweise kann veränderte DNA-Methylierung Gene stummschalten, die normalerweise eine gesunde Fettverwertung oder mitochondriale Funktion unterstützen, während gleichzeitig Gene gefördert werden, die Fettansammlung begünstigen. Hohe Zucker- und Cholesterinwerte in experimentellen Modellen führen zu DNA-Methylierungsänderungen über Tausende Gene hinweg und verschieben ganze Netzwerke der Lipidstoffwechselregulation. Enzyme, die Histone modifizieren, können DNA-Abschnitte öffnen, die Fettsynthese oder entzündliche Signalwege antreiben, während andere schützende Programme wie fasteninduzierte Fettverbrennung und zelluläre Aufräumprozesse fördern. Nicht-kodierende RNAs fungieren als Schnellregulatoren: bestimmte MicroRNAs und lange RNAs fördern Fettansammlung und Insulinresistenz, andere scheinen vor Steatose zu schützen, indem sie lipogene Enzyme hemmen oder entzündliche Signalübertragung dämpfen.
Von Mechanismen zu Tests und Therapien
Weil epigenetische Markierungen zugleich stabil und reversibel sind, sind sie vielversprechend als zukünftige diagnostische Werkzeuge und Arzneimittelziele. Einige DNA-Methylierungsmuster und MicroRNA-Signaturen lassen sich bereits im Blut nachweisen und korrelieren offenbar mit dem Schweregrad der MASLD, was die Möglichkeit einfacher Bluttests eröffnet, die manche Patientinnen und Patienten von einer Leberbiopsie entbinden könnten. Auf der therapeutischen Seite scheinen mehrere in Zell- und Tiermodellen getestete Medikamente und Naturstoffe — etwa Resveratrol, Betaïn, Berberin und bestimmte Diabetesmedikamente — die Fettleber zum Teil zu verbessern, indem sie epigenetische Regulatoren in Hepatozyten beeinflussen. Gleichzeitig warnen die Autoren, dass diese Schalter viele Gene in verschiedenen Organen steuern; breit wirkende Substanzen könnten daher unerwünschte Nebenwirkungen haben, wenn sie nicht gezielt eingesetzt werden.
Wohin diese Forschung führen könnte
Der Artikel schließt mit der Feststellung, dass die epigenetische Regulierung in Hepatozyten zentral dafür ist, wie MASLD beginnt, fortschreitet und möglicherweise rückgängig gemacht werden kann. Durch die Kartierung zellspezifischer epigenetischer Veränderungen mit modernen Einzelzell- und "Omics"-Werkzeugen hoffen Forschende, jene Schalter zu identifizieren, die am besten das Erkrankungsrisiko vorhersagen, jene, die gefährliche Progression markieren, und jene, die sicher manipuliert werden können. Für Nicht-Spezialisten lautet die Kernbotschaft: Lebergesundheit ist nicht allein durch Gene festgelegt. Alltägliche Einflüsse wie Ernährung und Stoffwechsellage hinterlassen chemische Fingerabdrücke auf DNA und RNA der Leberzellen, die das Organ in Richtung Gesundheit oder Krankheit schieben können. Das Verstehen und letztlich das gezielte Beeinflussen dieser Fingerabdrücke könnte den Weg zu früherer Diagnose und präziseren, weniger invasiven Behandlungen der Fettlebererkrankung eröffnen.
Zitation: Zhu, G., Zhao, Q., Ran, J. et al. The role of hepatocyte epigenetics in the pathogenesis of metabolic dysfunction-associated steatotic liver disease. Commun Med 6, 276 (2026). https://doi.org/10.1038/s43856-026-01651-1
Schlüsselwörter: Fettlebererkrankung, Epigenetik, Hepatozyten, DNA-Methylierung, nicht-kodierende RNA