Clear Sky Science · es
El papel de la epigenética de los hepatocitos en la patogenia de la enfermedad hepática esteatósica asociada a la disfunción metabólica
Por qué esta historia del hígado te importa
La enfermedad hepática esteatósica asociada a la disfunción metabólica, o MASLD, afecta a casi una de cada tres personas en el mundo y está estrechamente vinculada a la obesidad, la diabetes tipo 2 y las enfermedades cardiovasculares. La mayoría de las personas no presentan síntomas claros hasta que ya se ha producido un daño serio. Este artículo de revisión explora un campo de investigación en rápido desarrollo que plantea una pregunta simple pero poderosa: ¿cómo ayudan los “interruptores” químicos superpuestos sobre nuestros genes dentro de las células hepáticas a impulsar la enfermedad del hígado graso, y se pueden reconfigurar esos interruptores para prevenirla o tratarla?
Del simple acúmulo de grasa a la cicatrización hepática grave
MASLD es un término amplio que abarca condiciones que van desde un ligero acúmulo de grasa en el hígado hasta inflamación, formación de cicatrices, cirrosis e incluso cáncer hepático. La enfermedad se desarrolla por una mezcla de riesgo hereditario, dieta, microbiota intestinal y problemas metabólicos como la resistencia a la insulina. Los modelos clásicos describen un «primer golpe» en el que el exceso de calorías y hormonas empuja la grasa hacia los hepatocitos, seguido de «golpes» adicionales como el estrés oxidativo y la inflamación crónica que lesionan y matan esas células. Los enfoques más recientes de «múltiples impactos» incorporan capas adicionales, incluida la comunicación entre las células hepáticas, las células inmunitarias y las formadoras de tejido cicatricial. Entre estas influencias, la epigenética ha emergido como un puente clave que vincula el entorno y el estilo de vida con el comportamiento de las células hepáticas.
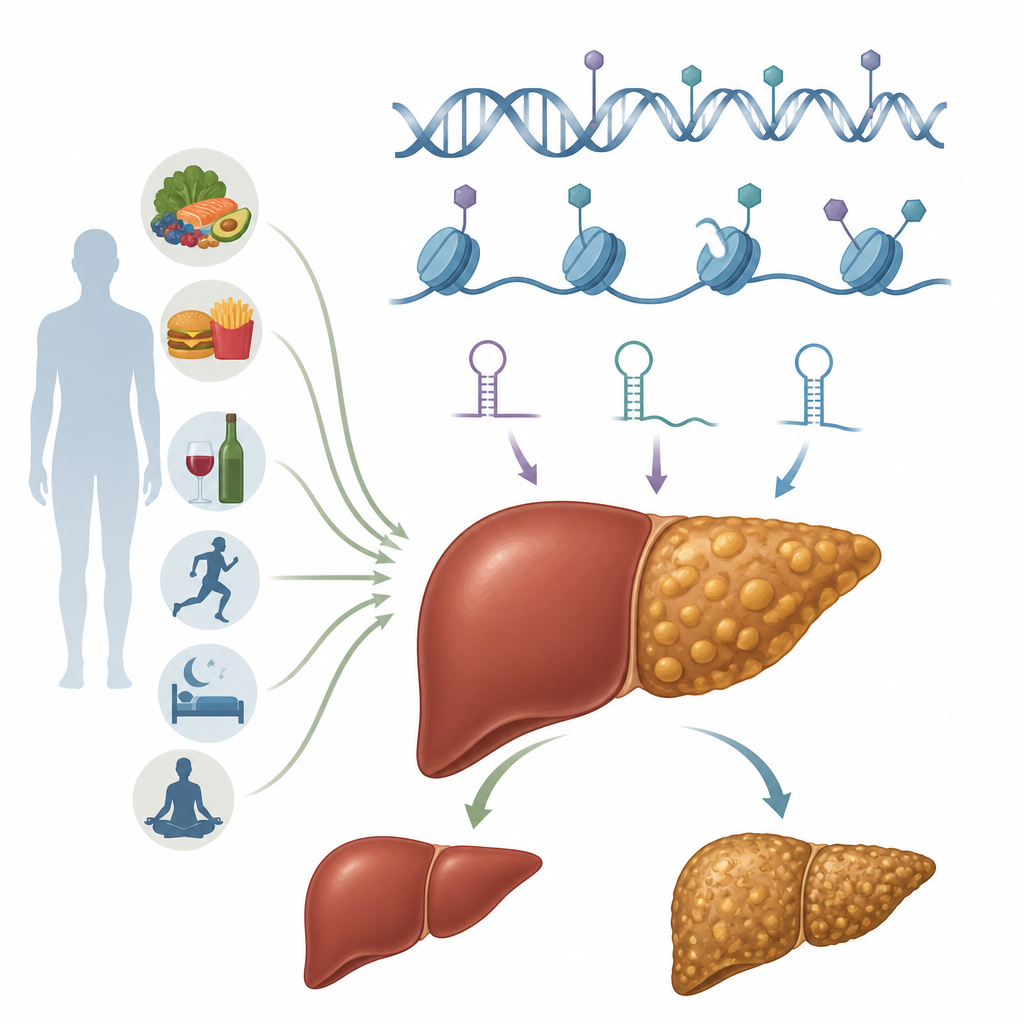
Interruptores epigenéticos en las células del hígado
La epigenética se refiere a marcas químicas y cambios estructurales que ajustan cómo se usan los genes sin alterar el código del ADN en sí. Estas marcas son reversibles y pueden ser moldeadas por la dieta, el estado metabólico y las toxinas. En los hepatocitos, las células trabajadoras del hígado, varios sistemas epigenéticos actúan de forma conjunta. La metilación del ADN puede silenciar o activar genes al colocar pequeñas etiquetas químicas en sitios específicos del ADN. La modificación de histonas altera los carretes proteicos alrededor de los que se enrolla el ADN, haciendo que regiones del genoma sean más accesibles o más cerradas. Los ARN no codificantes, incluidos microARNs y ARN largos, afinan qué mensajes se traducen en proteínas. Capas adicionales incluyen cambios químicos en el propio ARN y reordenamientos a gran escala de la cromatina, el complejo ADN–proteína que empaqueta el material genético. En conjunto, estos sistemas determinan cómo los hepatocitos manejan las grasas, los azúcares y las señales inflamatorias.
Cómo estos cambios empujan al hígado hacia la enfermedad
La revisión recoge evidencia de que patrones epigenéticos específicos en los hepatocitos favorecen el almacenamiento de grasa, dificultan la quema de lípidos y avivan la inflamación. Por ejemplo, la metilación alterada del ADN puede silenciar genes que normalmente apoyan la degradación saludable de las grasas o la función mitocondrial, mientras que potencia genes que fomentan la acumulación lipídica. Niveles altos de azúcar y colesterol en modelos experimentales conducen a cambios en la metilación del ADN a lo largo de miles de genes, desplazando redes enteras implicadas en el metabolismo de los lípidos. Las enzimas que modifican histonas pueden abrir tramos de ADN que impulsan la síntesis de grasas o vías inflamatorias, mientras que otras promueven programas protectores como la quema de grasas inducida por el ayuno y la limpieza celular. Los ARN no codificantes actúan como reguladores de respuesta rápida: ciertos microARN y ARN largos promueven la acumulación de grasa y la resistencia a la insulina, mientras que otros parecen proteger contra la esteatosis al frenar enzimas lipogénicas o atenuar la señalización inflamatoria.
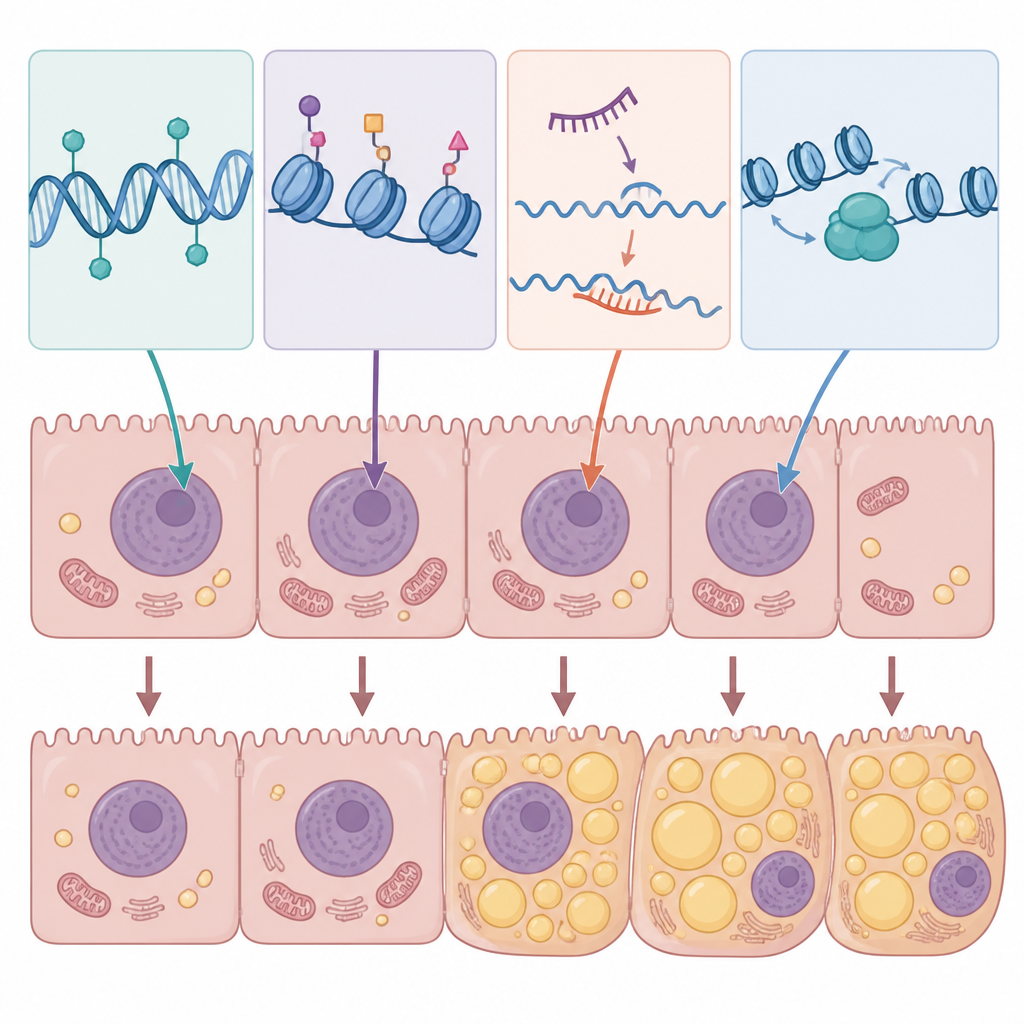
De los mecanismos a las pruebas y tratamientos
Como las marcas epigenéticas son a la vez estables y reversibles, resultan atractivas como herramientas diagnósticas y dianas farmacológicas futuras. Algunos patrones de metilación del ADN y firmas de microARN ya pueden detectarse en sangre y parecen correlacionar con la gravedad de la MASLD, lo que abre la posibilidad de pruebas sanguíneas simples que podrían evitar a algunos pacientes una biopsia hepática. En el ámbito terapéutico, varios fármacos y compuestos naturales probados en células y modelos animales, como el resveratrol, la betaína, la berberina y ciertos fármacos para la diabetes, parecen mejorar parcialmente el hígado graso al ajustar reguladores epigenéticos en los hepatocitos. Al mismo tiempo, los autores advierten que estos interruptores controlan muchos genes en varios órganos, por lo que fármacos de acción amplia podrían causar efectos adversos no deseados si no se dirigen con precisión.
Hacia dónde podría conducir esta investigación
El artículo concluye que la regulación epigenética en los hepatocitos es central para cómo comienza, progresa y, posiblemente, puede revertirse la MASLD. Al cartografiar los cambios epigenéticos específicos de cada célula con herramientas modernas de un solo célula y de “ómicas”, los científicos esperan identificar qué interruptores predicen mejor el riesgo de enfermedad, cuáles marcan una progresión peligrosa y cuáles pueden manipularse de forma segura. Para los no especialistas, el mensaje clave es que la salud hepática no está fijada solo por los genes. Factores cotidianos como la dieta y el estado metabólico dejan huellas químicas en el ADN y ARN de las células del hígado que pueden empujar al órgano hacia la salud o la enfermedad. Comprender y, eventualmente, dirigir esas huellas podría abrir la puerta a un diagnóstico más temprano y a tratamientos más precisos y menos invasivos para la enfermedad del hígado graso.
Cita: Zhu, G., Zhao, Q., Ran, J. et al. The role of hepatocyte epigenetics in the pathogenesis of metabolic dysfunction-associated steatotic liver disease. Commun Med 6, 276 (2026). https://doi.org/10.1038/s43856-026-01651-1
Palabras clave: enfermedad hepática grasa, epigenética, hepatocitos, metilación del ADN, ARN no codificante