Clear Sky Science · it
Il ruolo dell’epigenetica degli epatociti nella patogenesi della malattia epatica steatosica associata a disfunzione metabolica
Perché questa storia del fegato è importante per te
La malattia epatica steatosica associata a disfunzione metabolica, o MASLD, colpisce quasi una persona su tre nel mondo ed è strettamente legata all’obesità, al diabete di tipo 2 e alle malattie cardiovascolari. La maggior parte delle persone non avverte sintomi evidenti fino a quando non si è già verificato un danno serio. Questo articolo di revisione esplora un campo di ricerca in rapida evoluzione che pone una domanda semplice ma potente: come contribuiscono gli “interruttori” chimici sovrapposti ai nostri geni nelle cellule del fegato allo sviluppo della steatosi, e possono questi interruttori essere riprogrammati per prevenirla o curarla?
Dalla semplice accumulazione di grasso alla grave cicatrizzazione epatica
MASLD è un termine ampio che comprende condizioni che vanno dall’accumulo lieve di grasso nel fegato a infiammazione, cicatrizzazione, cirrosi e persino tumore epatico. La malattia si sviluppa attraverso una combinazione di rischio ereditario, dieta, microbi intestinali e problemi metabolici come la resistenza all’insulina. I modelli classici descrivono un “colpo” iniziale in cui calorie e ormoni in eccesso spingono il grasso dentro gli epatociti, seguito da ulteriori “colpi” come lo stress ossidativo e l’infiammazione cronica che danneggiano e uccidono quelle cellule. I modelli più recenti delle “multiplie sollecitazioni” aggiungono altri strati, inclusa la comunicazione tra cellule epatiche, cellule del sistema immunitario e cellule che formano tessuto cicatriziale. Tra queste influenze, l’epigenetica è emersa come un ponte chiave che collega ambiente e stile di vita al comportamento degli epatociti.
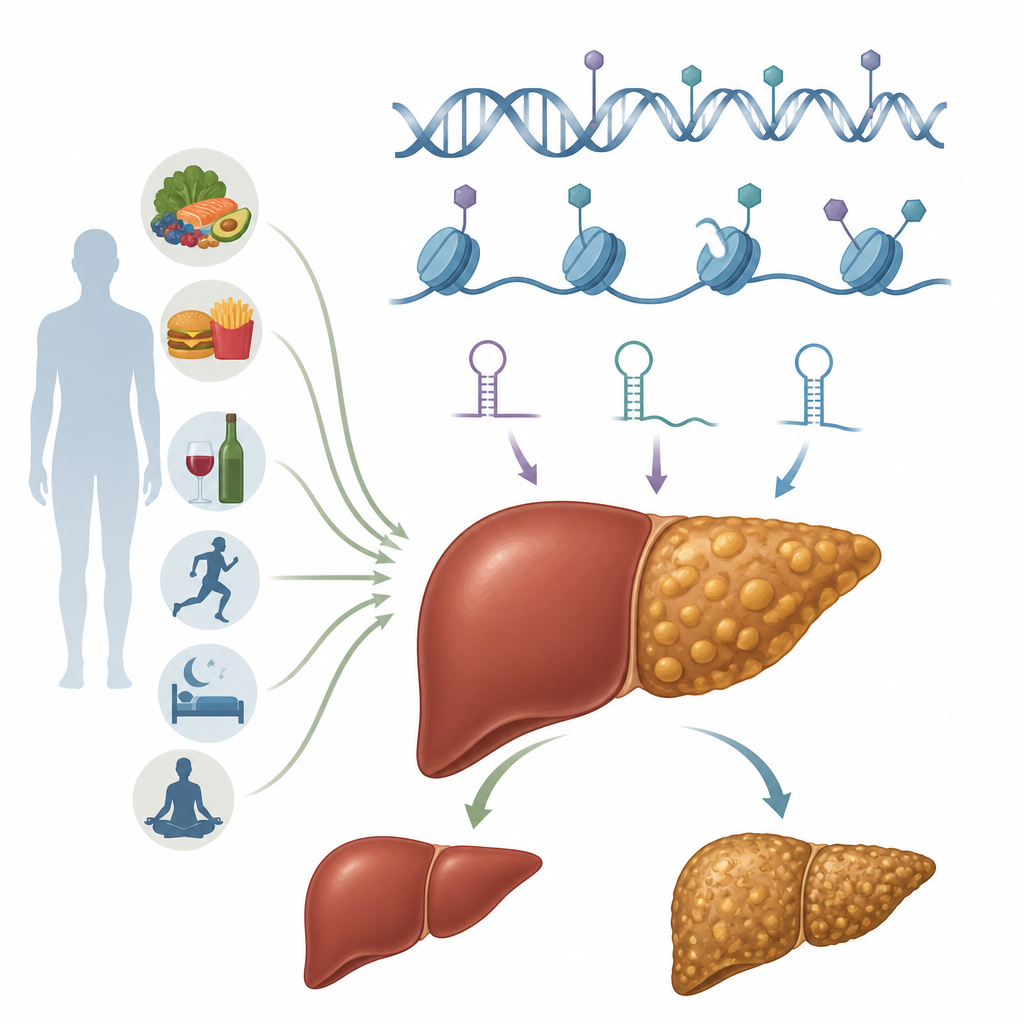
Interruttori epigenetici nelle cellule del fegato
Con epigenetica si intendono marchi chimici e cambiamenti strutturali che modulano l’uso dei geni senza alterare il codice del DNA. Questi marchi sono reversibili e possono essere plasmati dalla dieta, dallo stato metabolico e dalle tossine. Negli epatociti, le cellule lavoratrici del fegato, diversi sistemi epigenetici agiscono in sinergia. La metilazione del DNA può aumentare o diminuire l’espressione genica aggiungendo piccoli gruppi chimici su siti specifici del DNA. Le modificazioni degli istoni alterano i “bobbinaggi” proteici attorno ai quali il DNA è avvolto, rendendo regioni del genoma più aperte o più chiuse. Gli RNA non codificanti, inclusi microRNA e RNA lunghi, regolano con precisione quali messaggi vengono tradotti in proteine. Ulteriori livelli comprendono modifiche chimiche sull’RNA stesso e riorganizzazioni su larga scala della cromatina, il complesso DNA–proteine che impacchetta il materiale genetico. Nel loro insieme, questi sistemi definiscono come gli epatociti gestiscono grassi, zuccheri e segnali infiammatori.
Come questi cambiamenti spingono il fegato verso la malattia
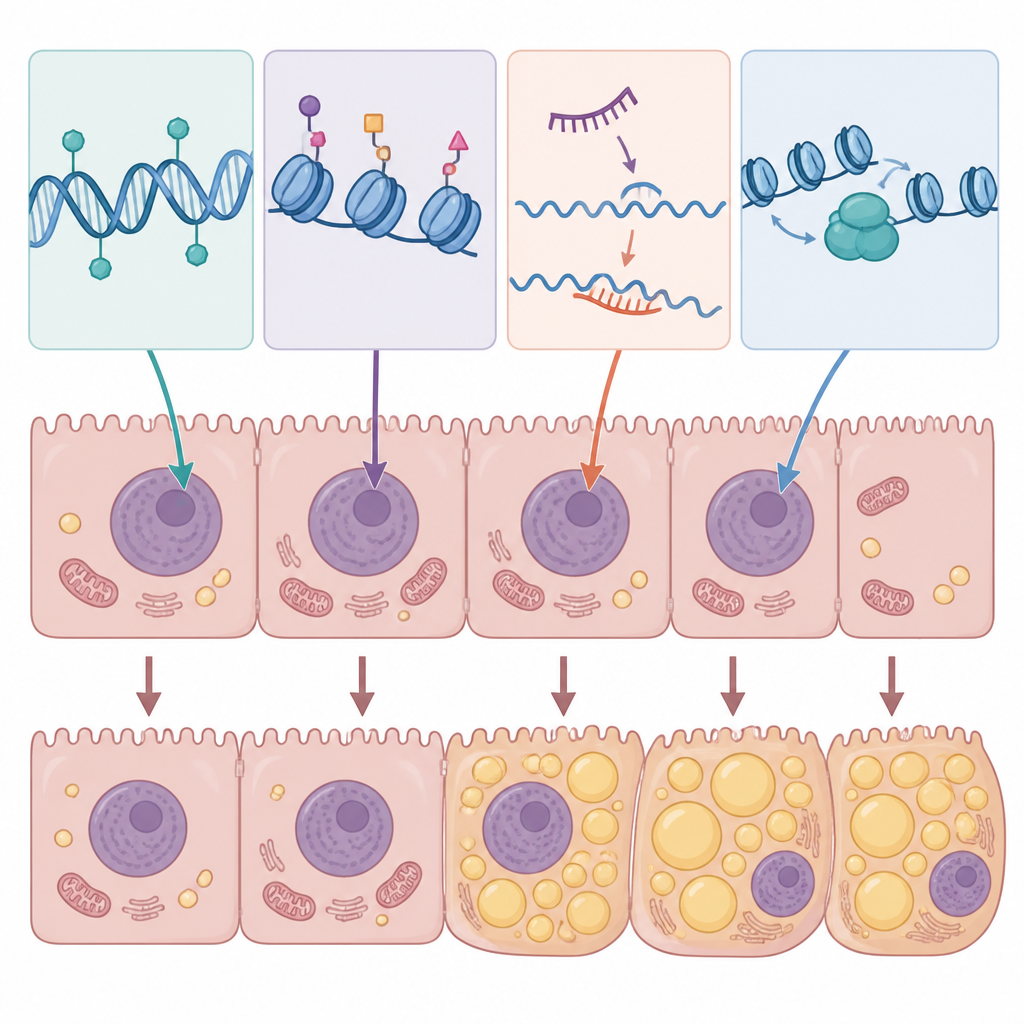
La rassegna raccoglie prove che specifici schemi epigenetici negli epatociti favoriscono l’accumulo di grasso, compromettono il suo consumo e alimentano l’infiammazione. Per esempio, alterazioni nella metilazione del DNA possono silenziare geni che normalmente supportano la corretta degradazione lipidica o la funzione mitocondriale, mentre aumentano l’espressione di geni che promuovono l’accumulo lipidico. Alti livelli di zuccheri e colesterolo nei modelli sperimentali portano a cambiamenti nella metilazione del DNA che coinvolgono migliaia di geni, spostando intere reti implicate nel metabolismo dei lipidi. Gli enzimi che modificano gli istoni possono aprire tratti di DNA che guidano la sintesi lipidica o percorsi infiammatori, mentre altri promuovono programmi protettivi come la mobilitazione dei grassi indotta dal digiuno e la pulizia cellulare. Gli RNA non codificanti agiscono come regolatori a risposta rapida: certi microRNA e RNA lunghi favoriscono l’accumulo di grasso e la resistenza all’insulina, mentre altri sembrano proteggere dalla steatosi limitando gli enzimi lipogenici o attenuando la segnalazione infiammatoria.
Dai meccanismi ai test e alle terapie
Poiché i marchi epigenetici sono allo stesso tempo stabili e reversibili, rappresentano candidati interessanti per futuri strumenti diagnostici e target farmacologici. Alcuni schemi di metilazione del DNA e profili di microRNA possono già essere rilevati nel sangue e sembrano corrispondere alla gravità della MASLD, aprendo la prospettiva di semplici esami del sangue che potrebbero risparmiare a molti pazienti la biopsia epatica. Sul fronte terapeutico, diversi farmaci e composti naturali testati su cellule e modelli animali, come resveratrolo, betaina, berberina e alcuni farmaci per il diabete, sembrano migliorare parzialmente la steatosi modulando regolatori epigenetici negli epatociti. Gli autori tuttavia avvertono che questi interruttori controllano molti geni in diversi organi, quindi farmaci ad azione ampia potrebbero causare effetti collaterali indesiderati se non mirati con precisione.
Dove potrebbe condurre questa ricerca
L’articolo conclude che la regolazione epigenetica negli epatociti è centrale per l’insorgenza, la progressione e la possibile reversibilità della MASLD. Mappando i cambiamenti epigenetici specifici per cellula con moderni strumenti single-cell e di “omics”, gli scienziati sperano di individuare quali interruttori predicono meglio il rischio di malattia, quali segnalano una progressione pericolosa e quali possono essere manipolati in sicurezza. Per i non specialisti, il messaggio chiave è che la salute del fegato non è fissata dai soli geni. Fattori quotidiani come dieta e stato metabolico lasciano impronte chimiche sul DNA e sull’RNA delle cellule epatiche che possono spingere l’organo verso la salute o la malattia. Comprendere e, in ultima analisi, guidare queste impronte potrebbe aprire la strada a diagnosi più precoci e a trattamenti più precisi e meno invasivi per la malattia del fegato grasso.
Citazione: Zhu, G., Zhao, Q., Ran, J. et al. The role of hepatocyte epigenetics in the pathogenesis of metabolic dysfunction-associated steatotic liver disease. Commun Med 6, 276 (2026). https://doi.org/10.1038/s43856-026-01651-1
Parole chiave: steatosi epatica, epigenetica, epatociti, metilazione del DNA, RNA non codificanti