Clear Sky Science · ja
肝細胞のエピジェネティクスが代謝性異常関連脂肪肝疾患の病因に果たす役割
なぜこの肝臓の話があなたに関係するのか
代謝性異常関連脂肪肝疾患(MASLD)は世界で約3人に1人が罹患するとされ、肥満、2型糖尿病、心血管疾患と強く関連しています。多くの人は明確な症状を感じることなく、深刻な障害が進行してしまうことが多いです。本レビューは、一見単純だが強力な問いを投げかける急速に発展する研究分野を探ります:肝細胞内の遺伝子に重ねられた化学的「スイッチ」は脂肪肝をどのように促進し、それらのスイッチをリセットして予防や治療に結びつけられるだろうか?
単純な脂肪蓄積から深刻な肝線維化へ
MASLDは、肝臓の軽度の脂肪蓄積から炎症、線維化、肝硬変、さらには肝がんに至る範囲を包含する広い用語です。疾患は遺伝的リスク、食事、腸内微生物、インスリン抵抗性などの代謝異常が混ざり合って進行します。古典的なモデルでは、余剰のカロリーやホルモンが肝細胞に脂肪を押し込む初期の「ヒット」があり、その後、酸化ストレスや慢性炎症といった追加の「ヒット」が細胞を傷つけたり死に至らせたりすると説明されます。近年の「多重打撃」的な考え方では、肝細胞が免疫細胞や線維化を引き起こす細胞とどう連携するかなど、さらなる層が加わります。こうした影響の中で、エピジェネティクスは環境や生活習慣と肝細胞の振る舞いをつなぐ重要な架け橋として浮上しています。
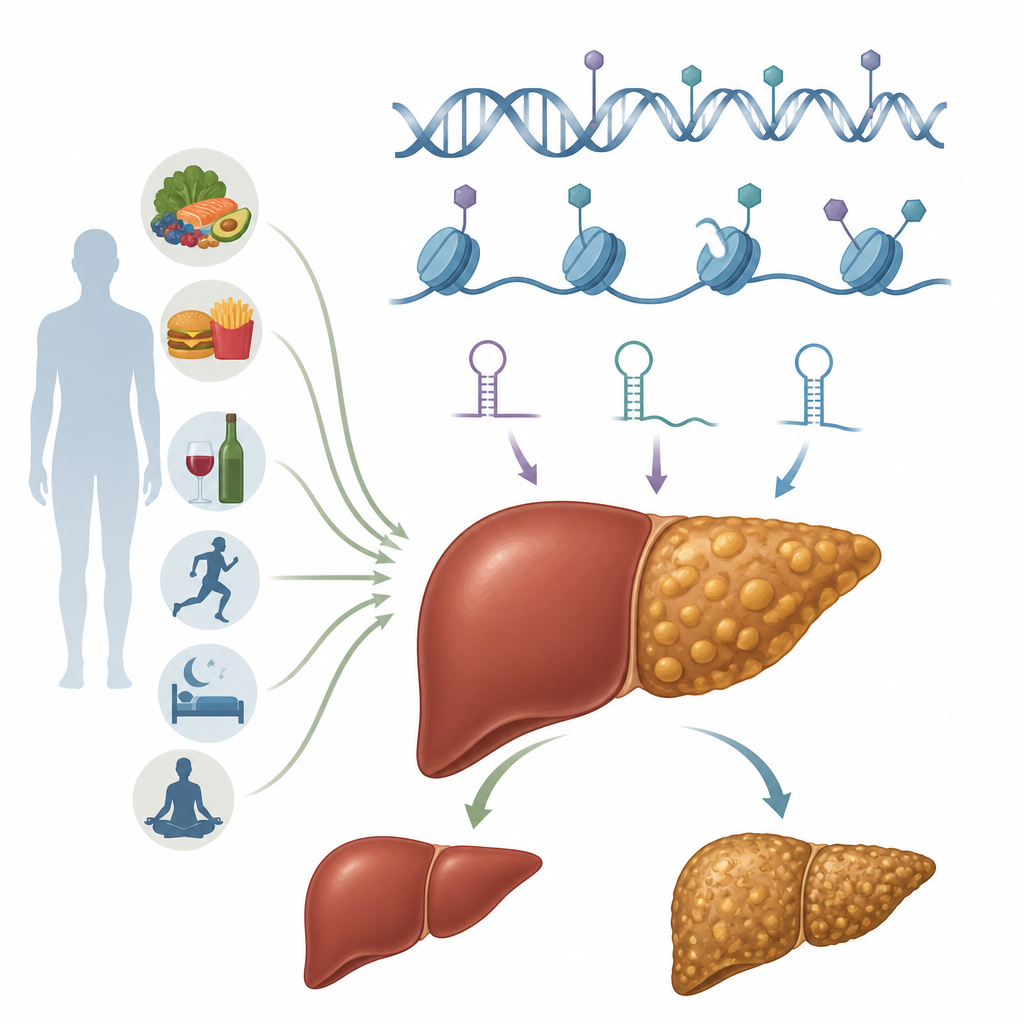
肝細胞におけるエピジェネティックなスイッチ
エピジェネティクスとは、DNA配列自体を変えずに遺伝子の利用のされ方を調節する化学的標識や構造変化を指します。これらの標識は可逆的であり、食事、代謝状態、毒物などによって形成されます。肝臓の働き手である肝細胞では、複数のエピジェネティックなシステムが協調して働きます。DNAメチル化は特定のDNA部位に小さな化学タグを置くことで遺伝子の発現を上げたり下げたりできます。ヒストン修飾はDNAが巻き付くタンパク質スプールを変化させ、ゲノム領域をより開放的にしたり閉鎖的にしたりします。マイクロRNAや長鎖RNAを含む非コードRNAは、どのメッセージがタンパク質に翻訳されるかを微調整します。さらに、RNA自身への化学修飾やクロマチン(遺伝物質を包むDNA–タンパク質複合体)の大規模な再編成などの層もあります。これらのシステムが一体となって、肝細胞が脂肪や糖、炎症シグナルをどう扱うかを形作ります。
これらの変化が肝臓を病へと傾ける仕組み
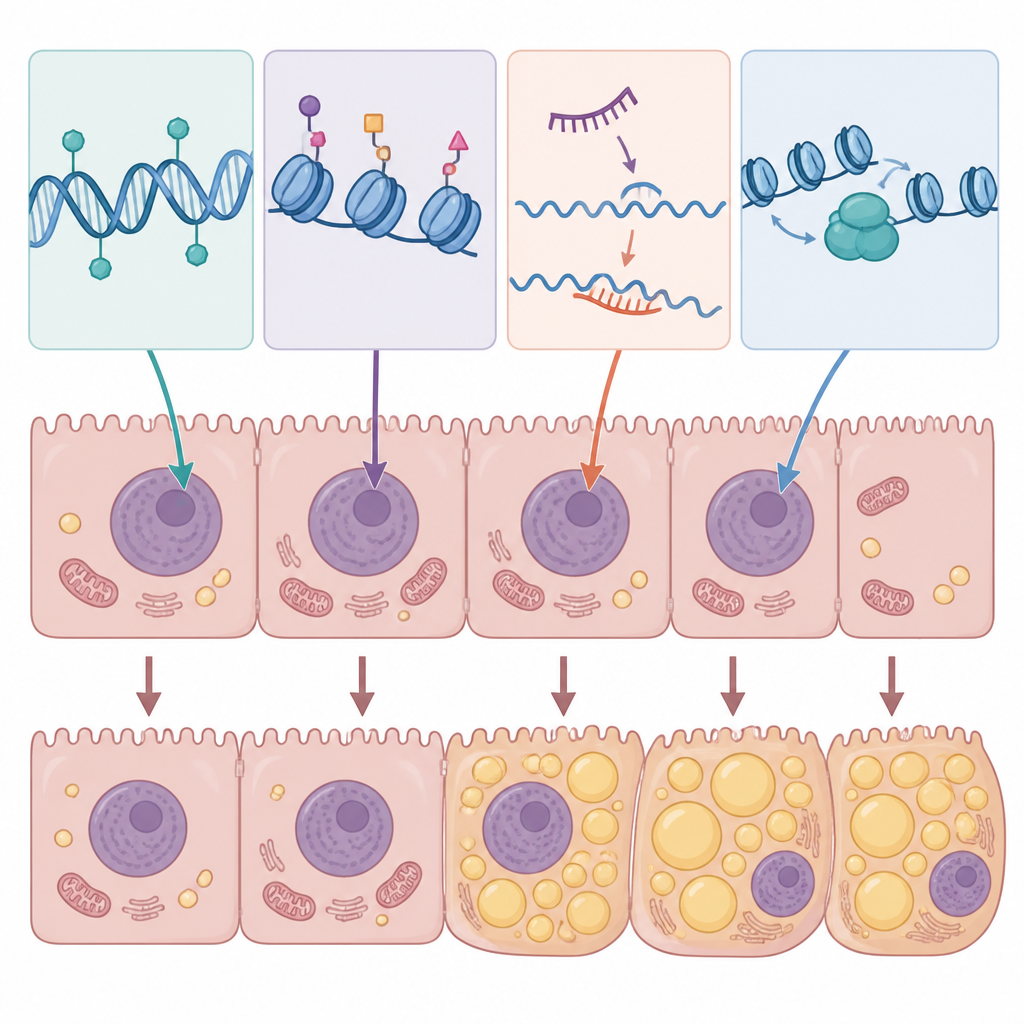
レビューは、肝細胞における特定のエピジェネティックパターンが脂肪の貯蔵を促し、脂肪燃焼を阻害し、炎症を助長することを示す証拠を集めています。たとえば、変化したDNAメチル化は通常は健全な脂肪分解やミトコンドリア機能を支える遺伝子をサイレンシングし、一方で脂肪蓄積を促す遺伝子を増強することがあります。実験モデルでは高糖や高コレステロール状態が数千に及ぶ遺伝子のDNAメチル化を変化させ、脂質代謝に関わるネットワーク全体をシフトさせます。ヒストン修飾酵素は脂肪合成や炎症経路を駆動するDNA領域を開くことがあり、逆に断食誘導の脂肪燃焼や細胞のクリアランスといった保護的プログラムを促進するものもあります。非コードRNAは迅速な応答を行う調整子として働き、特定のマイクロRNAや長鎖RNAは脂肪蓄積やインスリン抵抗性を促進する一方で、脂質合成酵素を抑えたり炎症シグナルを抑制したりして脂肪肝から保護するものも存在します。
メカニズムから検査・治療へ
エピジェネティックな標識は安定性と可逆性を兼ね備えているため、将来の診断ツールや薬剤標的として有望です。いくつかのDNAメチル化パターンやマイクロRNAの署名は血液中で検出可能で、MASLDの重症度と相関するように見え、肝生検を回避できる簡便な血液検査の可能性を示唆しています。治療面では、レスベラトロール、ベタイン、ベンベリン、ある種の糖尿病薬など、細胞や動物モデルで試された幾つかの薬剤や天然化合物が、肝細胞のエピジェネティック調節因子を調整することで脂肪肝を部分的に改善するように見えます。一方で著者らは、これらのスイッチは複数の臓器にまたがって多くの遺伝子を制御するため、広範に作用する薬剤は慎重に標的化しないと望ましくない副作用を引き起こす可能性があると注意を促しています。
この研究が向かう先
記事は、肝細胞におけるエピジェネティック制御がMASLDの発症、進行、そして可逆性に中心的な役割を果たすと結論付けています。単一細胞解析やオミクス技術で細胞特異的なエピジェネティック変化をマッピングすることで、どのスイッチが疾患リスクを最も予測するか、どれが危険な進行を示すか、そして安全に操作可能かを特定することが期待されています。非専門家にとっての主要なメッセージは、肝の健康は遺伝子だけで決まるわけではない、ということです。食事や代謝状態といった日常的な要因が肝細胞のDNAやRNAに化学的な足跡を残し、それが臓器を健康か病に傾ける可能性があります。これらの足跡を理解し、最終的に制御することは、脂肪肝の早期診断や、より精密で侵襲性の低い治療への道を開くかもしれません。
引用: Zhu, G., Zhao, Q., Ran, J. et al. The role of hepatocyte epigenetics in the pathogenesis of metabolic dysfunction-associated steatotic liver disease. Commun Med 6, 276 (2026). https://doi.org/10.1038/s43856-026-01651-1
キーワード: 脂肪肝疾患, エピジェネティクス, 肝細胞, DNAメチル化, 非コードRNA