Clear Sky Science · ru
Роль эпигенетики гепатоцитов в патогенезе стеатотической болезни печени, связанной с метаболической дисфункцией
Почему эта история о печени важна для вас
Стеатотическая болезнь печени, связанная с метаболической дисфункцией (MASLD), поражает почти каждого третьего человека в мире и тесно связана с ожирением, сахарным диабетом 2-го типа и сердечно-сосудистыми заболеваниями. У большинства людей явные симптомы не проявляются до тех пор, пока не наступят серьёзные повреждения. В этом обзорном материале рассматривается быстро развивающаяся область исследований, которая задаёт простой, но важный вопрос: как химические «переключатели», нанесённые на наши гены внутри клеток печени, способствуют развитию жировой болезни печени и можно ли эти переключатели сбросить, чтобы предотвратить или лечить её?
От простого накопления жира до серьёзного рубцевания печени
MASLD — широкий термин, охватывающий состояния от лёгкого накопления жира в печени до воспаления, образования рубцов, цирроза и даже рака печени. Заболевание развивается под влиянием наследственных факторов, питания, микробиоты кишечника и метаболических нарушений, таких как инсулинорезистентность. Классические модели описывают начальный «удар», когда избыточные калории и гормоны задвигают жир в клетки печени, за которым следуют дополнительные «удары» — окислительный стресс и хроническое воспаление, повреждающие и убивающие эти клетки. Современные концепции с «множественными ударами» добавляют новые уровни, включая способы общения между печёночными клетками, иммунными клетками и клетками, формирующими рубцовую ткань. Среди этих влияний эпигенетика выступает ключевым мостом, связывающим окружающую среду и образ жизни с поведением клеток печени.
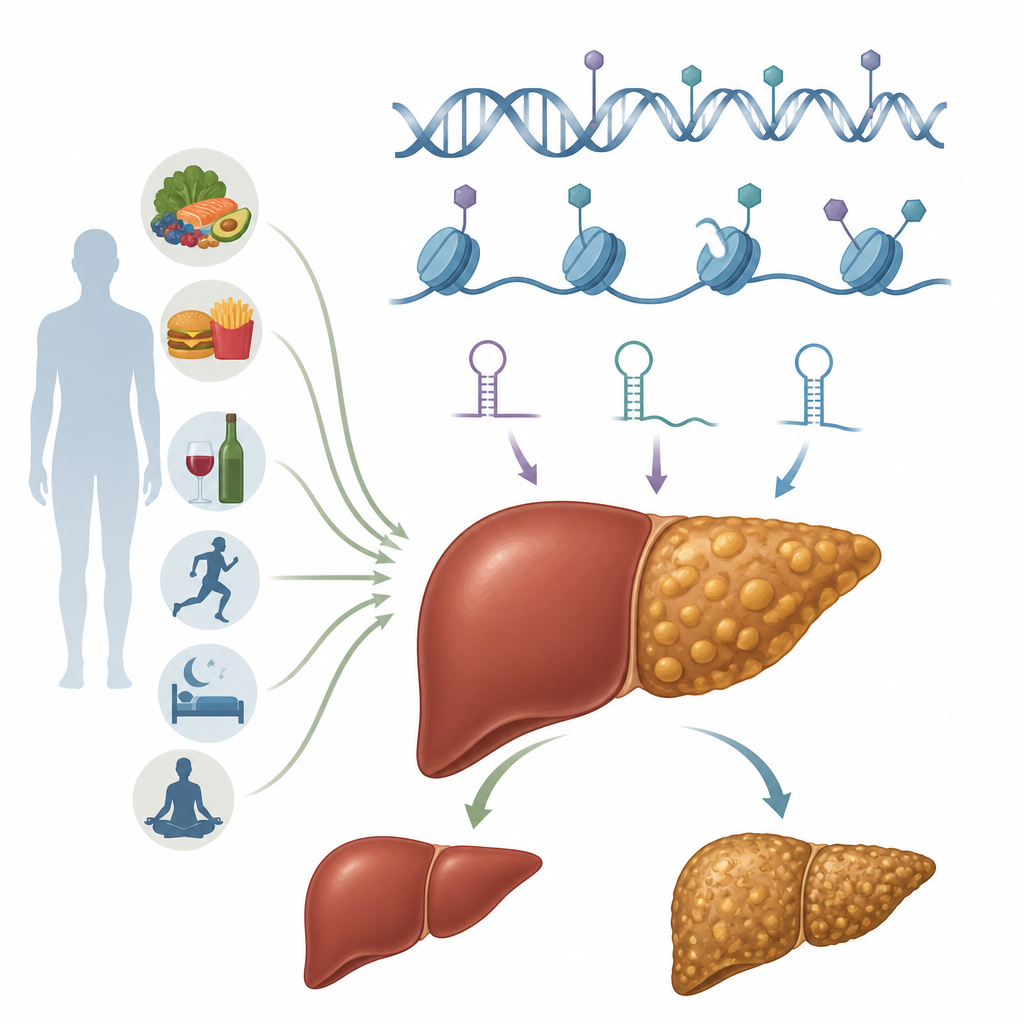
Эпигенетические переключатели в клетках печени
Эпигенетика означает химические метки и структурные изменения, которые регулируют использование генов без изменения самой последовательности ДНК. Эти метки обратимы и формируются под влиянием питания, метаболического статуса и токсинов. В гепатоцитах, трудолюбивых клетках печени, несколько эпигенетических систем действуют совместно. Метилирование ДНК может усиливать или подавлять гены путём нанесения небольших химических меток в конкретных участках ДНК. Модификация гистонов меняет свойства «шпулек», вокруг которых намотана ДНК, делая участки генома более открытыми или закрытыми. Некодирующие РНК, включая микроРНК и длинные РНК, тонко настраивают, какие сообщения будут трансляцированы в белки. Дополнительные уровни включают химические изменения на самой РНК и крупномасштабную перестройку хроматина — ДНК–белкового комплекса, упаковующего генетический материал. В совокупности эти системы формируют то, как гепатоциты справляются с липидами, сахаром и сигнальными молекулами воспаления.
Как эти изменения сдвигают печень в сторону болезни
Обзор сводит воедино данные, что определённые эпигенетические паттерны в гепатоцитах способствуют отложению жира, уменьшают его расщепление и усиливают воспаление. Например, изменённое метилирование ДНК может заглушать гены, обычно поддерживающие здоровый распад жиров или функцию митохондрий, одновременно активируя гены, поощряющие накопление липидов. Высокий уровень сахара и холестерина в экспериментальных моделях вызывает изменения метилирования ДНК в тысячах генов, сдвигая целые сети, вовлечённые в липидный метаболизм. Ферменты, модифицирующие гистоны, могут «открывать» участки ДНК, запускающие синтез жиров или воспалительные пути, тогда как другие стимулируют защитные программы, такие как окисление жира при голодании и клеточный «ремонт». Некодирующие РНК действуют как быстрые регуляторы: отдельные микроРНК и длинные РНК способствуют накоплению жира и инсулинорезистентности, тогда как другие защищают от стеатоза, сдерживая липогенные ферменты или ослабляя воспалительные сигналы.
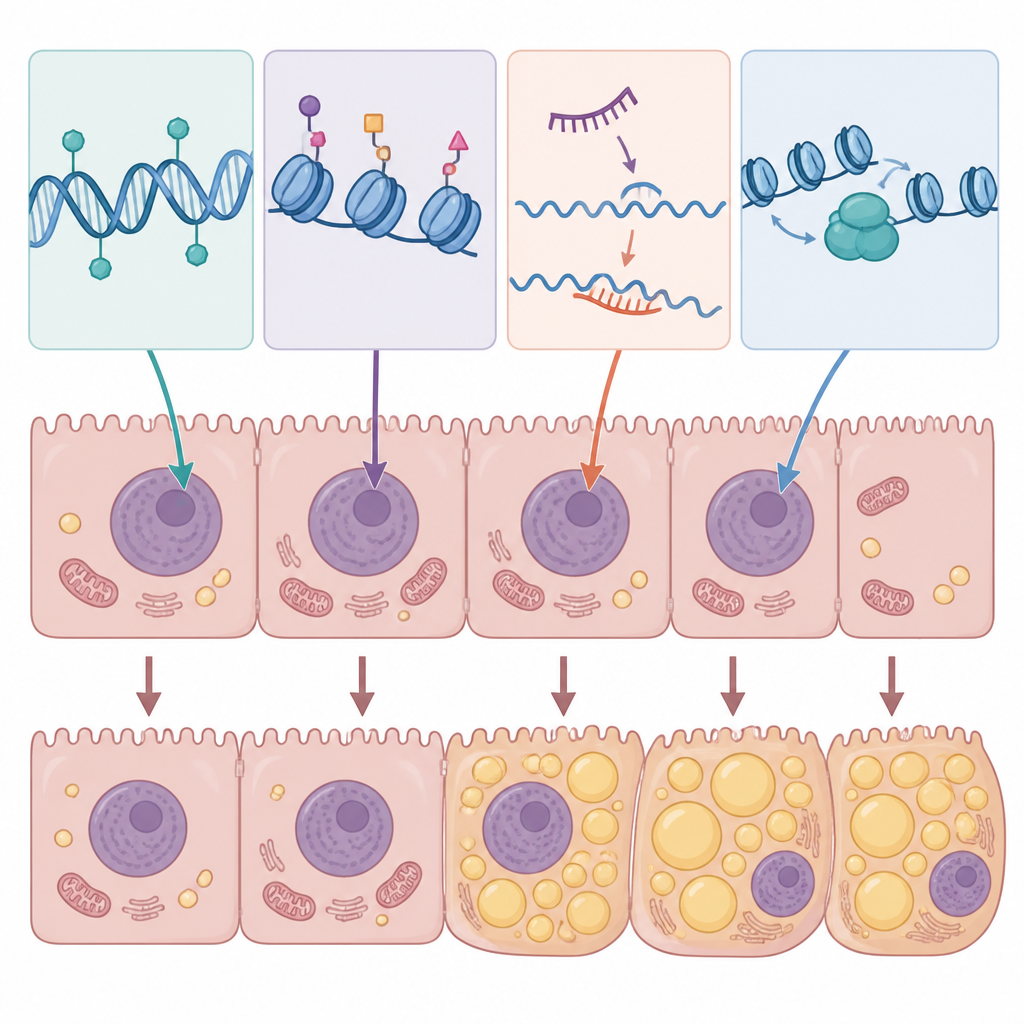
От механизмов к тестам и лечению
Поскольку эпигенетические метки одновременно стабильны и обратимы, они представляют интерес как потенциальные диагностические маркеры и лекарственные мишени. Некоторые паттерны метилирования ДНК и подписи микроРНК уже можно обнаружить в крови, и они коррелируют с тяжестью MASLD, что открывает перспективу простых анализов крови, способных избавить часть пациентов от необходимости биопсии печени. В терапевтическом плане несколько лекарств и природных соединений, протестированных в клеточных и животных моделях — например, ресвератрол, бетаин, берберин и некоторые препараты для лечения диабета — частично улучшают состояние жировой печени, влияя на эпигенетические регуляторы в гепатоцитах. Авторы при этом предупреждают, что такие переключатели контролируют множество генов в разных органах, и поэтому препараты широкого действия могут вызывать нежелательные эффекты, если их не направить селективно.
К чему может привести это исследование
В статье делается вывод, что эпигенетическая регуляция в гепатоцитах играет центральную роль в том, как MASLD начинается, прогрессирует и, возможно, может быть обращена. С помощью современных одноклеточных и «омических» методов учёные надеются картировать клеточно‑специфические эпигенетические изменения, чтобы выявить, какие переключатели лучше всего предсказывают риск болезни, какие отмечают опасное прогрессирование и какие из них можно безопасно модифицировать. Для неспециалистов ключевая мысль такова: здоровье печени не предопределено только генами. Повседневные факторы, такие как питание и метаболическое состояние, оставляют химические отпечатки на ДНК и РНК печёночных клеток, которые могут толкать орган к здоровью или болезни. Понимание и в конечном счёте управление этими отпечатками может открыть путь к более ранней диагностике и более точным, менее инвазивным методам лечения жировой болезни печени.
Цитирование: Zhu, G., Zhao, Q., Ran, J. et al. The role of hepatocyte epigenetics in the pathogenesis of metabolic dysfunction-associated steatotic liver disease. Commun Med 6, 276 (2026). https://doi.org/10.1038/s43856-026-01651-1
Ключевые слова: жировая болезнь печени, эпигенетика, гепатоциты, метилирование ДНК, некодирующая РНК