Clear Sky Science · pt
O papel da epigenética dos hepatócitos na patogênese da doença hepática esteatótica associada à disfunção metabólica
Por que esta história do fígado importa para você
Doença hepática esteatótica associada à disfunção metabólica, ou MASLD, afeta quase uma em cada três pessoas no mundo e está fortemente relacionada à obesidade, diabetes tipo 2 e doenças cardiovasculares. A maioria das pessoas não percebe sintomas claros até que danos sérios já tenham ocorrido. Este artigo de revisão explora uma área de pesquisa em rápido desenvolvimento que faz uma pergunta simples, porém poderosa: como os “interruptores” químicos colocados sobre nossos genes dentro das células do fígado ajudam a impulsionar a doença hepática gordurosa, e esses interruptores podem ser redefinidos para preveni-la ou tratá-la?
Do simples acúmulo de gordura à fibrose hepática grave
MASLD é um termo amplo que abrange condições que vão desde o acúmulo leve de gordura no fígado até inflamação, formação de cicatriz, cirrose e até câncer de fígado. A doença se desenvolve por uma mistura de risco herdado, dieta, micróbios intestinais e problemas metabólicos como resistência à insulina. Modelos clássicos descrevem um “primeiro golpe” inicial em que calorias e hormônios em excesso empurram gordura para os hepatócitos, seguido por “golpes” adicionais como estresse oxidativo e inflamação crônica que lesionam e matam essas células. Pensamentos mais recentes de “múltiplos ataques” adicionam camadas, incluindo como as células do fígado se comunicam com células imunes e formadoras de fibrose. Entre essas influências, a epigenética emergiu como uma ponte chave que liga o ambiente e o estilo de vida ao comportamento das células hepáticas.
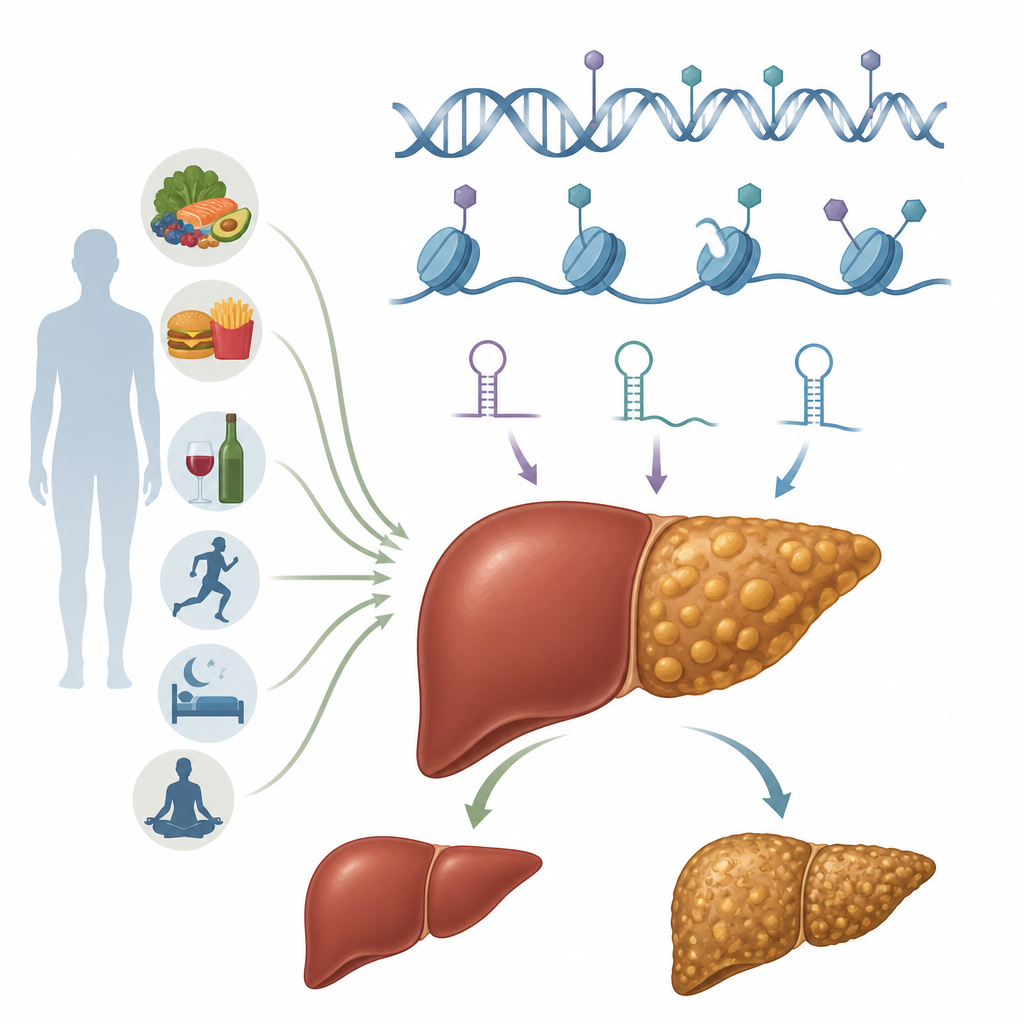
Interruptores epigenéticos nas células do fígado
Epigenética refere-se a marcas químicas e mudanças estruturais que ajustam como os genes são usados sem alterar o código de DNA em si. Essas marcas são reversíveis e podem ser moldadas pela dieta, pelo estado metabólico e por toxinas. Nos hepatócitos, as células de trabalho do fígado, vários sistemas epigenéticos atuam em conjunto. A metilação do DNA pode ligar ou desligar genes ao colocar pequenas tags químicas em sítios específicos do DNA. Modificações de histonas alteram os carretéis proteicos em torno dos quais o DNA está enrolado, tornando regiões do genoma mais abertas ou mais fechadas. RNAs não codificantes, incluindo microRNAs e RNAs longos, afinam quais mensagens são traduzidas em proteínas. Camadas adicionais incluem modificações químicas no próprio RNA e rearranjos em grande escala da cromatina, o complexo DNA–proteína que empacota o material genético. Juntos, esses sistemas moldam como os hepatócitos lidam com gordura, açúcar e sinais inflamatórios.
Como essas mudanças empurram o fígado para a doença
A revisão reúne evidências de que padrões epigenéticos específicos nos hepatócitos favorecem o armazenamento de gordura, prejudicam a queima de gordura e atiçam a inflamação. Por exemplo, metilação do DNA alterada pode silenciar genes que normalmente apoiam a quebra saudável de gordura ou a função mitocondrial, enquanto aumenta genes que incentivam o acúmulo lipídico. Altos níveis de açúcar e colesterol em modelos experimentais levam a alterações na metilação do DNA em milhares de genes, deslocando redes inteiras envolvidas no metabolismo lipídico. Enzimas que modificam histonas podem abrir trechos de DNA que impulsionam a síntese de gordura ou vias inflamatórias, enquanto outras promovem programas protetores, como a queima de gordura induzida pelo jejum e a limpeza celular. RNAs não codificantes atuam como reguladores de resposta rápida: certos microRNAs e RNAs longos promovem o acúmulo de gordura e resistência à insulina, enquanto outros parecem proteger contra a esteatose ao conter enzimas lipogênicas ou atenuar sinais inflamatórios.
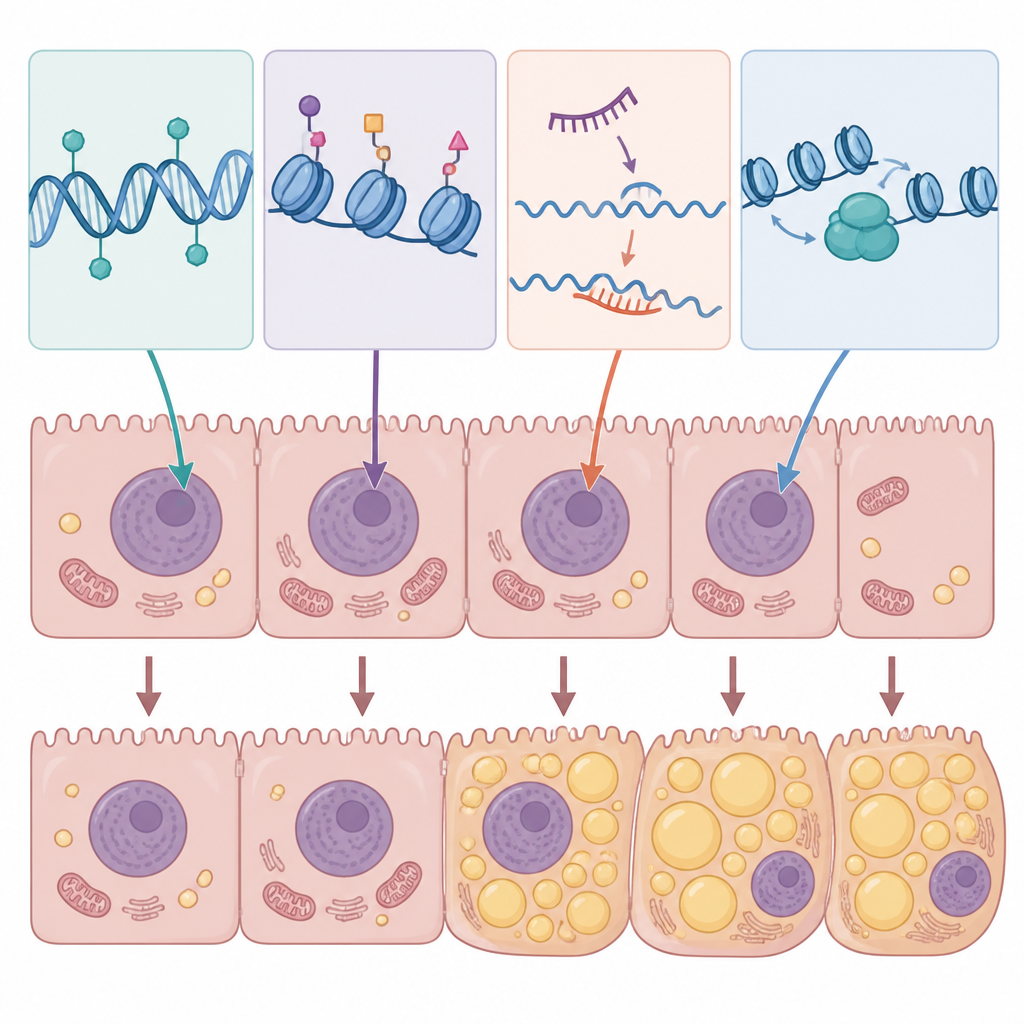
De mecanismos a testes e tratamentos
Porque as marcas epigenéticas são ao mesmo tempo estáveis e reversíveis, elas são atraentes como futuras ferramentas diagnósticas e alvos de fármacos. Alguns padrões de metilação do DNA e assinaturas de microRNA já podem ser detectados no sangue e parecem acompanhar a gravidade da MASLD, abrindo a possibilidade de testes sanguíneos simples que poupariam alguns pacientes da biópsia hepática. Na vertente terapêutica, vários medicamentos e compostos naturais testados em células e modelos animais, como resveratrol, betaína, berberina e certos fármacos para diabetes, aparentam melhorar parcialmente o fígado gorduroso ao ajustar reguladores epigenéticos nos hepatócitos. Ao mesmo tempo, os autores advertem que esses interruptores controlam muitos genes em vários órgãos, de modo que fármacos de ação ampla podem causar efeitos colaterais indesejados se não forem cuidadosamente direcionados.
Para onde essa pesquisa pode levar
O artigo conclui que a regulação epigenética nos hepatócitos é central para como a MASLD se inicia, progride e, possivelmente, pode ser revertida. Ao mapear alterações epigenéticas específicas de célula com ferramentas modernas de célula única e “ômicas”, os cientistas esperam identificar quais interruptores melhor predizem o risco de doença, quais marcam progressão perigosa e quais podem ser manipulados com segurança. Para não especialistas, a mensagem chave é que a saúde do fígado não é determinada apenas pelos genes. Fatores do dia a dia, como dieta e estado metabólico, deixam impressões químicas no DNA e no RNA das células hepáticas que podem empurrar o órgão em direção à saúde ou à doença. Entender e, eventualmente, orientar essas impressões pode abrir a porta para um diagnóstico mais precoce e tratamentos mais precisos e menos invasivos para a doença hepática gordurosa.
Citação: Zhu, G., Zhao, Q., Ran, J. et al. The role of hepatocyte epigenetics in the pathogenesis of metabolic dysfunction-associated steatotic liver disease. Commun Med 6, 276 (2026). https://doi.org/10.1038/s43856-026-01651-1
Palavras-chave: doença hepática gordurosa, epigenética, hepatócitos, metilação do DNA, RNA não codificante