Clear Sky Science · ar
دور العلامات فوق الجينية في الخلايا الكبدية في مرض الكبد الدهني المرتبط بخلل التمثّل الغذائي
لماذا تهمك هذه القصة عن الكبد
يصيب مرض الكبد الدهني المرتبط بخلل التمثّل الغذائي، أو MASLD، ما يقرب من شخص واحد من بين كل ثلاثة أشخاص على مستوى العالم ويرتبط ارتباطًا وثيقًا بالسمنة، ومرض السكري من النوع الثاني، وأمراض القلب. معظم الأشخاص لا يشعرون بأعراض واضحة حتى حدوث ضرر خطير بالفعل. تستعرض هذه المقالة منطقة بحث سريعة التطور تسأل سؤالًا بسيطًا لكنه قويًا: كيف تُسهِم "مفاتيح" كيميائية مورّثة على جيناتنا داخل خلايا الكبد في دفع مرض الكبد الدهني، وهل يمكن إعادة ضبط هذه المفاتيح للوقاية منه أو علاجه؟
من تراكم بسيط للدهون إلى تندب كبدي خطير
MASLD هو مصطلح واسع يشمل حالات تتراوح من تراكم بسيط للدهون في الكبد إلى التهاب، وتندب، وتليف، وحتى سرطان الكبد. يتطور المرض عبر مزيج من عوامل وراثية، والنظام الغذائي، والميكروبيوم المعوي، ومشكلات تمثيل غذائي مثل مقاومة الإنسولين. تصف النماذج الكلاسيكية "الضربة" الأولية التي تدفع فيها السعرات الزائدة والهرمونات الدهون إلى الخلايا الكبدية، تليها "ضربات" إضافية مثل الإجهاد التأكسدي والالتهاب المزمن التي تضر بهذه الخلايا وتقتلها. يضيف تفكير "الضربات المتعددة" الحديث طبقات إضافية، بما في ذلك كيفية تواصل الخلايا الكبدية مع خلايا الجهاز المناعي وخلايا تكوين النسيج الندبي. من بين هذه التأثيرات، برزت العلامات فوق الجينية كجسر رئيسي يربط البيئة ونمط الحياة بسلوك الخلايا الكبدية.
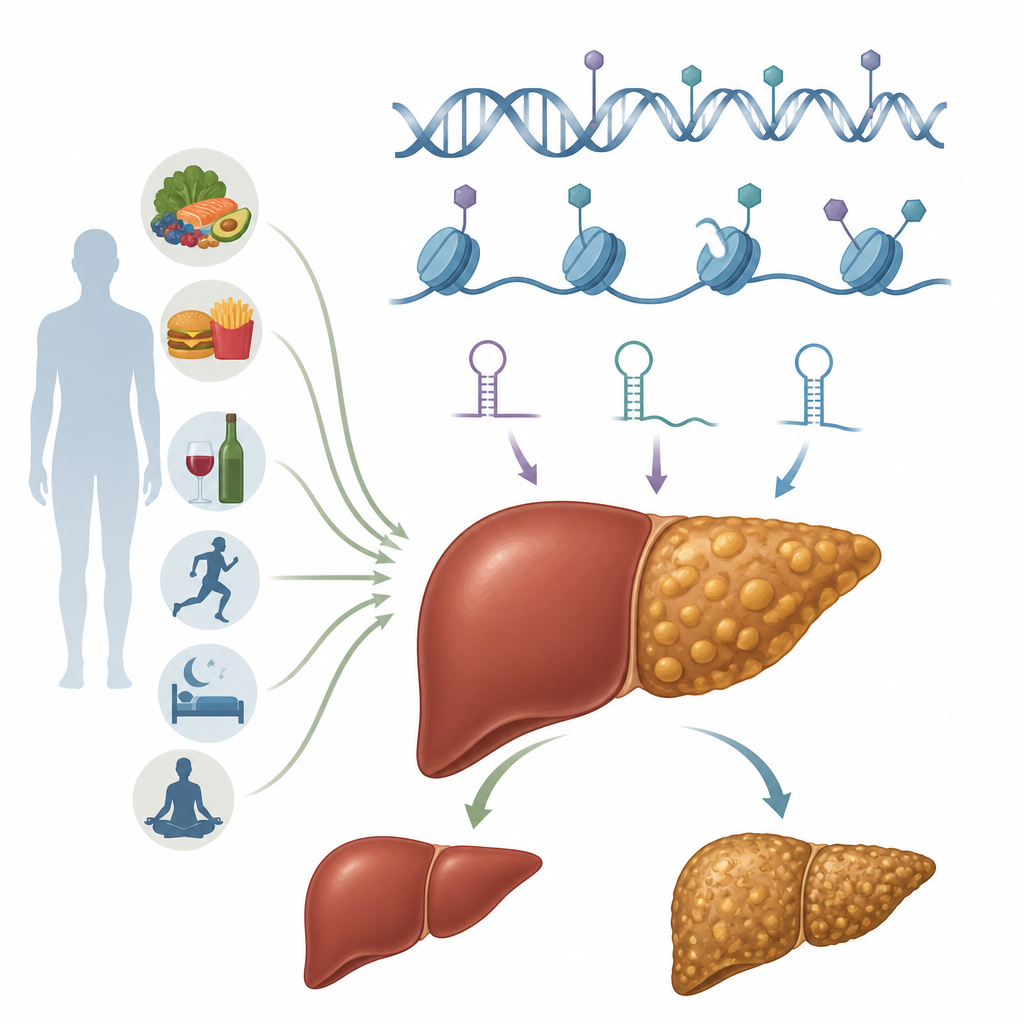
المفاتيح فوق الجينية في الخلايا الكبدية
تشير العلامات فوق الجينية إلى علامات كيميائية وتغيرات هيكلية تعدّل كيفية استخدام الجينات دون تغيير رمز الحمض النووي نفسه. هذه العلامات قابلة للعكس ويمكن تشكيلها بواسطة النظام الغذائي، والحالة التمثيلية، والسموم. في الخلايا الكبدية، وهي الخلايا الفعالة في الكبد، تعمل عدة أنظمة فوق جينية معًا. يمكن لمثيلة الحمض النووي أن ترفع أو تخفض نشاط جينات عن طريق وضع علامات كيميائية صغيرة على مواقع محددة من الحمض النووي. تغير تعديلات الهيستون البروتينات الحلزونية التي يلتف حولها الحمض النووي، مما يجعل مناطق من الجينوم أكثر انفتاحًا أو إغلاقًا. تعدّ الحمضيات النووية غير المشفرة، بما في ذلك الميكرو RNA والـ RNA طويلة السلسلة، الضوابط الدقيقة التي تضبط أي الرسائل تُترجم إلى بروتينات. تشمل الطبقات الإضافية تغييرات كيميائية على الحمض النووي الريبي نفسه وإعادة ترتيب واسعة النطاق للكروماتين، وهو مركب الحمض النووي–البروتين الذي يعبّئ المادة الوراثية. معًا تشكل هذه الأنظمة كيفية تعامل الخلايا الكبدية مع الدهون، والسكر، والإشارات الالتهابية.
كيف تدفع هذه التغيرات الكبد نحو المرض
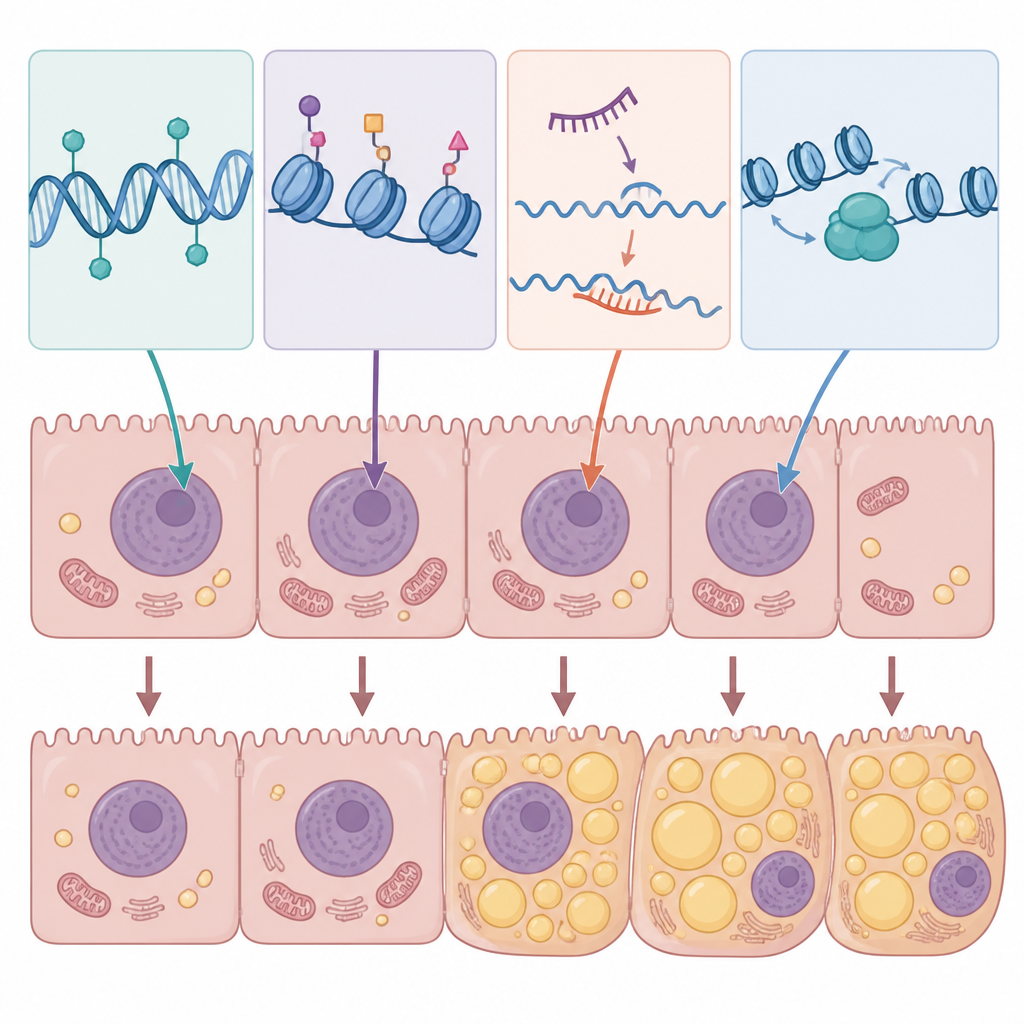
تجمع المراجعة الدلائل على أن أنماطًا فوق جينية محددة في الخلايا الكبدية تُفضّل تخزين الدهون، وتعيق حرق الدهون، وتوقد جذوة الالتهاب. على سبيل المثال، يمكن أن تُسكت مثيلة الحمض النووي جينات كانت تدعم تحلل الدهون الصحي أو وظيفة الميتوكوندريا، بينما تعزز جينات تشجع تراكم الدهون. تؤدي مستويات السكر والكوليسترول المرتفعة في نماذج تجريبية إلى تغييرات في مثيلة الحمض النووي عبر آلاف الجينات، محوّلة شبكات كاملة تشارك في تمثيل الدهنيات. قد تفتح إنزيمات تعديل الهستون مقاطع من الحمض النووي التي تحث على تخليق الدهون أو المسارات الالتهابية، بينما يروّج بعضها الآخر لبرامج واقية مثل حرق الدهون الناجم عن الصيام وتنظيف الخلايا. تعمل الحمضيات النووية غير المشفرة كمنظّمات ذات استجابة سريعة: بعض الميكرو RNA والـ RNA طويلة السلسلة تعزز تراكم الدهون ومقاومة الإنسولين، بينما يبدو أن بعضها يحمي من الاستسقاء الدهني عن طريق كبح إنزيمات تكوين الدهون أو تهدئة الإشارات الالتهابية.
من الآليات إلى الفحوصات والعلاجات
بما أن العلامات فوق الجينية مستقرة وقابلة للعكس في آن واحد، فهي جذابة كأدوات تشخيصية مستقبلية وكمستهدفات دوائية. يمكن الكشف عن بعض أنماط مثيلة الحمض النووي وتواقيع الميكرو RNA بالفعل في الدم ويبدو أنها تتبع شدة MASLD، مما يفتح إمكانية اختبارات دم بسيطة قد تُجنّب بعض المرضى الخزعة الكبدية. على جانب العلاج، يبدو أن عدة أدوية ومركبات طبيعية اختُبرت في الخلايا ونماذج الحيوان، مثل الريسفيراترول، والبيتين، والبيربيرين، وبعض أدوية السكري، تحسّن جزئيًا الكبد الدهني بتعديل منظّمات فوق جينية في الخلايا الكبدية. وفي الوقت نفسه، يحذر المؤلفون من أن هذه المفاتيح تتحكم في العديد من الجينات عبر أعضاء متعددة، لذا قد تتسبب العقاقير واسعة التأثير في آثار جانبية غير مرغوب فيها إذا لم تُستهدف بعناية.
إلى أين قد تقودنا هذه الأبحاث
تختم المقالة بأن التنظيم فوق الجيني في الخلايا الكبدية مركزي لكيفية بدء MASLD وتقدمه وإمكانية عكسه. من خلال رسم تغييرات فوق جينية خاصة بكل خلية باستخدام أدوات الخلية الواحدة و"الأوميكس" الحديثة، يأمل العلماء في تحديد أي المفاتيح تتنبأ بخطر المرض بشكل أفضل، وأيها تشير إلى تقدم خطير، وأيها يمكن التلاعب به بأمان. للقراء غير المتخصصين، الرسالة الأساسية هي أن صحة الكبد ليست محددة بالجينات وحدها. تترك عوامل يومية مثل النظام الغذائي والحالة التمثيلية بصمات كيميائية على حمض نووي ورنا الخلايا الكبدية يمكن أن تدفع العضو نحو الصحة أو المرض. قد يفتح فهم هذه البصمات وإمكانية توجيهها الباب لتشخيص أبكر وعلاجات أكثر دقة وأقل توغلاً لمرض الكبد الدهني.
الاستشهاد: Zhu, G., Zhao, Q., Ran, J. et al. The role of hepatocyte epigenetics in the pathogenesis of metabolic dysfunction-associated steatotic liver disease. Commun Med 6, 276 (2026). https://doi.org/10.1038/s43856-026-01651-1
الكلمات المفتاحية: مرض الكبد الدهني, العلامات فوق الجينية, الخلايا الكبدية, مثيلة الحمض النووي, الحمض النووي الراكب غير المشفر