Clear Sky Science · zh
一种可选择且可增强的丁酸‑FFAR2 信号回路可编程肠嗜铬样 L 细胞的细胞身份
肠道纤维如何与饥饿激素对话
为什么高纤维饮食能让人更容易感到饱并避免体重增加?这项研究通过聚焦一类释放调节食欲激素的特殊肠道细胞来探究这一问题。研究人员展示了当肠道微生物消化纤维产生的一种分子如何重编程这些细胞,使其更倾向于产生肽 YY(PYY,一种抑制饥饿的激素),并提出了可在未来肥胖治疗中放大这一自然通路的方法。
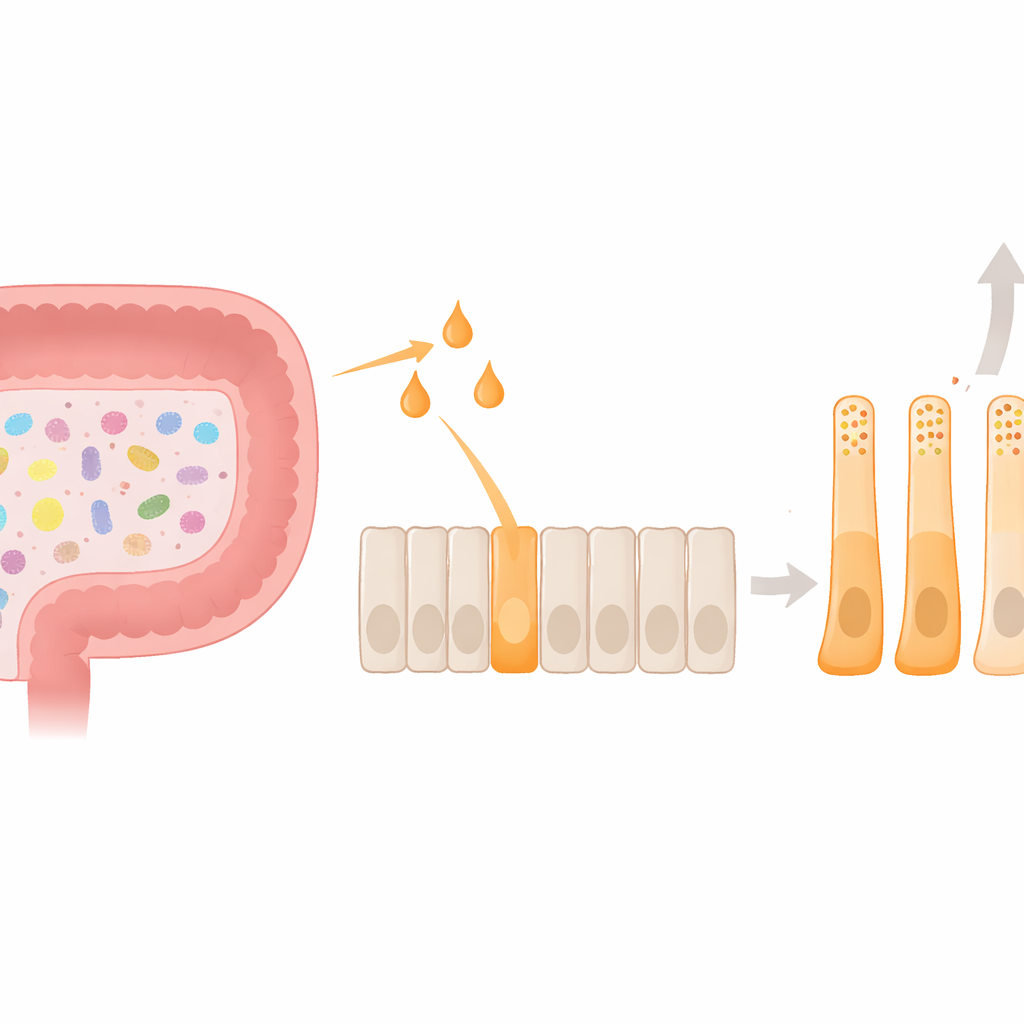
肠道饥饿回路的关键角色
在大肠上皮深处存在肠嗜铬样 L 细胞,这些微小的激素工厂在进食后释放胰高血糖素样肽‑1(GLP‑1)和 PYY。这些激素向大脑传递减少食欲的信号,并有助于维持血糖平衡。肠道微生物组为这一系统增加了额外层面:当细菌发酵膳食纤维时,会产生乙酸、丙酸和丁酸等短链脂肪酸。这些小分子反过来会激活 L 细胞表面的受体 FFAR2。到目前为止,大多数研究集中在这种信号如何触发短暂的激素释放;而它如何持久地塑造 L 细胞本身的身份和行为知之甚少。
丁酸使细胞偏向富含 PYY 的身份
研究团队在人体 L 细胞模型中比较了乙酸、丙酸和丁酸对激素产生和细胞形态的影响。三者都提高了 PYY 基因活性,但丁酸的作用最强,并且独特地提升了实际的 PYY 分泌。同时,丁酸降低了 GLP‑1 前体基因的表达。显微镜下,受丁酸处理的细胞延伸为细长带有长突起的形态,极其类似于在人类结肠组织中观察到的富含 PYY 的细胞。细胞内部的激素储存颗粒发生了变化:PYY 颗粒数量增加并在总体激素库中占比更大。总体来看,这些改变表明丁酸不仅触发短暂的激素释放——它在功能和形态上将细胞引导到一种稳定的、偏向 PYY 的状态。
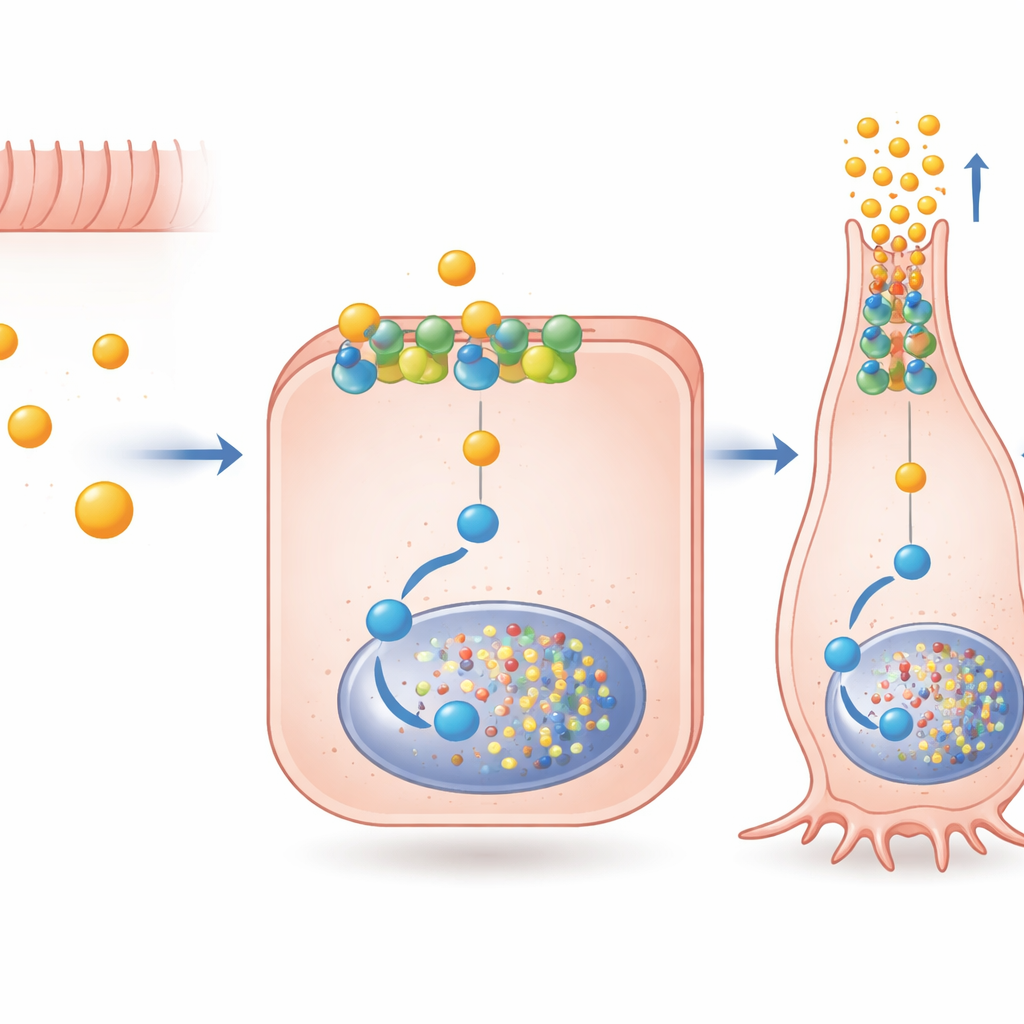
细胞内的专门化信号通路
作者接着探究丁酸如何通过 FFAR2 传递如此特异的信息,FFAR2 是一个可连接多条细胞内信号通路的受体。他们发现乙酸和丙酸强烈激活两条主要的 FFAR2 通路,而丁酸偏好与被称为 Gαi 的蛋白相关联的一条通路。通过用针对性的药物阻断这条通路,他们证明通过 FFAR2 的 Gαi 信号对丁酸提升 PYY 基因活性和启动 Pax6(一个对激素细胞成熟后期重要的转录因子)至关重要。重要的是,这一信号不依赖于受体被内吞进入细胞;它可以直接从外膜发挥作用。一种实验性分子 AZ‑1729,可选择性增强 FFAR2‑Gαi 信号,进一步放大了丁酸对 PYY 和 Pax6 的影响,提示药理学“增强剂”可能精细调节这一自然回路。
引导干细胞走向分泌型肠细胞
为了解丁酸是否也影响新产生的激素分泌细胞的生成,研究人员使用了小鼠结肠类器官——由干细胞培养而成的小型肠道。在该体系中,细胞命运受 Notch 通路强烈控制,Notch 倾向于使细胞保持增殖或吸收导向状态,并阻止其成为像 L 细胞这样的分泌细胞。使用荧光 Notch 报告系统,团队显示丁酸在不同类器官类型和时间点普遍减弱了 Notch 活性,基因表达分析也证实与 Notch 相关的程序被抑制。他们还在这些类器官中观察到罕见的 PYY 阳性细胞增加。在人 L 细胞系中,丁酸选择性地上调了晚期内分泌成熟的标志物,尤其是 NeuroD1 和 Pax6,强调了它在推动细胞向完全发育、产生 PYY 的身份方向上的作用。
从微生物代谢物到未来疗法
这项工作勾勒出一幅连贯的图景:丁酸——结肠中纤维发酵的常见产物——既能重塑成熟 L 细胞,又能影响其发育路径,使之偏向于富含 PYY、形态延长、准备与神经系统交流并抑制食欲的细胞。该信号主要依赖于位于细胞表面的受丁酸激活的 FFAR2–Gαi 回路,并且可以被一种偏向该通路的设计分子进一步强化。对非专业读者而言,关键信息是:我们的肠道微生物对纤维的代谢不仅仅触发短暂的激素爆发——它还能重塑肠道感知食欲细胞的组成,提示了将饮食与靶向药物结合以支持饱腹感和代谢健康的新策略。
引用: Hirdaramani, A., Cheng, CW., Hanyaloglu, A.C. et al. A selective and augmentable butyrate-FFAR2 signal circuitry programs the cellular identity of enteroendocrine L-cells. Commun Biol 9, 606 (2026). https://doi.org/10.1038/s42003-026-09830-5
关键词: 丁酸, 肠嗜铬样 L 细胞, 肽 YY, 肠道微生物组, FFAR2 信号传导