Clear Sky Science · fr
Une voie de signalisation butyrate‑FFAR2 sélective et amplifiable programme l’identité cellulaire des cellules entéroendocrines L
Comment les fibres intestinales parlent aux hormones de la faim
Pourquoi un régime riche en fibres aide‑t‑il à se sentir rassasié et à éviter la prise de poids ? Cette étude explore la question en se concentrant sur un groupe particulier de cellules intestinales qui libèrent des hormones contrôlant l’appétit. Les chercheurs montrent comment une molécule produite lorsque nos microbes intestinaux digèrent les fibres peut reprogrammer ces cellules en faveur du peptide YY (PYY), une hormone qui réduit la faim, et suggèrent des moyens d’amplifier cette voie naturelle pour de futurs traitements de l’obésité.
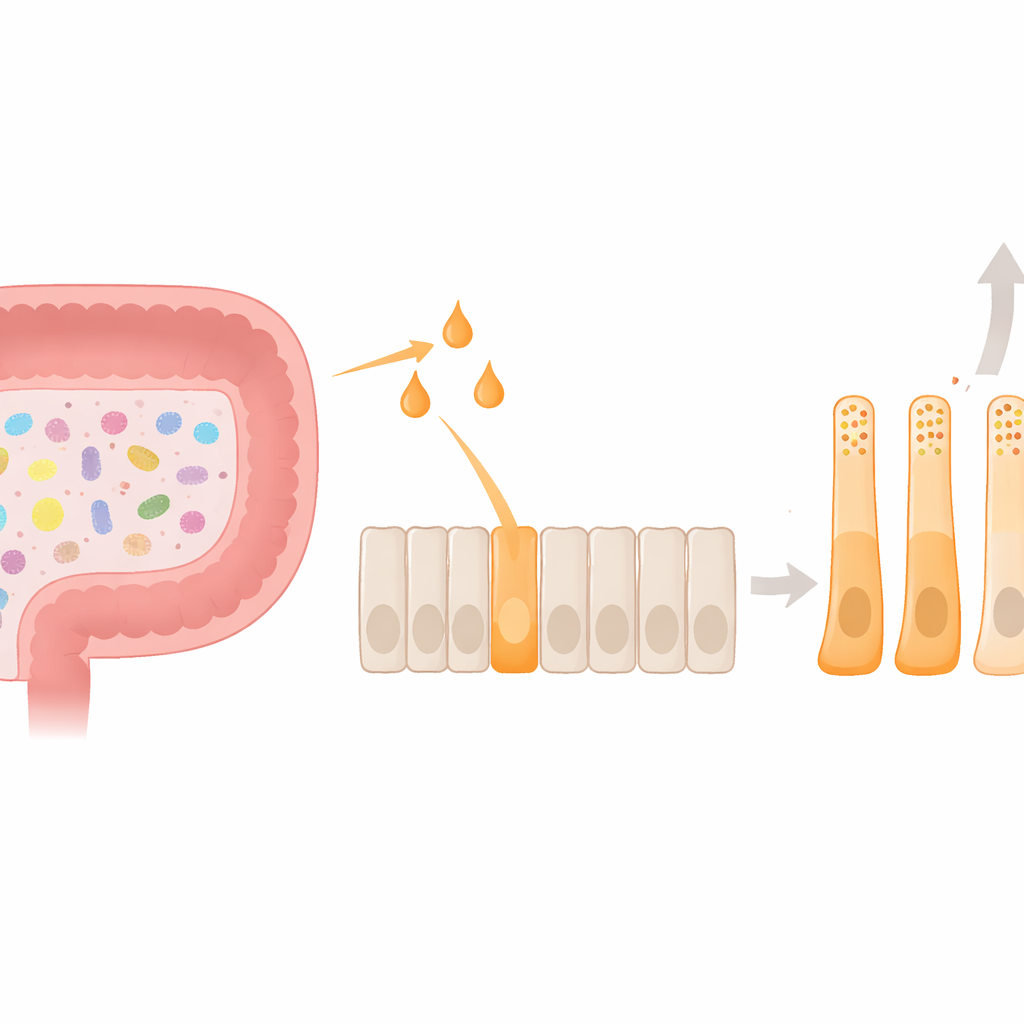
Un acteur clé du circuit de la faim dans l’intestin
Dans la muqueuse du côlon résident les cellules entéroendocrines L, de petites usines hormonales qui libèrent le peptide‑1 de type glucagon (GLP‑1) et le PYY après un repas. Ces hormones envoient des signaux au cerveau pour réduire l’appétit et contribuent à l’équilibre glycémique. Le microbiote intestinal ajoute une couche supplémentaire à ce système : lorsque les bactéries fermentent les fibres alimentaires, elles produisent des acides gras à chaîne courte comme l’acétate, le propionate et le butyrate. Ces petites molécules activent à leur tour un récepteur de surface des cellules L appelé FFAR2. Jusqu’à présent, la plupart des travaux s’étaient concentrés sur la façon dont cette signalisation déclenche des poussées hormonales brèves ; on savait beaucoup moins comment elle pouvait durablement façonner l’identité et le comportement des cellules L elles‑mêmes.
Le butyrate oriente les cellules vers une identité riche en PYY
En utilisant un modèle humain de cellules L, l’équipe a comparé l’effet de l’acétate, du propionate et du butyrate sur la production hormonale et la morphologie cellulaire. Les trois molécules ont augmenté l’activité du gène PYY, mais le butyrate a eu de loin l’effet le plus marqué et a été le seul à accroître la sécrétion effective de PYY. Parallèlement, le butyrate a réduit l’expression du gène précurseur du GLP‑1. Au microscope, les cellules traitées au butyrate se sont allongées et ont développé de longs prolongements, ressemblant fortement aux cellules riches en PYY observées dans le tissu colique humain. En interne, leurs granules de stockage hormonal ont changé : les granules contenant du PYY sont devenus plus nombreux et ont constitué une part plus importante du pool hormonal total. Ensemble, ces modifications montrent que le butyrate ne se contente pas de déclencher une libération hormonale rapide — il oriente les cellules vers un état stable, biaisé en faveur du PYY, tant sur le plan fonctionnel que morphologique.
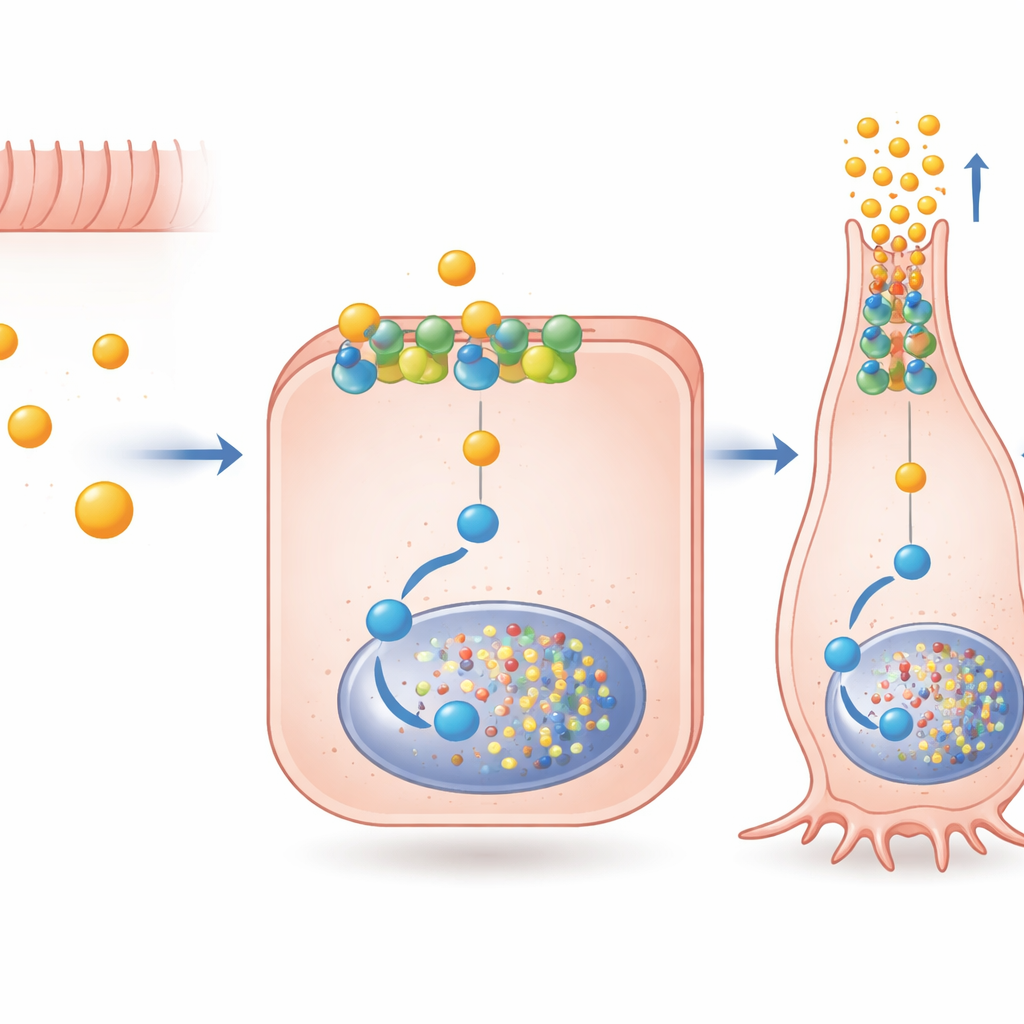
Une voie de signalisation spécialisée à l’intérieur de la cellule
Les auteurs ont ensuite cherché à savoir comment le butyrate transmet un message aussi spécifique via FFAR2, un récepteur pouvant se raccorder à plusieurs voies de signalisation internes. Ils ont constaté que l’acétate et le propionate activent fortement les deux principales voies FFAR2, tandis que le butyrate privilégie une voie liée à une protéine appelée Gαi. En bloquant cette voie avec des médicaments ciblés, ils ont montré que la signalisation Gαi via FFAR2 est nécessaire pour une grande partie de l’augmentation de l’activité du gène PYY induite par le butyrate et pour l’activation de Pax6, un facteur de transcription important pour les stades tardifs de maturation des cellules hormonales. Fait notable, cette signalisation ne dépendait pas de l’internalisation du récepteur ; elle peut fonctionner directement depuis la membrane externe. Une molécule expérimentale, AZ‑1729, qui améliore sélectivement la signalisation FFAR2–Gαi, a encore amplifié les effets du butyrate sur le PYY et Pax6, suggérant que des « amplificateurs » pharmacologiques pourraient affiner ce circuit naturel.
Orienter les cellules souches vers des cellules sécrétoires intestinales
Pour vérifier si le butyrate influence aussi la formation de nouvelles cellules sécrétrices d’hormones, les chercheurs ont utilisé des organoïdes coliques de souris — mini‑intestins cultivés à partir de cellules souches. Dans ce système, le destin cellulaire est fortement contrôlé par la voie Notch, qui tend à maintenir les cellules dans un état prolifératif ou axé sur l’absorption et les empêche de devenir des cellules sécrétoires comme les cellules L. À l’aide d’un rapporteur fluorescent de Notch, l’équipe a montré que le butyrate diminuait l’activité de Notch à travers différents types d’organoïdes et à différents moments, et le profilage de l’expression génique a confirmé que les programmes liés à Notch étaient réprimés. Ils ont aussi observé une augmentation de cellules rares positives pour le PYY dans ces organoïdes. Dans la lignée humaine de cellules L, le butyrate a augmenté sélectivement les marqueurs de la maturation endocrine tardive, en particulier NeuroD1 et Pax6, soulignant son rôle dans la poussée des cellules vers une identité pleinement développée et productrice de PYY.
Du métabolite microbien aux thérapies futures
Ce travail dresse un tableau cohérent : le butyrate, produit courant de la fermentation des fibres dans le côlon, peut à la fois reconfigurer des cellules L matures et influencer leur voie de développement pour favoriser des cellules allongées et riches en PYY, prêtes à communiquer avec le système nerveux et à réduire l’appétit. La signalisation repose largement sur un circuit FFAR2–Gαi activé par le butyrate à la surface cellulaire et peut être renforcée par une molécule conçue pour biaiser cette voie. Pour le grand public, le message clé est que l’action de nos microbes sur les fibres ne se limite pas à déclencher des poussées hormonales de courte durée — elle peut remodeler la composition même des cellules sensorielles intestinales de l’appétit, ouvrant la voie à des stratégies combinant alimentation et médicaments ciblés pour soutenir la satiété et la santé métabolique.
Citation: Hirdaramani, A., Cheng, CW., Hanyaloglu, A.C. et al. A selective and augmentable butyrate-FFAR2 signal circuitry programs the cellular identity of enteroendocrine L-cells. Commun Biol 9, 606 (2026). https://doi.org/10.1038/s42003-026-09830-5
Mots-clés: butyrate, cellules entéroendocrines L, peptide YY, microbiote intestinal, signalisation FFAR2