Clear Sky Science · es
Un circuito de señalización butirato-FFAR2 selectivo y aumentable programa la identidad celular de las células endocrinas intestinales L
Cómo la fibra intestinal habla con las hormonas del hambre
¿Por qué una dieta rica en fibra ayuda a que la gente se sienta saciada y evite el aumento de peso? Este estudio aborda la cuestión al centrarse en un grupo especial de células intestinales que liberan hormonas que controlan el apetito. Los investigadores muestran cómo una molécula producida cuando nuestros microbios digestivos fermentan la fibra puede reprogramar estas células para favorecer el péptido YY (PYY), una hormona que reduce el hambre, y sugieren maneras de potenciar esta vía natural para futuros tratamientos contra la obesidad.
Un actor clave en el circuito del hambre intestinal
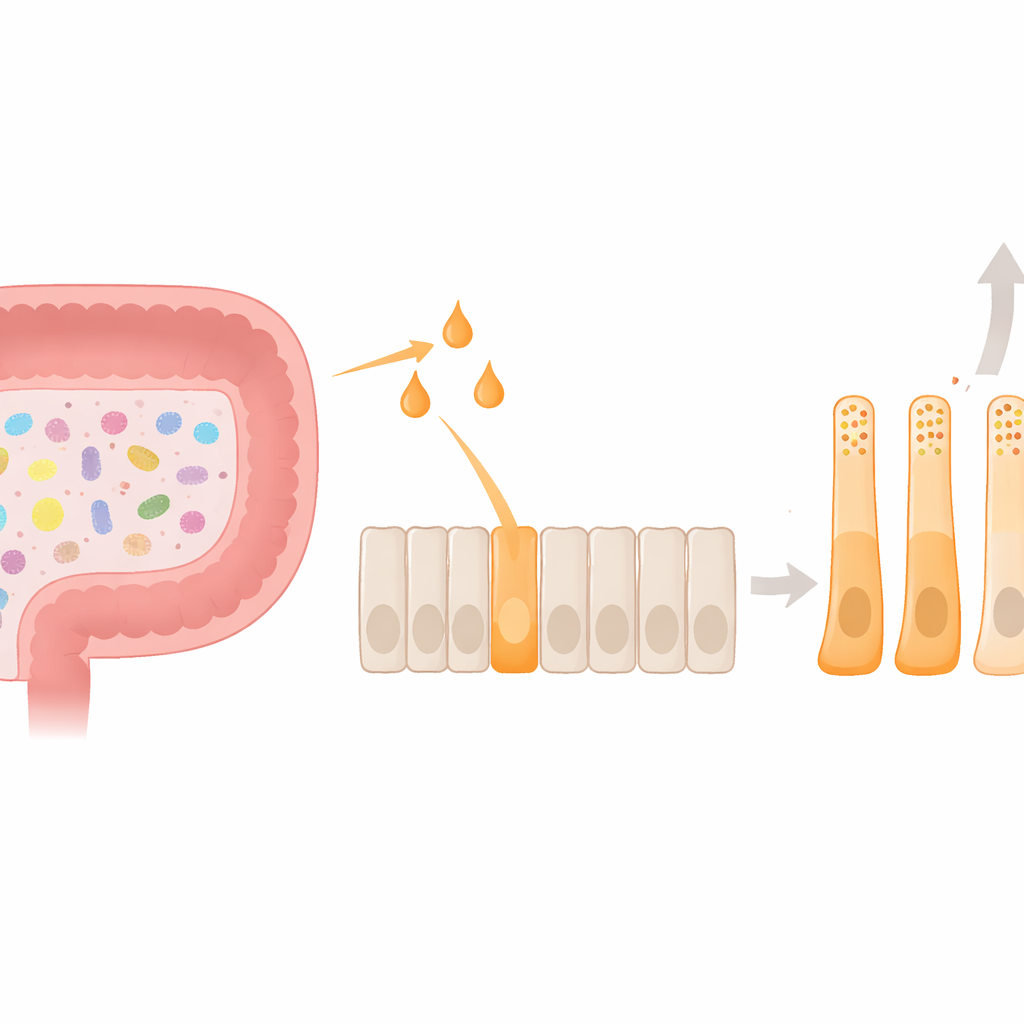
En lo profundo del revestimiento del colon residen las células endocrinas intestinales L, pequeñas fábricas hormonales que liberan péptido similar al glucagón‑1 (GLP‑1) y PYY tras comer. Estas hormonas envían señales al cerebro para reducir el apetito y ayudan a equilibrar la glucemia. El microbioma intestinal añade una capa extra a este sistema: cuando las bacterias fermentan la fibra dietética, producen ácidos grasos de cadena corta como acetato, propionato y butirato. Estas pequeñas moléculas, a su vez, activan un receptor de superficie en las células L llamado FFAR2. Hasta ahora, la mayor parte del trabajo se había centrado en cómo esta señalización desencadena ráfagas cortas de liberación hormonal; se sabía mucho menos sobre cómo podría moldear de forma duradera la identidad y el comportamiento de las propias células L.
El butirato inclina las células hacia una identidad rica en PYY
Utilizando un modelo humano de células L, el equipo comparó cómo acetato, propionato y butirato afectan la producción de hormonas y la morfología celular. Las tres moléculas aumentaron la actividad del gen PYY, pero el butirato tuvo con mucho el efecto más potente y aumentó de forma única la secreción real de PYY. Al mismo tiempo, el butirato redujo la expresión del gen precursor de GLP‑1. Bajo el microscopio, las células tratadas con butirato se alargaron y desarrollaron procesos largos, asemejándose estrechamente a las células ricas en PYY observadas en tejido de colon humano. En su interior, los gránulos de almacenamiento hormonal cambiaron: los gránulos de PYY se volvieron más numerosos y constituyeron una mayor proporción de la reserva total de hormonas. En conjunto, estos cambios muestran que el butirato hace más que provocar una liberación hormonal rápida: orienta a las células hacia un estado estable, sesgado hacia el PYY, tanto en función como en forma.
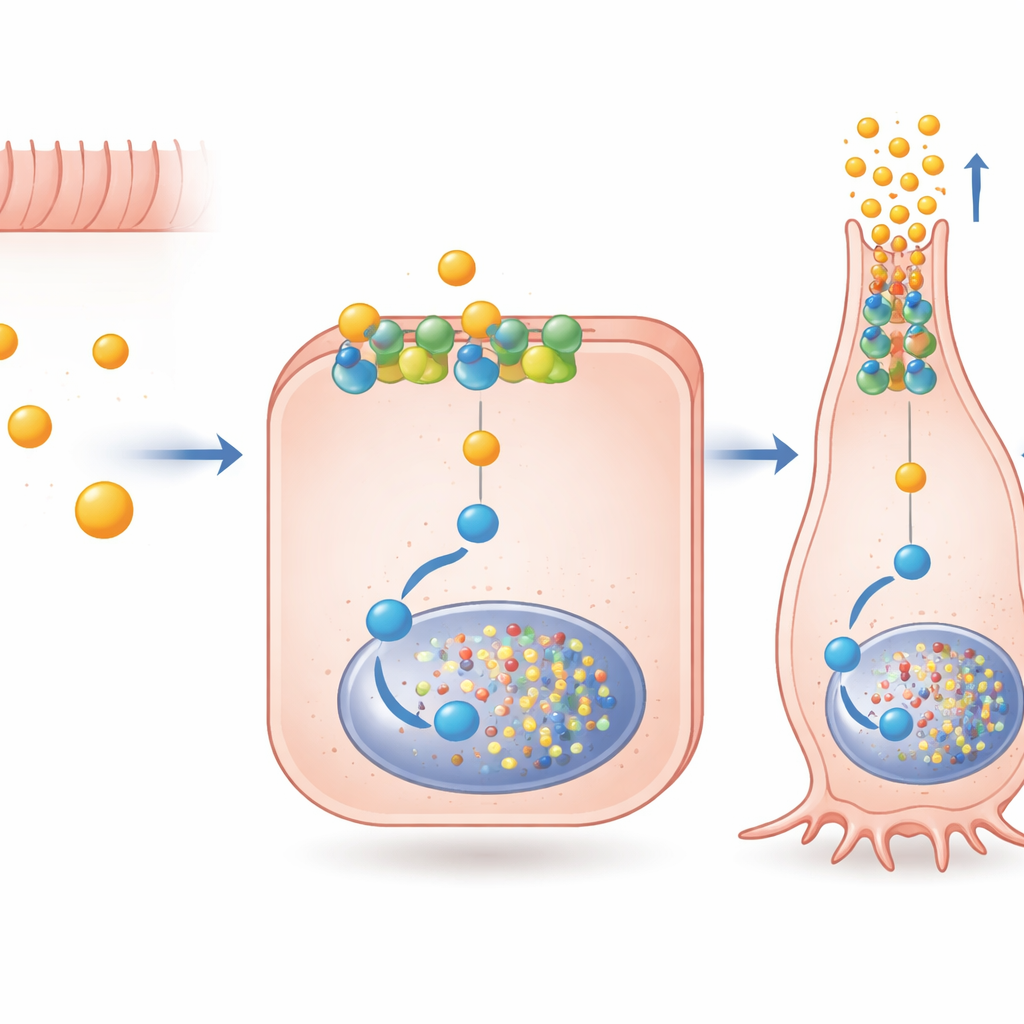
Una vía de señalización especializada dentro de la célula
Los autores se preguntaron luego cómo el butirato transmite un mensaje tan específico a través de FFAR2, un receptor que puede conectarse a más de una ruta de señalización interna. Encontraron que el acetato y el propionato activan con fuerza ambas vías principales de FFAR2, mientras que el butirato prefiere una vinculada a una proteína llamada Gαi. Al bloquear esta vía con fármacos dirigidos, demostraron que la señalización Gαi a través de FFAR2 es necesaria para gran parte del aumento de la actividad del gen PYY inducido por butirato y para la activación de Pax6, un factor de transcripción importante en las fases tardías de maduración de las células productoras de hormonas. Es importante destacar que esta señalización no dependía de que el receptor fuera internalizado; podía operar directamente desde la membrana externa. Una molécula experimental, AZ‑1729, que potencia de forma selectiva la señalización FFAR2‑Gαi, amplificó aún más los efectos del butirato sobre PYY y Pax6, lo que sugiere que “potenciadores” farmacológicos podrían ajustar finamente este circuito natural.
Guiando a las células madre hacia células secretoras intestinales
Para ver si el butirato también influye en cómo se generan nuevas células secretoras de hormonas, los investigadores recurrieron a organoides colónicos de ratón —mini‑intestinos cultivados a partir de células madre. En este sistema, el destino celular está fuertemente controlado por la vía Notch, que tiende a mantener a las células en un estado proliferativo o enfocado en la absorción y les impide convertirse en células secretoras como las L. Usando un informe fluorescente de Notch, el equipo mostró que el butirato atenuó la actividad de Notch en diferentes tipos de organoides y momentos, y el perfil de expresión génica confirmó que los programas relacionados con Notch estaban reprimidos. También observaron un aumento de células raras positivas para PYY dentro de estos organoides. En la línea celular humana de L, el butirato incrementó selectivamente marcadores de maduración endocrina tardía, especialmente NeuroD1 y Pax6, subrayando su papel en empujar a las células hacia una identidad plenamente desarrollada y productora de PYY.
Del metabolito microbiano a futuras terapias
Este trabajo dibuja un panorama coherente: el butirato, un producto común de la fermentación de fibra en el colon, puede tanto reconfigurar células L maduras como influir en su vía de desarrollo para favorecer células alargadas y ricas en PYY que están preparadas para comunicarse con el sistema nervioso y frenar el apetito. La señalización depende en gran medida de un circuito FFAR2–Gαi activado por butirato en la superficie celular y puede reforzarse mediante una molécula diseñada que sesga esta vía. Para el público general, el mensaje clave es que lo que hacen nuestros microbios con la fibra no solo desencadena ráfagas hormonales de corta duración: puede remodelar la propia composición de las células sensoras del apetito en el intestino, lo que sugiere nuevas estrategias para aprovechar la dieta y fármacos dirigidos para favorecer la saciedad y la salud metabólica.
Cita: Hirdaramani, A., Cheng, CW., Hanyaloglu, A.C. et al. A selective and augmentable butyrate-FFAR2 signal circuitry programs the cellular identity of enteroendocrine L-cells. Commun Biol 9, 606 (2026). https://doi.org/10.1038/s42003-026-09830-5
Palabras clave: butirato, células endocrinas intestinales L, péptido YY, microbioma intestinal, señalización FFAR2