Clear Sky Science · tr
Seçici ve güçlendirilebilir bir bütirat‑FFAR2 sinyal devresi, enteroendokrin L‑hücrelerin hücresel kimliğini programlar
Bağırsak lifi açlık hormonlarıyla nasıl konuşur
Yüksek lifli bir diyet insanların neden tokluk hissetmesine ve kilo almaktan kaçınmasına yardımcı olur? Bu çalışma, iştahı kontrol eden hormonları salgılayan özel bir bağırsak hücresi grubuna odaklanarak bu soruyu inceliyor. Araştırmacılar, bağırsak mikrobilerimizin lifleri sindirirken ürettiği bir molekülün bu hücreleri iştahı azaltan peptid YY (PYY) lehine programlayabileceğini gösteriyor ve bu doğal yolun gelecekte obezite tedavileri için nasıl güçlendirilebileceğine dair yollar öneriyor.
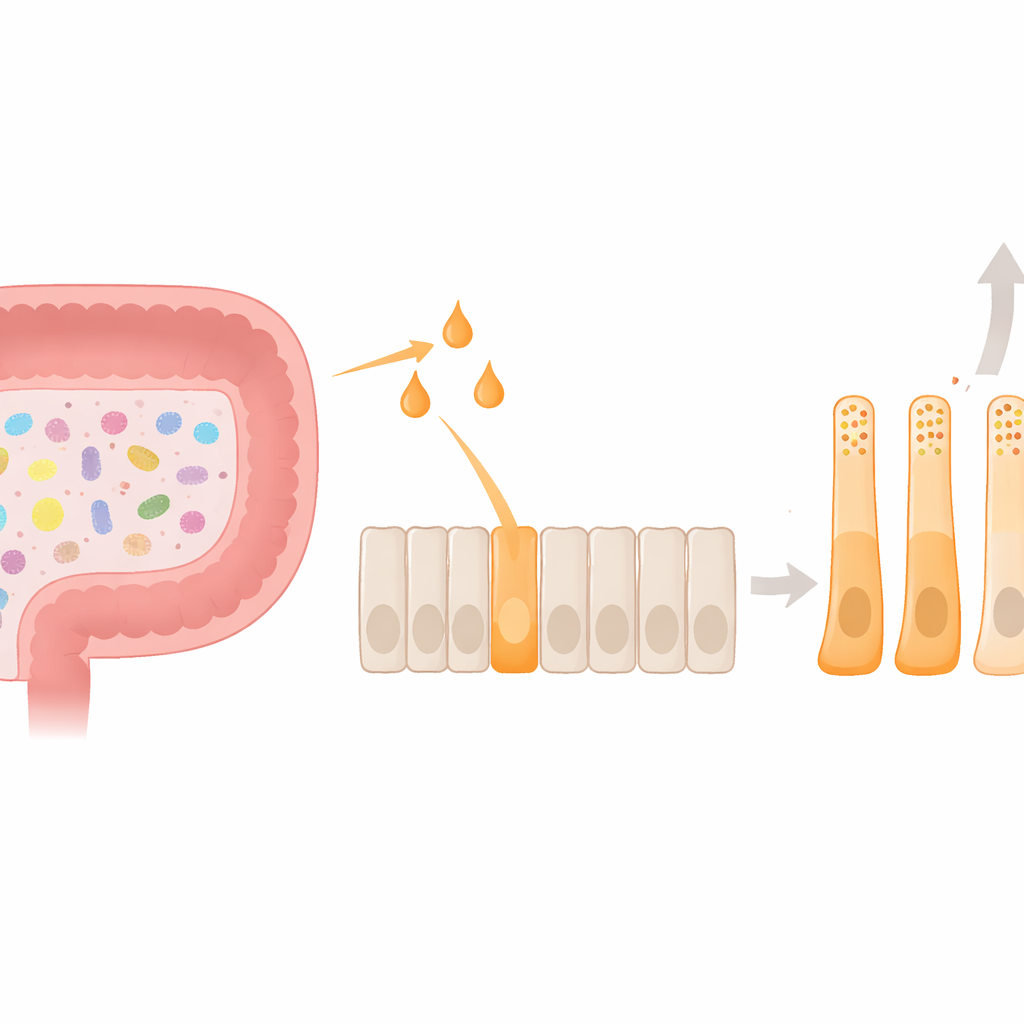
Bağırsaktaki açlık devresinin kilit oyuncusu
Kalın bağırsağın iç yüzeyinde, yediğimizde glukagon‑benzeri peptid‑1 (GLP‑1) ve PYY salgılayan, küçük hormon fabrikaları olan enteroendokrin L‑hücreleri bulunur. Bu hormonlar beyne iştahı azaltması için sinyal gönderir ve kan şekeri dengesine yardımcı olur. Bağırsak mikrobiyomu bu sisteme ekstra bir katman ekler: bakteriler diyet liflerini fermente ettiğinde asetat, propiyonat ve bütirat gibi kısa zincirli yağ asitleri üretir. Bu küçük moleküller de L‑hücrelerin yüzeyindeki FFAR2 adlı bir reseptörü aktive eder. Bugüne kadar yapılan çalışmaların çoğu bu sinyallemenin kısa süreli hormon salınımını nasıl tetiklediğine odaklanmıştı; bu sinyalin L‑hücrelerin kimliğini ve davranışını kalıcı olarak nasıl şekillendirebileceği ise çok daha az bilinirdi.
Bütirat hücreleri PYY açısından zengin bir kimliğe yönlendiriyor
Bir insan L‑hücre modeli kullanarak ekip, asetat, propiyonat ve bütiratın hormon üretimi ve hücre morfolojisi üzerindeki etkilerini karşılaştırdı. Üç molekül de PYY gen aktivitesini artırdı, ancak bütirat açık ara en güçlü etkiye sahipti ve benzersiz şekilde gerçek PYY salgısını da yükseltti. Aynı zamanda bütirat GLP‑1 öncül geni ifadesini azalttı. Mikroskop altında, bütiratla muamele edilen hücreler uzun uzantılara sahip, uzamış formlara dönüştü ve insan kolon dokusunda görülen PYY‑zengin hücrelere çok benzedi. İçeride hormon depolama granülleri değişti: PYY granülleri daha çok sayıda hale geldi ve toplam hormon havuzunda daha büyük bir pay oluşturdu. Bu değişiklikler birlikte bütiratın sadece kısa süreli hormon salınımı tetiklemekten öte, hücreleri işlev ve form açısından stabil, PYY eğilimli bir duruma yönlendirdiğini gösteriyor.
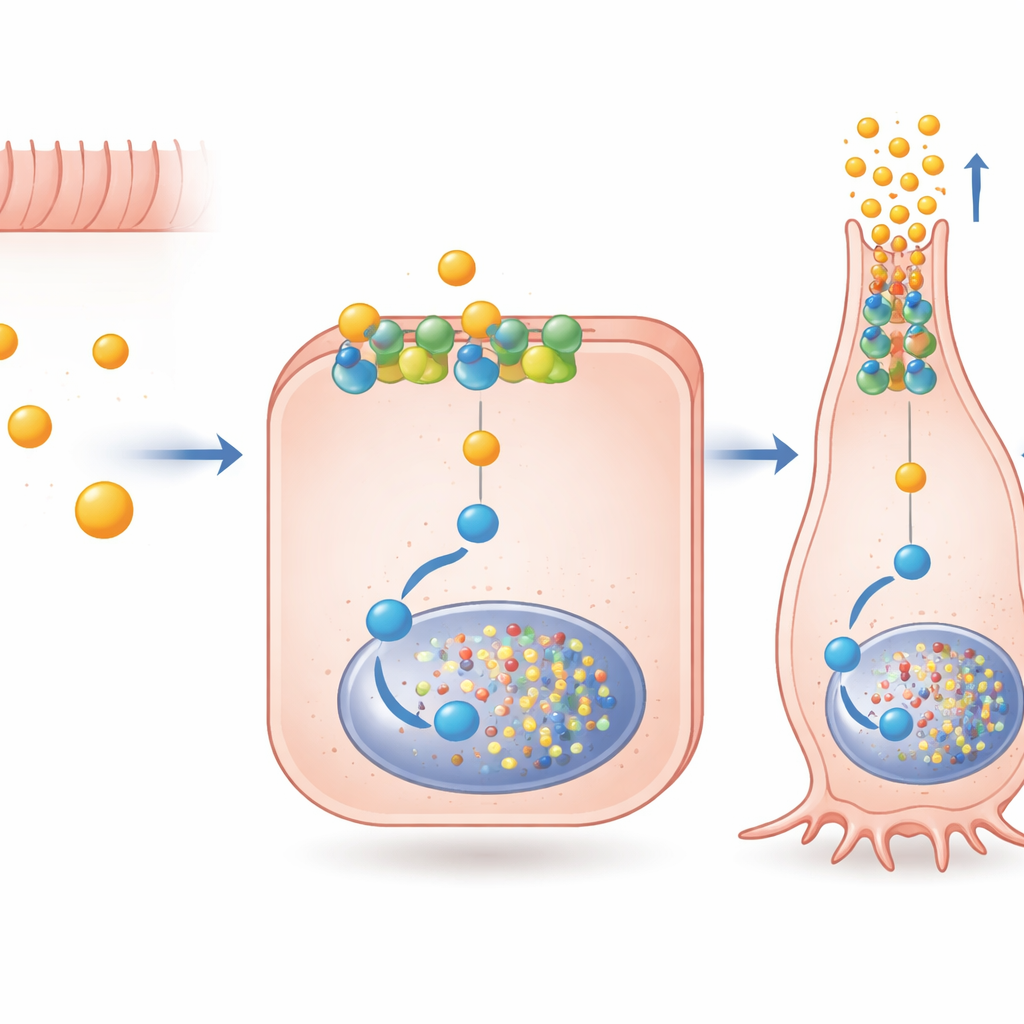
Hücre içindeki uzman bir sinyal yolculuğu
Yazarlar daha sonra bütiratın FFAR2 aracılığıyla böyle seçici bir mesajı nasıl ilettiğini sorguladılar; FFAR2 birden fazla iç sinyal yoluna bağlanabilen bir reseptördür. Asetat ve propiyonatın her iki ana FFAR2 yolunu güçlü şekilde aktive ettiğini, oysa bütiratın Gαi adlı bir proteine bağlı olan bir yolu tercih ettiğini buldular. Bu yolu hedefli ilaçlarla engelleyerek, FFAR2 üzerinden Gαi sinyallemesinin bütiratın PYY gen aktivitesindeki artışının büyük bir kısmı ve hormon‑hücresi olgunlaşmasının ileri evreleri için önemli olan Pax6 adlı transkripsiyon faktörünün açılması için gerekli olduğunu gösterdiler. Önemli olarak, bu sinyalin reseptörün hücre içine çekilmesine bağlı olmadığı; dış zardan doğrudan çalışabileceği görüldü. FFAR2‑Gαi sinyalini seçici olarak güçlendiren deneysel bir molekül olan AZ‑1729, PYY ve Pax6 üzerindeki bütirat etkilerini daha da artırdı; bu da farmakolojik "güçlendiricilerin" bu doğal devreyi ince ayarlayabileceğine işaret ediyor.
Kök hücreleri salgılayıcı bağırsak hücrelerine yönlendirmek
Bütiratın yeni hormon‑salgılayan hücrelerin oluşumunu da etkileyip etkilemediğini görmek için araştırmacılar, kök hücrelerden yetiştirilen mini bağırsaklar olan fare kolonik organoidlerine yöneldiler. Bu sistemde hücre kaderi büyük ölçüde, hücreleri çoğalmaya veya emilim odaklı durumda tutma ve onları L‑hücre gibi salgılayıcı hücrelere dönüşmekten engelleme eğiliminde olan Notch yolu tarafından kontrol edilir. Floresan bir Notch raporlama aracı kullanarak ekip, bütiratın farklı organoid türleri ve zaman noktalarında Notch aktivitesini azalttığını ve gen ifade profillemesiyle Notch‑ile ilişkili programların baskılandığını doğruladı. Ayrıca bu organoidlerde nadir bulunan PYY‑pozitif hücrelerin arttığını gözlemlediler. İnsan L‑hücre hattında ise bütirat özellikle NeuroD1 ve Pax6 gibi geç endocrine olgunlaşma belirteçlerini seçici olarak artırdı; bu da hücreleri tam gelişmiş, PYY üreten bir kimliğe itmedeki rolünü vurguluyor.
Mikrobiyal metabolitten gelecekteki terapilere
Bu çalışma tutarlı bir tablo çiziyor: kolonlardaki lif fermantasyonunun yaygın bir ürünü olan bütirat, hem olgun L‑hücreleri yeniden kablolayabiliyor hem de gelişim yolunu PYY‑zengin, uzamış hücreleri tercih edecek şekilde etkileyebiliyor; bu hücreler sinir sistemiyle iletişim kurmaya ve iştahı baskılamaya hazır hale geliyor. Sinyalleme büyük ölçüde yüzeydeki bütirat‑aktif FFAR2–Gαi devresine bağlı ve bu yolcu bir dizayn molekülle daha da güçlendirilebiliyor. Halk için ana mesaj şudur: bağırsak mikrobilerimizin lifle yaptıkları sadece kısa süreli hormon patlamaları tetiklemekle kalmıyor—bağırsaktaki iştah algılayan hücrelerin bileşimini yeniden şekillendiriyor ve diyeti ile hedefe yönelik ilaçları kullanarak tokluk ve metabolik sağlığı desteklemek için yeni stratejiler öneriyor.
Atıf: Hirdaramani, A., Cheng, CW., Hanyaloglu, A.C. et al. A selective and augmentable butyrate-FFAR2 signal circuitry programs the cellular identity of enteroendocrine L-cells. Commun Biol 9, 606 (2026). https://doi.org/10.1038/s42003-026-09830-5
Anahtar kelimeler: bütirat, enteroendokrin L‑hücreler, peptid YY, bağırsak mikrobiyomu, FFAR2 sinyallemesi