Clear Sky Science · ru
Селективная и усиливаемая схема сигнализации бутирата–FFAR2 программирует клеточную идентичность энтероэндокринных L‑клеток
Как клетчатка в кишечнике «разговаривает» с гормонами голода
Почему диета с высоким содержанием клетчатки помогает испытывать насыщение и избегать набора веса? Это исследование углубляется в вопрос, фокусируясь на особой популяции кишечных клеток, которые выделяют гормоны, контролирующие аппетит. Авторы показывают, как молекула, образующаяся при расщеплении клетчатки нашими микробами, может перепрограммировать эти клетки в пользу пептида YY (PYY) — гормона, снижающего аппетит — и предлагают пути, как этот природный механизм можно усилить для будущих методов лечения ожирения.
Ключевой игрок в цепи голода кишечника
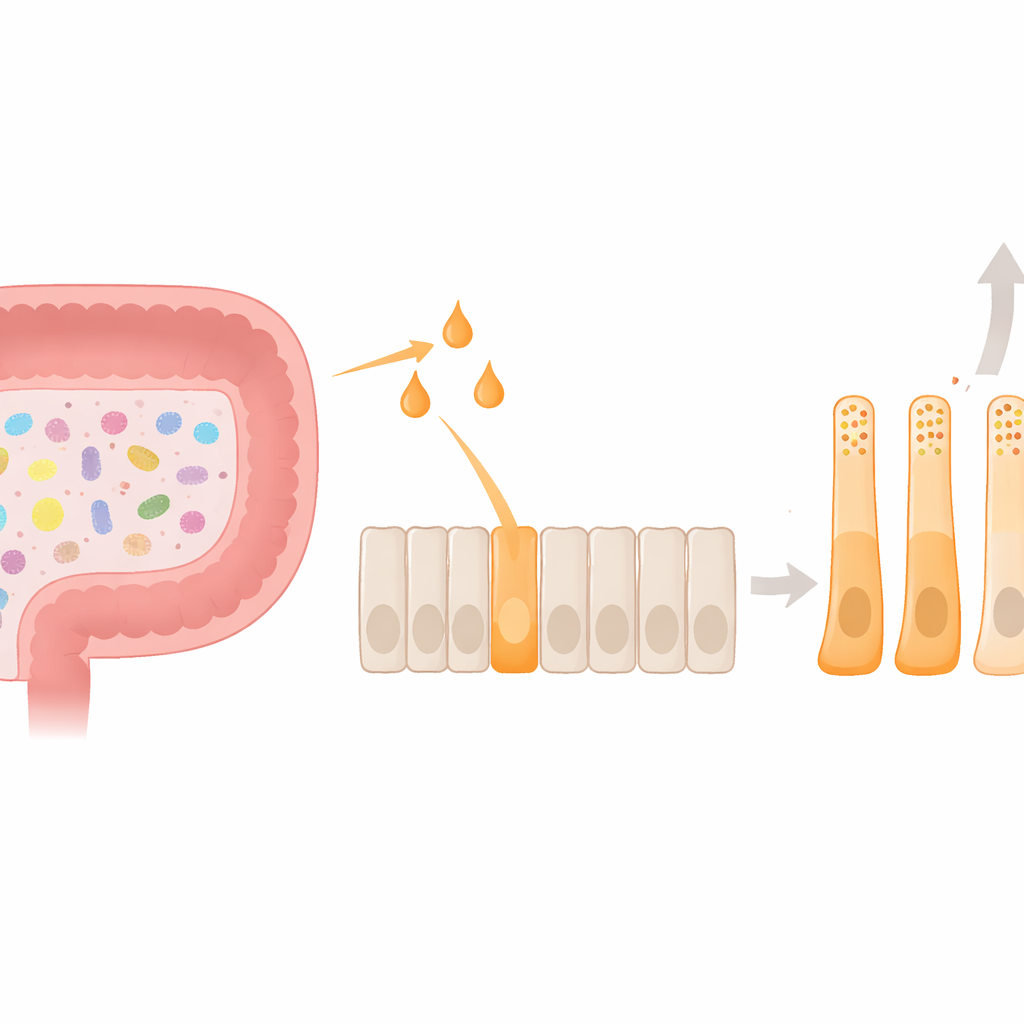
Глубоко в слизистой оболочке толстой кишки находятся энтероэндокринные L‑клетки — крошечные гормонопродуцирующие «фабрики», которые после еды выделяют глюкагоноподобный пептид‑1 (GLP‑1) и PYY. Эти гормоны посылают в мозг сигналы о снижении аппетита и помогают поддерживать гомеостаз глюкозы. Микробиом кишечника добавляет к этой системе ещё один слой: при ферментации пищевой клетчатки бактерии вырабатывают короткоцепочечные жирные кислоты, такие как ацетат, пропионат и бутират. Эти небольшие молекулы, в свою очередь, активируют поверхностный рецептор на L‑клетках, называемый FFAR2. До настоящего времени большинство работ сосредотачивалось на том, как эта сигнализация вызывает кратковременное выбрасывание гормонов; гораздо меньше было известно о том, как она может устойчиво формировать идентичность и поведение самих L‑клеток.
Бутират склоняет клетки к PYY‑обогащённой идентичности
Используя модель человеческих L‑клеток, исследователи сравнили влияние ацетата, пропионата и бутирата на синтез гормонов и форму клеток. Все три молекулы усиливали активность гена PYY, но бутират оказал наиболее выраженный эффект и уникально увеличивал фактическую секрецию PYY. Одновременно бутират снижал экспрессию гена предшественника GLP‑1. Под микроскопом обработанные бутиратом клетки растягивались в удлинённые формы с длинными отростками, напоминая PYY‑богатые клетки, наблюдаемые в ткани человеческой ободочной кишки. Внутри их гранул для хранения гормонов произошёл сдвиг: гранул PYY стало больше, и они составляли большую долю общего пула гормонов. В совокупности эти изменения показывают, что бутират делает больше, чем просто вызывает кратковременный выброс гормона — он направляет клетки в стабильное, смещённое в пользу PYY состояние как по функции, так и по форме.
Специализированный сигнальный путь внутри клетки
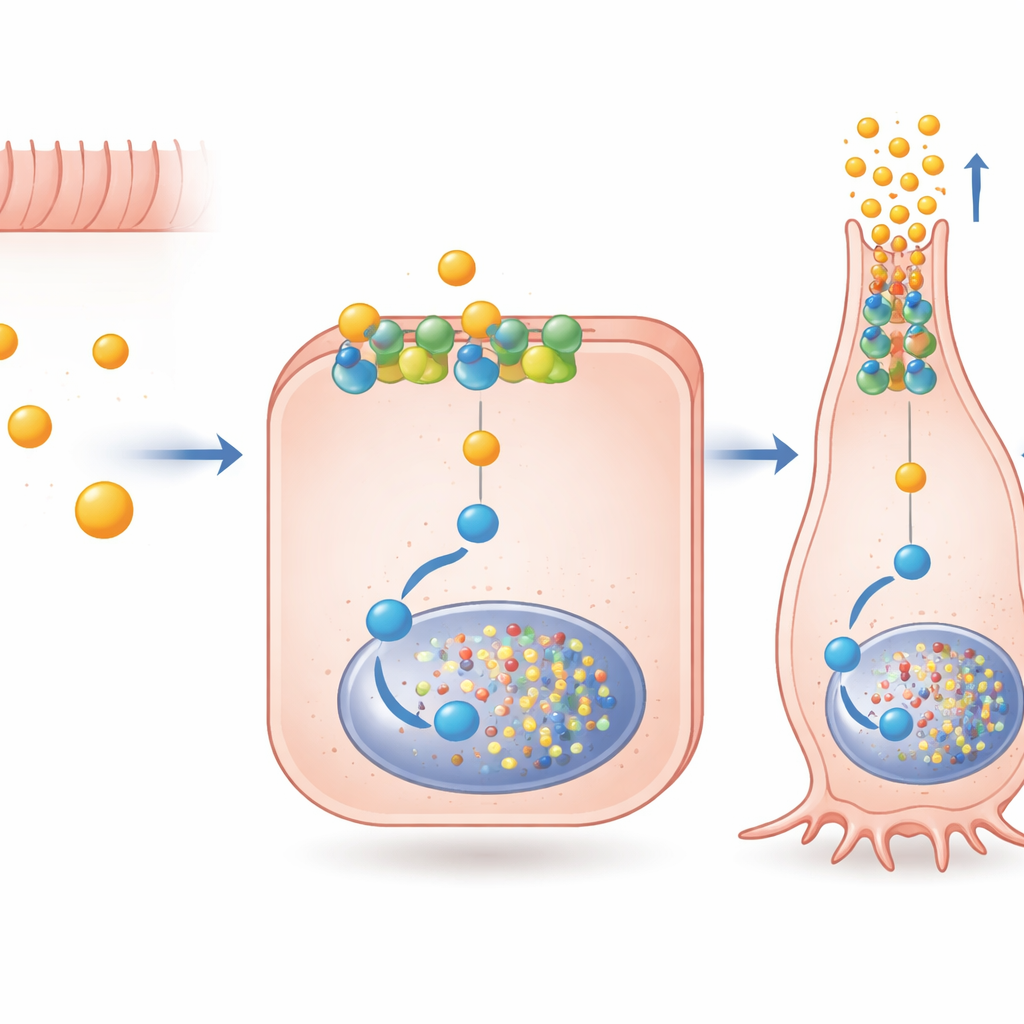
Авторы затем выясняли, как бутират передаёт такое специфическое сообщение через FFAR2, рецептор, который может связываться более чем с одним внутриклеточным сигнальным маршрутом. Они обнаружили, что ацетат и пропионат сильно активируют оба основных пути FFAR2, тогда как бутират предпочитает путь, связанный с белком Gαi. Блокируя этот путь с помощью направленных препаратов, они показали, что сигнализация Gαi через FFAR2 необходима для значительной части эффекта бутирата на активность гена PYY и для включения Pax6 — фактора транскрипции, важного на поздних стадиях созревания гормонопродуцирующих клеток. Важно, что эта сигнализация не зависела от эндоцитоза рецептора; она могла работать непосредственно из наружной мембраны. Экспериментальная молекула AZ‑1729, селективно усиливающая сигнализацию FFAR2–Gαi, дополнительно усиливала эффекты бутирата на PYY и Pax6, что намекает на возможность фармакологического «усиления» этой природной схемы.
Направление стволовых клеток к секреторным клеткам кишечника
Чтобы проверить, влияет ли бутират на образование новых гормон‑секретирующих клеток, исследователи использовали органоиды толстой кишки мыши — мини‑кишечники, выращенные из стволовых клеток. В этой системе судьба клетки в значительной степени контролируется путем Notch, который склоняет клетки к пролиферации или всасывательной роли и препятствует их превращению в секреторные клетки, такие как L‑клетки. Используя флуоресцентный репортер пути Notch, команда показала, что бутират ослаблял активность Notch в разных типах органоидов и в разные моменты времени, а профиль экспрессии генов подтвердил подавление программ, связанных с Notch. Они также наблюдали увеличение редких PYY‑положительных клеток в этих органоидах. В человеческой линии L‑клеток бутират селективно повышал маркеры позднего эндокринного созревания, особенно NeuroD1 и Pax6, подчёркивая его роль в продвижении клеток к полностью развитой, продуцирующей PYY идентичности.
От микробного метаболита к потенциальным терапиям
Эта работа рисует согласованную картину: бутират, распространённый продукт ферментации клетчатки в толстой кишке, может как перепрограммировать зрелые L‑клетки, так и влиять на их путь развития в пользу PYY‑обогащённых, удлинённых клеток, готовых взаимодействовать с нервной системой и подавлять аппетит. Сигнализация во многом опирается на активируемую бутиратом цепь FFAR2–Gαi на поверхности клетки и может быть дополнительно усилена дизайнерской молекулой, смещающей баланс этого пути. Для неспециалистской аудитории ключевая мысль такова: то, что наши кишечные микробы делают с клетчаткой, не только вызывает кратковременные выбросы гормонов — это может изменить сам состав клеток, отвечающих за ощущение голода, что открывает новые стратегии использования диеты и целенаправленных препаратов для поддержания сытости и метаболического здоровья.
Цитирование: Hirdaramani, A., Cheng, CW., Hanyaloglu, A.C. et al. A selective and augmentable butyrate-FFAR2 signal circuitry programs the cellular identity of enteroendocrine L-cells. Commun Biol 9, 606 (2026). https://doi.org/10.1038/s42003-026-09830-5
Ключевые слова: бутират, энтероэндокринные L‑клетки, пептид YY, микробиом кишечника, сигнализация FFAR2