Clear Sky Science · nl
Een selectief en versterkbaar butyraat‑FFAR2 signaalcircuit programmeert de cellulaire identiteit van entero-endocriene L‑cellen
Hoe vezels in de darm met hongergevoelens communiceren
Waarom helpt een vezelrijk dieet mensen om zich verzadigd te voelen en gewichtstoename te vermijden? Deze studie onderzoekt die vraag door in te zoomen op een speciale groep darmcellen die hormonen vrijgeven die de eetlust reguleren. De onderzoekers laten zien hoe een molecuul dat ontstaat wanneer onze darmmicroben vezels afbreken deze cellen kan herprogrammeren in de richting van peptide YY (PYY), een hormoon dat de honger remt, en suggereren manieren waarop deze natuurlijke route versterkt zou kunnen worden voor toekomstige obesitasbehandelingen.
Een sleutelspeler in het honger‑circuit van de darm
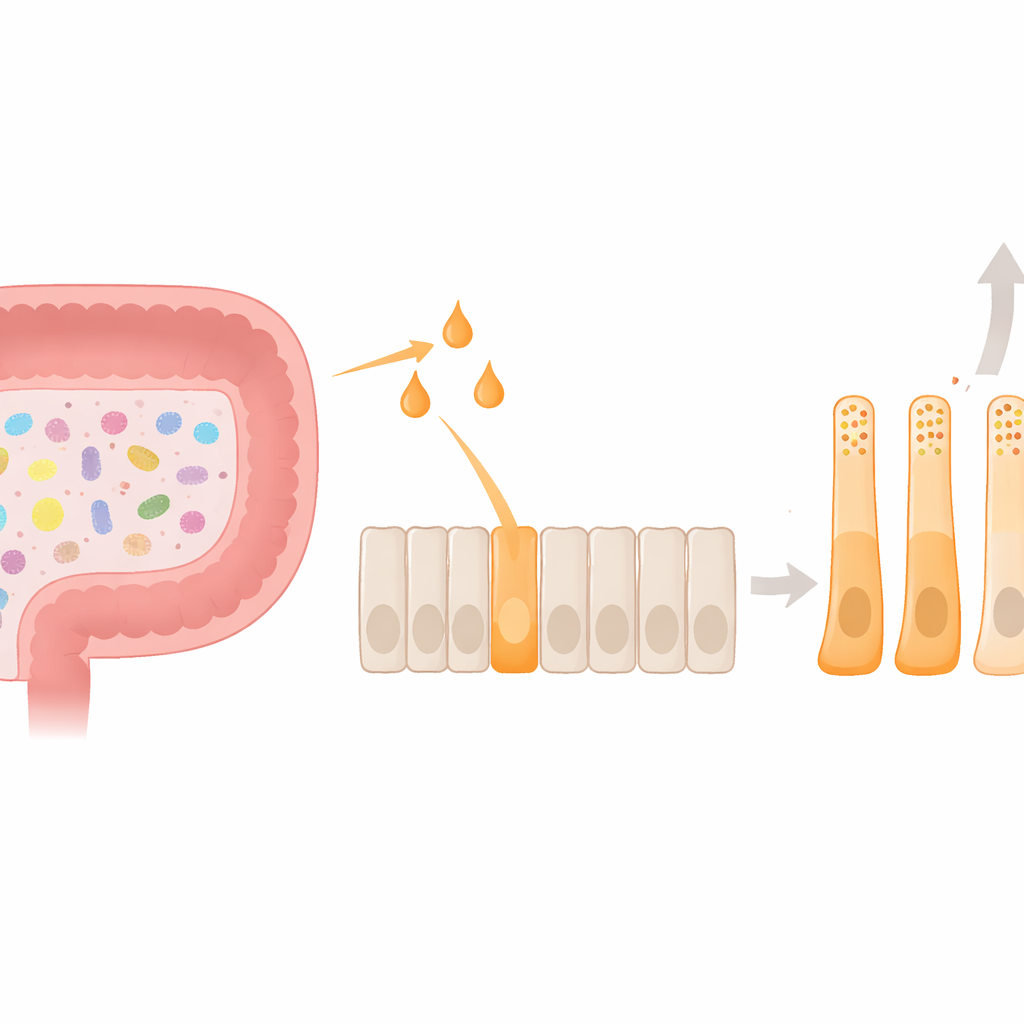
Diep in het slijmvlies van de dikke darm bevinden zich entero‑endocriene L‑cellen, kleine hormoonfabriekjes die na het eten glucagon‑achtig peptide‑1 (GLP‑1) en PYY vrijgeven. Deze hormonen geven signalen aan de hersenen om de eetlust te verminderen en helpen de bloedsuiker te reguleren. Het darmmicrobioom voegt een extra laag toe aan dit systeem: wanneer bacteriën voedingsvezels vergisten, produceren ze korteketenvetzuren zoals acetaat, propionaat en butyraat. Deze kleine moleculen activeren op hun beurt een membraanreceptor op L‑cellen genaamd FFAR2. Tot nu toe richtte het meeste werk zich op hoe deze signalering korte hormoonpiekjes veroorzaakt; veel minder was bekend over hoe het de identiteit en het gedrag van de L‑cellen zelf blijvend zou kunnen vormen.
Butyraat kantelt cellen naar een PYY‑rijke identiteit
Met een humaan L‑celmodel vergeleek het team hoe acetaat, propionaat en butyraat de hormoonproductie en celvorm beïnvloeden. Alle drie de moleculen verhoogden de activiteit van het PYY‑gen, maar butyraat had verreweg het sterkste effect en verhoogde daarnaast uniek de daadwerkelijke PYY‑secretie. Tegelijkertijd verlaagde butyraat de expressie van het GLP‑1‑voorlopergen. Onder de microscoop strekten butyraat‑behandelde cellen uit tot langgerekte vormen met lange uitlopers, sterk gelijkend op PYY‑rijke cellen in menselijk colonweefsel. Intern verschoven hun hormoonopslaggranules: PYY‑granules werden talrijker en namen een groter deel van de totale hormoonvoorraad in. Samen tonen deze veranderingen aan dat butyraat meer doet dan een korte hormoonvrijgave opwekken — het stuurt cellen naar een stabiele, op PYY bevoordeelde staat in zowel functie als vorm.
Een gespecialiseerd signaalpad binnen de cel
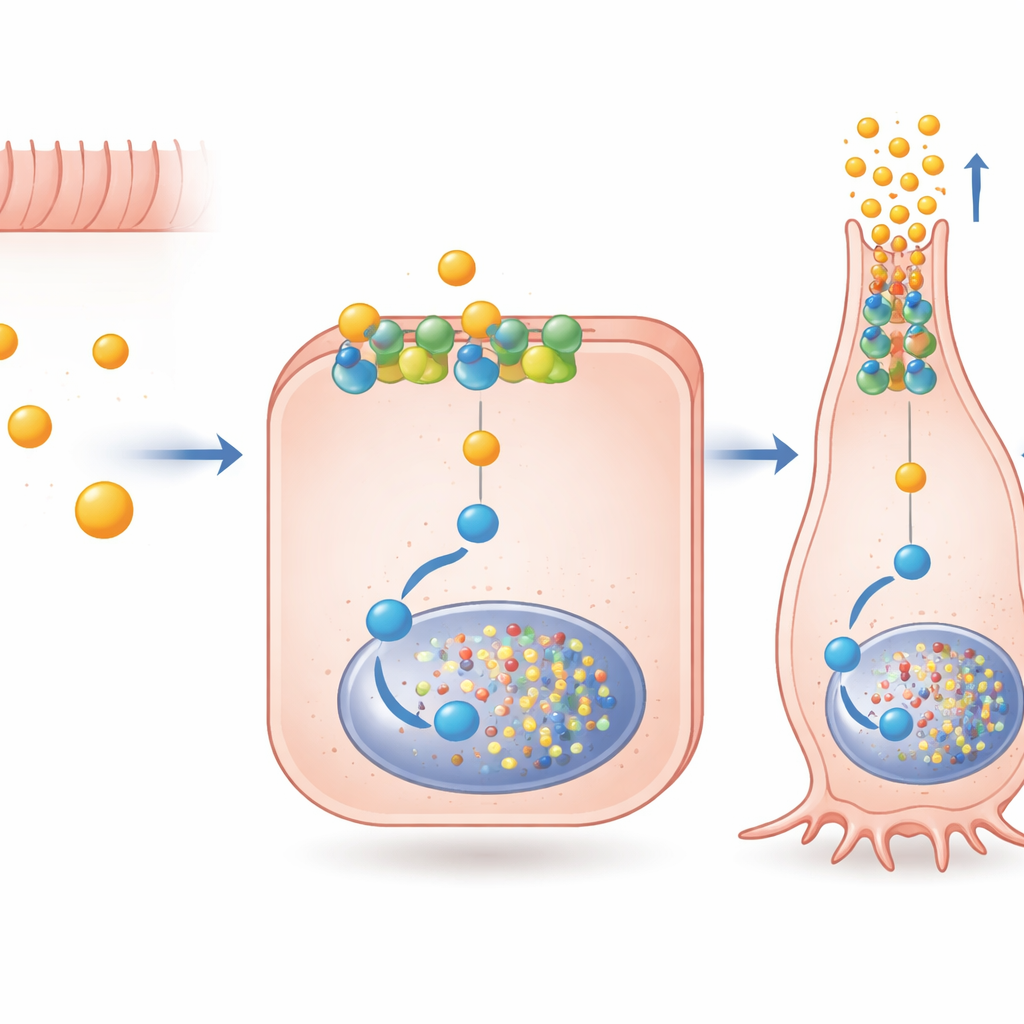
De auteurs vroegen zich vervolgens af hoe butyraat zo’n specifiek bericht door FFAR2 zendt, een receptor die met meer dan één interne signaalroute kan koppelen. Ze vonden dat acetaat en propionaat beide belangrijke FFAR2‑routes sterk activeren, terwijl butyraat een voorkeur heeft voor een route die gekoppeld is aan een eiwit genaamd Gαi. Door deze route met gerichte geneesmiddelen te blokkeren, toonden ze aan dat Gαi‑signalering via FFAR2 nodig is voor een groot deel van butyraats stimulatie van PYY‑genactiviteit en voor het inschakelen van Pax6, een transcriptiefactor die belangrijk is voor latere stadia van hormooncelmaturatie. Belangrijk is dat deze signalering niet afhankelijk was van het naar binnen sleuren van de receptor; het kon direct vanaf het buitenmembraan werken. Een experimenteel molecuul, AZ‑1729, dat selectief FFAR2‑Gαi‑signalering versterkt, vergrootte de effecten van butyraat op PYY en Pax6 nog verder, wat suggereert dat farmacologische “versterkers” dit natuurlijke circuit fijn kunnen afstemmen.
Sturing van stamcellen naar secretorische darmcellen
Om te onderzoeken of butyraat ook beïnvloedt hoe nieuwe hormoon‑afgevende cellen worden gemaakt, gebruikten de onderzoekers muis‑colische organoïden — mini‑darmen gekweekt uit stamcellen. In dit systeem wordt het cel lot sterk gecontroleerd door het Notch‑pad, dat neigt cellen in een prolifereerde of absorptiegerichte staat te houden en verhindert dat ze secretorische cellen zoals L‑cellen worden. Met een fluorescerende Notch‑reporter liet het team zien dat butyraat de Notch‑activiteit dempte in verschillende organoïde‑typen en tijdstippen, en genexpressieprofilering bevestigde dat Notch‑gerelateerde programma’s werden onderdrukt. Ze zagen ook een toename van zeldzame PYY‑positieve cellen binnen deze organoïden. In de humane L‑cellijn verhoogde butyraat selectief markers van late endocriene rijping, vooral NeuroD1 en Pax6, waarmee het belang wordt benadrukt van butyraat in het duwen van cellen naar een volledig ontwikkelde, PYY‑producerende identiteit.
Van microbieel metaboliet naar toekomstige therapieën
Dit werk schetst een samenhangend beeld: butyraat, een veelvoorkomend product van vezelvergisting in de dikke darm, kan zowel rijpe L‑cellen herbedraden als hun ontwikkelingspad beïnvloeden om PYY‑rijke, langgerekte cellen te bevoordelen die klaar zijn om met het zenuwstelsel te communiceren en de eetlust te remmen. De signalering berust grotendeels op een butyraat‑geactiveerd FFAR2–Gαi‑circuit aan het celoppervlak en kan verder worden versterkt door een ontworpen molecuul dat deze route bevoordeelt. Voor niet‑specialisten is de kernboodschap dat wat onze darmmicroben met vezels doen niet alleen korte hormoonpiekjes veroorzaakt — het kan de samenstelling van de darmcellen die op verzadiging letten veranderen, wat nieuwe strategieën suggereert om dieet en gerichte geneesmiddelen te benutten ter ondersteuning van verzadiging en metabole gezondheid.
Bronvermelding: Hirdaramani, A., Cheng, CW., Hanyaloglu, A.C. et al. A selective and augmentable butyrate-FFAR2 signal circuitry programs the cellular identity of enteroendocrine L-cells. Commun Biol 9, 606 (2026). https://doi.org/10.1038/s42003-026-09830-5
Trefwoorden: butyraat, entero-endocriene L‑cellen, peptide YY, darmmicrobioom, FFAR2‑signalering