Clear Sky Science · ar
دائرة إشارة مختارة وقابلة للتعزيز للبيوتيرات-FFAR2 تُبرمج هوية خلايا L المعوية الإفرازية
كيف يتواصل ألياف الأمعاء مع هرمونات الجوع
لماذا يساعد النظام الغذائي الغني بالألياف الناس على الشعور بالشبع وتجنّب زيادة الوزن؟ يتناول هذا البحث السؤال عبر التركيز على مجموعة خاصة من خلايا الأمعاء التي تفرز هرمونات تتحكم في الشهية. يوضح الباحثون كيف يمكن لجزيء يتكوّن عندما تهضم ميكروبات الأمعاء الألياف أن يعيد برمجة هذه الخلايا لتفضيل ببتيد YY (PYY)، وهو هرمون يكبح الشهية، ويقترحون طرقًا يمكن من خلالها تضخيم هذا المسار الطبيعي لعلاجات محتملة للسمنة في المستقبل.
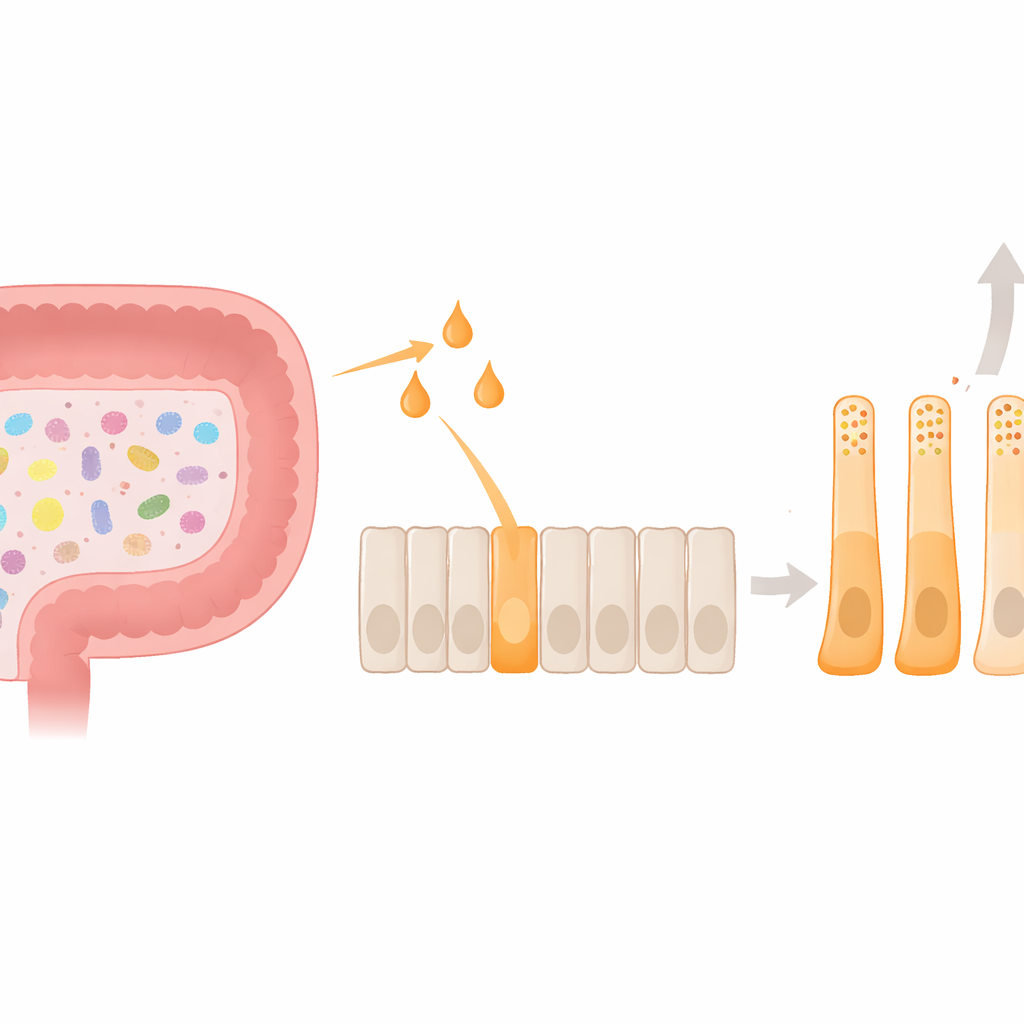
لاعب رئيسي في دائرة الجوع المعوية
في عمق بطانة القولون توجد خلايا L الإفرازية المعوية، مصانع هرمونية صغيرة تُفرز الببتيد المشابه للجلوكاجون‑1 (GLP‑1) وPYY بعد تناول الطعام. ترسل هذه الهرمونات إشارات إلى الدماغ لتقليل الشهية وتساعد على موازنة مستويات السكر في الدم. يضيف الميكروبيوم المعوي طبقة إضافية إلى هذا النظام: عندما تقوم البكتيريا بتخمير الألياف الغذائية، تنتج أحماضًا دهنية قصيرة السلسلة مثل الأسيتيت والبروبونات والبيوتيرات. هذه الجزيئات الصغيرة تنشط بدورها مستقبلًا غشائيًا على خلايا L يُدعى FFAR2. حتى الآن، ركز معظم العمل على كيفية تحفيز هذه الإشارات لتفريغ هرموني قصير المدى؛ بينما كان يُعرف أقل عن كيفية تأثيرها طويل الأمد على هوية وسلوك خلايا L نفسها.
البيوتيرات توجّه الخلايا نحو هوية غنية بـ PYY
باستخدام نموذج لخلايا L البشرية، قارن الفريق كيفية تأثير الأسيتيت والبروبونات والبيوتيرات على إنتاج الهرمونات وشكل الخلية. رفعت الجزيئات الثلاثة نشاط جين PYY، لكن البيوتيرات كان له التأثير الأقوى بفارق كبير، وميزًا بصفة فريدة زيادة إفراز PYY الفعلي. في الوقت نفسه، قلّل البيوتيرات من تعبير جين سلف GLP‑1. تحت المجهر، اتخذت الخلايا المعالجة بالبيوتيرات أشكالًا ممدودة ذات استطالات طويلة، تشبه عن قرب الخلايا الغنية بـ PYY المرصودة في نسيج الإنسان القولوني. داخليًا، تحوّلت حبيبات تخزين الهرمونات: أصبحت حبيبات PYY أكثر عددًا وشكّلت حصة أكبر من إجمالي مخزون الهرمونات. معًا، تُظهر هذه التغيرات أن البيوتيرات يفعل أكثر من مجرد تحفيز دفعة هرمونية قصيرة—إنه يوجّه الخلايا نحو حالة ثابتة متحيزة تجاه PYY على مستوى الوظيفة والشكل.
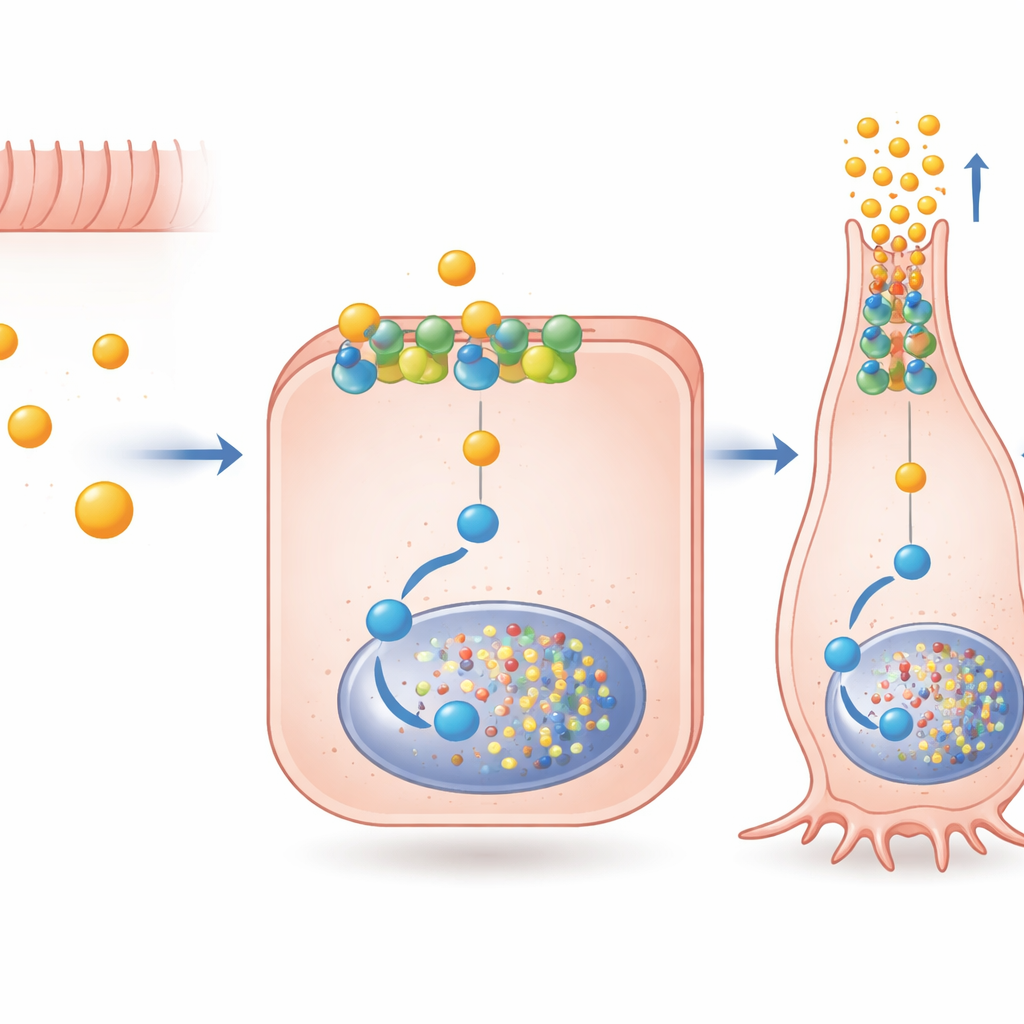
مسار إشاري متخصص داخل الخلية
سأل المؤلفون بعد ذلك كيف يرسل البيوتيرات رسالة محددة عبر FFAR2، وهو مستقبل قادر على الارتباط بأكثر من مسار إشاري داخلي. وجدوا أن الأسيتيت والبروبونات ينشطان بقوة كلا المسارين الرئيسيين لـ FFAR2، في حين يُفضّل البيوتيرات مسارًا مرتبطًا ببروتين يُدعى Gαi. عبر حجب هذا المسار بأدوية موجهة، أظهروا أن إشارة Gαi عبر FFAR2 ضرورية لجزء كبير من زيادة نشاط جين PYY ولتشغيل Pax6، وهو عامل نسخي مهم للمراحل المتأخرة من نضوج الخلايا الهرمونية. ومن المهم أن هذه الإشارة لم تعتمد على بَلع المستقبل إلى داخل الخلية؛ إذ يمكن أن تعمل مباشرة من الغشاء الخارجي. جزيء تجريبي، AZ‑1729، الذي يعزّز انتقائيًا إشارة FFAR2‑Gαi، ضاعف أكثر آثار البيوتيرات على PYY وPax6، مما يوحي بأن «معزّزات» دوائية يمكن أن تضبط هذه الدائرة الطبيعية بدقة.
توجيه الخلايا الجذعية نحو خلايا معوية إفرازية
لمعرفة ما إذا كان البيوتيرات يؤثر أيضًا على كيفية تكوّن خلايا جديدة مفرزة للهرمونات، تحوّل الباحثون إلى عضويات قولونية فأرية—أمعاء مصغّرة مُنموة من خلايا جذعية. في هذا النظام، يتحكم مسار Notch بشكل كبير في مصير الخلايا، إذ يميل إلى إبقائها في حالة تكاثر أو حالة تركز على الامتصاص ويمنعها من أن تصبح خلايا إفرازية مثل خلايا L. باستخدام آداة تقرير فلورية لمسار Notch، أظهر الفريق أن البيوتيرات قلّل نشاط Notch عبر أنواع العضويات ونقاط زمنية مختلفة، كما أكّدت تحليلات التعبير الجيني قمع البرامج المرتبطة بـ Notch. ولاحظوا أيضًا زيادة في الخلايا النادرة الموجبة لـ PYY داخل هذه العضويات. في خط خلايا L البشري، زاد البيوتيرات انتقائيًا من العلامات المتعلقة بالنضج الغدي المتأخر، وخاصة NeuroD1 وPax6، مما يؤكد دوره في دفع الخلايا نحو هوية ناضجة بالكامل تُنتج PYY.
من مستقلب ميكروبي إلى علاجات مستقبلية
يقدّم هذا العمل صورة متماسكة: فالبيوتيرات، المنتج الشائع لتخمير الألياف في القولون، يمكنه إعادة برمجة خلايا L الناضجة والتأثير في مسار تطورها ليُفضّل خلايا ممدودة غنية بـ PYY تكون مستعدة للتواصل مع الجهاز العصبي وكبح الشهية. تعتمد هذه الإشارة بدرجة كبيرة على دائرة FFAR2–Gαi المنشَّطة بالبيوتيرات على سطح الخلية، ويمكن تقويتها أكثر بواسطة جزيء مصمّم يميّل هذا المسار. للقراء العامين، الرسالة الأساسية هي أن ما تفعله ميكروبات أمعائنا بالألياف لا يقتصر على إثارة دفعات هرمونية قصيرة الأمد—بل يمكنه إعادة تشكيل التركيب نفسه لخلايا استشعار الشهية في الأمعاء، مما يقدّم استراتيجيات جديدة لاستغلال النظام الغذائي والأدوية الموجهة لدعم الشبع والصحة الأيضية.
الاستشهاد: Hirdaramani, A., Cheng, CW., Hanyaloglu, A.C. et al. A selective and augmentable butyrate-FFAR2 signal circuitry programs the cellular identity of enteroendocrine L-cells. Commun Biol 9, 606 (2026). https://doi.org/10.1038/s42003-026-09830-5
الكلمات المفتاحية: بيوتيرات, خلايا L المعوية الإفرازية, ببتيد YY, الميكروبيوم المعوي, إشارة FFAR2