Clear Sky Science · it
Un circuito segnale FFAR2 selettivo e potenziabile dal butirrato programma l’identità cellulare delle cellule enteroendocrine L
Come la fibra intestinale dialoga con gli ormoni della fame
Perché una dieta ricca di fibre aiuta le persone a sentirsi sazie ed evitare l’aumento di peso? Questo studio affronta la domanda concentrandosi su un gruppo speciale di cellule intestinali che rilasciano ormoni che controllano l’appetito. I ricercatori mostrano come una molecola prodotta dalla fermentazione delle fibre da parte del microbiota possa riprogrammare queste cellule per favorire il peptide YY (PYY), un ormone che riduce la fame, e suggeriscono modi per amplificare questo percorso naturale in vista di possibili terapie per l’obesità.
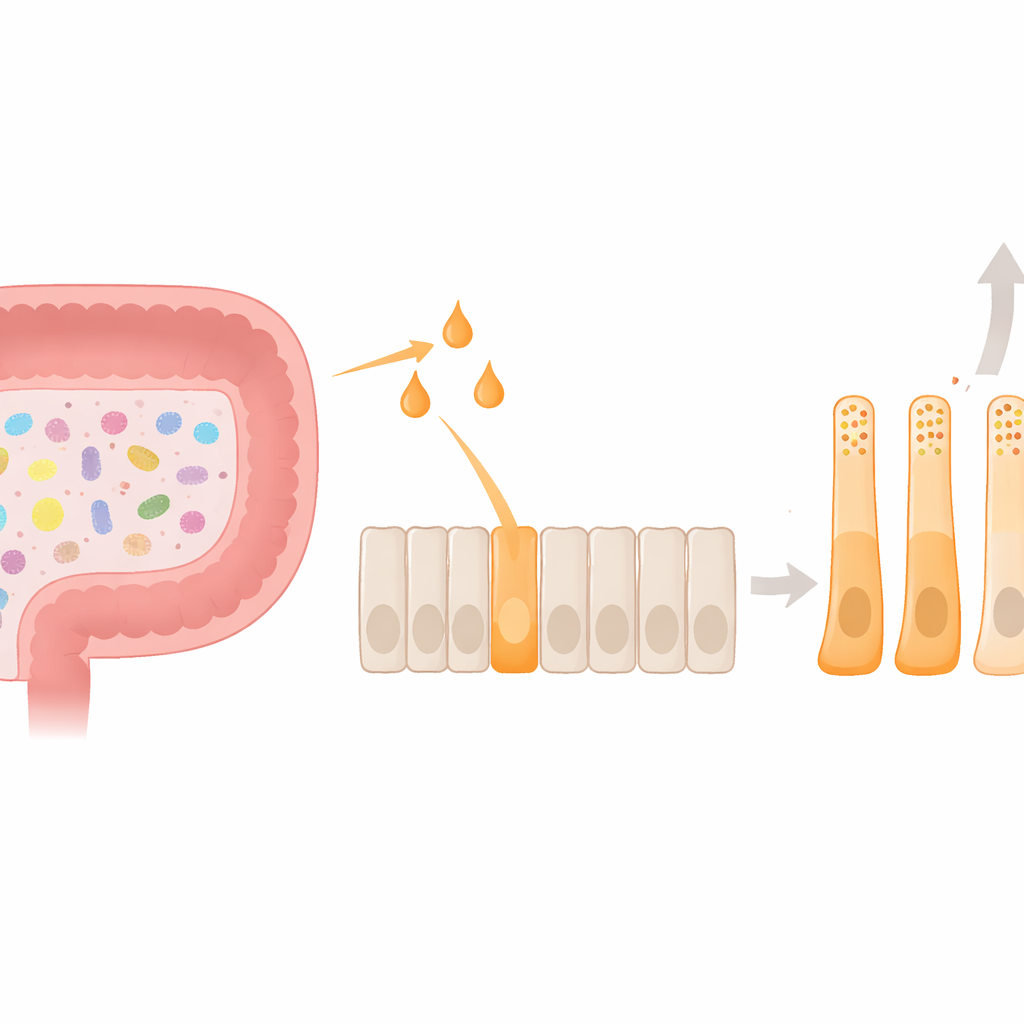
Un attore chiave nel circuito della fame dell’intestino
Profondamente nella mucosa del colon risiedono le cellule enteroendocrine L, minuscole fabbriche di ormoni che rilasciano il peptide‑like glucagone‑1 (GLP‑1) e il PYY dopo i pasti. Questi ormoni inviano segnali al cervello per ridurre l’appetito e aiutano a regolare la glicemia. Il microbioma intestinale aggiunge un ulteriore livello a questo sistema: quando i batteri fermentano le fibre dietetiche, producono acidi grassi a catena corta come acetato, propionato e butirrato. Queste piccole molecole, a loro volta, attivano un recettore di membrana sulle L‑cell chiamato FFAR2. Fino ad ora, la maggior parte degli studi si era concentrata su come questa segnalazione induca rilasci ormonali rapidi; si sapeva molto meno su come possa plasmare in modo duraturo l’identità e il comportamento delle stesse L‑cell.
Il butirrato indirizza le cellule verso un’identità ricca di PYY
Usando un modello umano di L‑cell, il gruppo ha confrontato l’effetto di acetato, propionato e butirrato sulla produzione ormonale e sulla morfologia cellulare. Tutti e tre gli acidi aumentavano l’attività genica del PYY, ma il butirrato mostrava di gran lunga l’effetto più marcato e aumentava in modo unico la secrezione effettiva di PYY. Allo stesso tempo, il butirrato riduceva l’espressione del gene precursore del GLP‑1. Al microscopio, le cellule trattate con butirrato si allungavano e sviluppavano lunghi processi, somigliando da vicino alle cellule ricche di PYY osservate nel tessuto colico umano. All’interno, i loro granuli di stoccaggio ormonale cambiarono: i granuli contenenti PYY divennero più numerosi e rappresentarono una quota maggiore del totale ormonale. Messo insieme, questi cambiamenti indicano che il butirrato fa più che scatenare un rilascio ormonale rapido: orienta le cellule verso uno stato stabile, funzionalmente e morfologicamente, sbilanciato a favore del PYY.
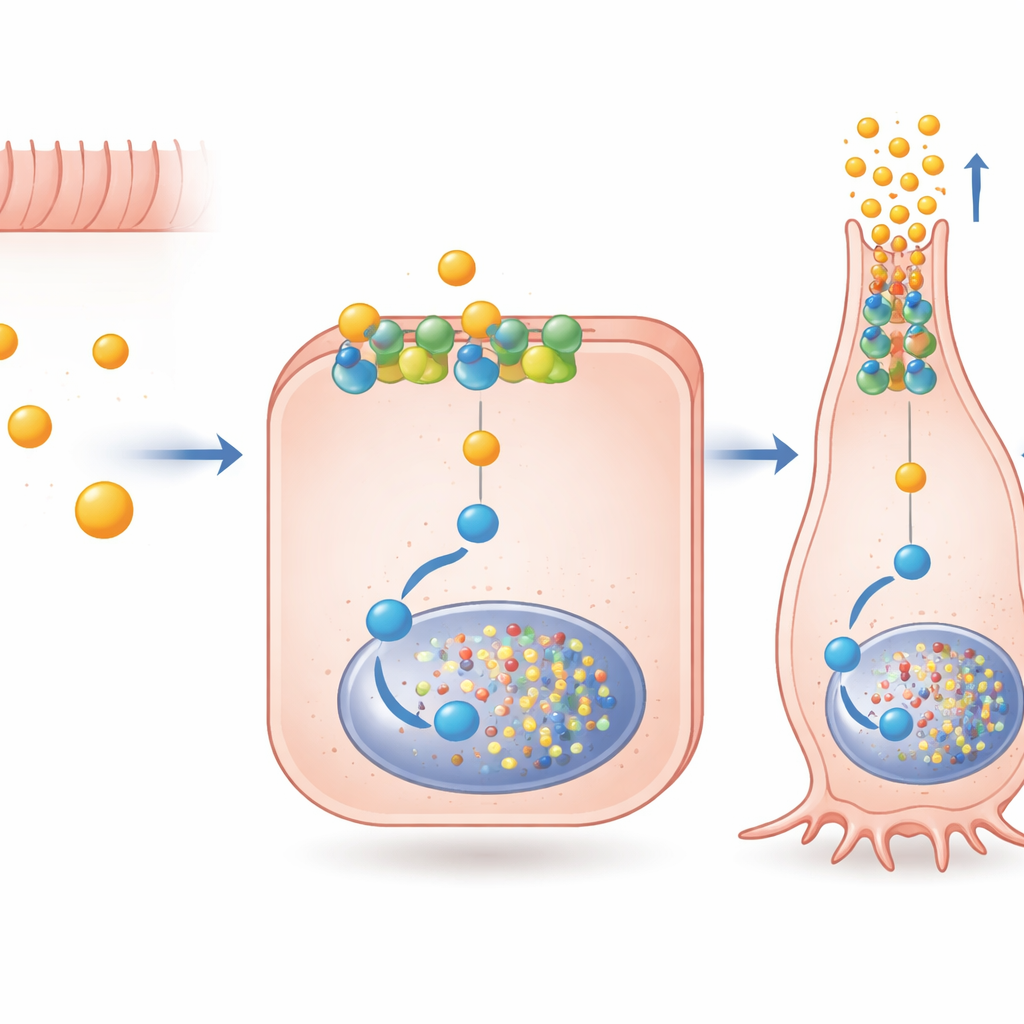
Un percorso di segnalazione specializzato all’interno della cellula
Gli autori hanno quindi indagato come il butirrato invii un messaggio così specifico attraverso FFAR2, un recettore in grado di collegarsi a più vie di segnalazione interne. Hanno scoperto che acetato e propionato attivano robustamente entrambe le principali vie di FFAR2, mentre il butirrato preferisce una via collegata a una proteina chiamata Gαi. Bloccando questa via con farmaci mirati, hanno dimostrato che la segnalazione Gαi tramite FFAR2 è necessaria per gran parte dell’aumento dell’attività genetica del PYY indotto dal butirrato e per l’attivazione di Pax6, un fattore di trascrizione importante per le fasi avanzate della maturazione delle cellule endocrine. È importante notare che questa segnalazione non dipendeva dall’internalizzazione del recettore; poteva avvenire direttamente dalla membrana plasmatica esterna. Una molecola sperimentale, AZ‑1729, che potenzia selettivamente la segnalazione FFAR2–Gαi, amplificava ulteriormente gli effetti del butirrato su PYY e Pax6, suggerendo che “potenziatori” farmacologici potrebbero modulare finemente questo circuito naturale.
Indirizzare le cellule staminali verso cellule secretorie intestinali
Per verificare se il butirrato influenzi anche la generazione di nuove cellule secernenti ormoni, i ricercatori hanno utilizzato organoidi colici murini — mini‑intesti coltivati a partire da cellule staminali. In questo sistema il destino cellulare è fortemente controllato dalla via Notch, che tende a mantenere le cellule in uno stato proliferativo o orientato all’assorbimento e ne impedisce la differenziazione in cellule secretorie come le L‑cell. Utilizzando un reporter fluorescente di Notch, il gruppo ha dimostrato che il butirrato attenuava l’attività di Notch in diversi tipi di organoidi e in vari momenti, e il profilo di espressione genica ha confermato la soppressione dei programmi legati a Notch. Hanno anche osservato un aumento di rare cellule PYY‑positive all’interno di questi organoidi. Nella linea cellulare umana di L‑cell, il butirrato aumentava selettivamente i marcatori della maturazione endocrina tardiva, in particolare NeuroD1 e Pax6, sottolineando il suo ruolo nel spingere le cellule verso un’identità completamente sviluppata e produttrice di PYY.
Dal metabolita microbico alle terapie future
Questo lavoro disegna un quadro coerente: il butirrato, prodotto comune della fermentazione delle fibre nel colon, può sia rimodellare le L‑cell mature sia influenzare il loro percorso di sviluppo per favorire cellule allungate e ricche di PYY, pronte a comunicare con il sistema nervoso e a ridurre l’appetito. La segnalazione si basa in gran parte su un circuito FFAR2–Gαi attivato dal butirrato sulla superficie cellulare e può essere ulteriormente rafforzata da una molecola progettata che sbilancia la via. Per il lettore non specialistico, il messaggio chiave è che ciò che i nostri microbi fanno con le fibre non si limita a scatenare rilasci ormonali di breve durata: può rimodellare la composizione stessa delle cellule intestinali che rilevano l’appetito, suggerendo nuove strategie per sfruttare dieta e farmaci mirati a favore della sazietà e della salute metabolica.
Citazione: Hirdaramani, A., Cheng, CW., Hanyaloglu, A.C. et al. A selective and augmentable butyrate-FFAR2 signal circuitry programs the cellular identity of enteroendocrine L-cells. Commun Biol 9, 606 (2026). https://doi.org/10.1038/s42003-026-09830-5
Parole chiave: butirrato, cellule enteroendocrine L, peptide YY, microbioma intestinale, segnalazione FFAR2