Clear Sky Science · pl
Selektowny i wzmacnialny obwód sygnałowy butyrat–FFAR2 programuje tożsamość komórkową komórek enteroendokrynnych L
Jak włókno pokarmowe z jelita rozmawia z hormonami głodu
Dlaczego dieta bogata w błonnik pomaga poczuć sytość i uniknąć przyrostu masy ciała? Badanie przygląda się temu zagadnieniu, skupiając się na szczególnej grupie komórek jelitowych wydzielających hormony kontrolujące apetyt. Autorzy pokazują, w jaki sposób cząsteczka powstająca podczas trawienia włókna przez mikroby jelitowe może przestawić program tych komórek na produkcję peptydu YY (PYY), hormonu tłumiącego głód, i sugerują sposoby, by tę naturalną ścieżkę wzmocnić jako potencjalne leczenie otyłości.
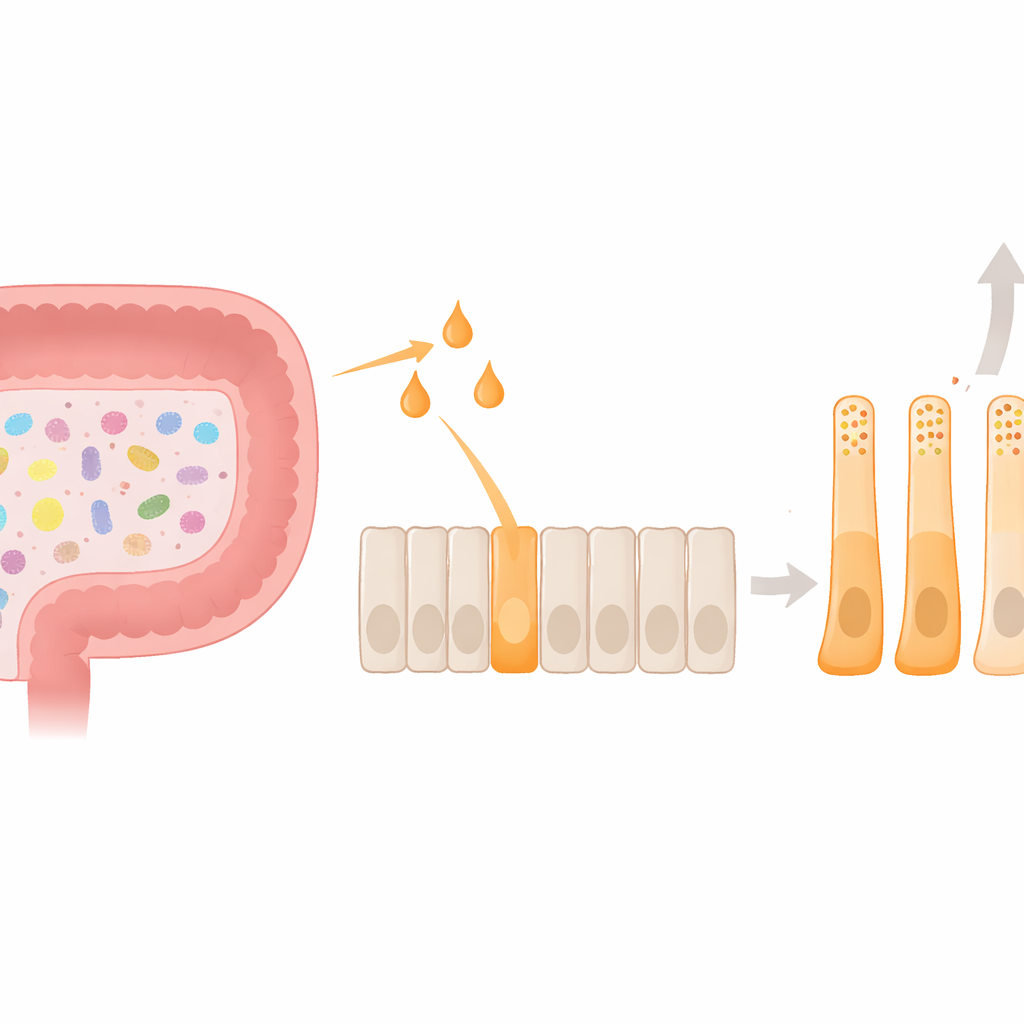
Kluczowy gracz w obwodzie głodu w jelicie
Głęboko w wyściółce jelita grubego znajdują się komórki enteroendokrynne L — maleńkie „fabryki” hormonów, które po posiłku uwalniają glukagonopodobny peptyd‑1 (GLP‑1) i PYY. Hormony te sygnalizują do mózgu, by zmniejszył apetyt, i pomagają regulować poziom cukru we krwi. Mikrobiom jelitowy dokłada kolejny poziom kontroli: gdy bakterie fermentują błonnik, powstają krótkołańcuchowe kwasy tłuszczowe, takie jak octan, propionian i butyrat. Te małe molekuły aktywują receptor powierzchniowy na komórkach L zwany FFAR2. Do tej pory większość prac skupiała się na tym, jak ta sygnalizacja wywołuje krótkotrwałe wyrzuty hormonów; znacznie mniej wiadomo o tym, jak może ona trwale kształtować tożsamość i zachowanie samych komórek L.
Butyrat przesuwa komórki w stronę tożsamości bogatej w PYY
Wykorzystując ludzki model komórek L, zespół porównał wpływ octanu, propionianu i butyratu na produkcję hormonów i morfologię komórek. Wszystkie trzy związki zwiększały aktywność genu PYY, ale najsilniejszy efekt miała przewyraźnie butyrat, który jednocześnie jako jedyny zwiększał rzeczywiste wydzielanie PYY. Równocześnie butyrat zmniejszał ekspresję genu prekursorowego GLP‑1. Pod mikroskopem komórki traktowane butyratem wydłużały się i tworzyły długie wypustki, bardzo przypominając komórki bogate w PYY obserwowane w tkance jelita ludzkiego. Wewnątrz zmienił się rozkład ziarnistości z hormonami: ziarnistości zawierające PYY stały się liczniejsze i stanowiły większy udział w całkowitym zasobie hormonów. Razem te zmiany pokazują, że butyrat robi coś więcej niż wywołuje krótkotrwały wyrzut hormonów — kieruje komórki ku trwałemu, funkcjonalnemu i morfologicznemu stanowi z przewagą PYY.
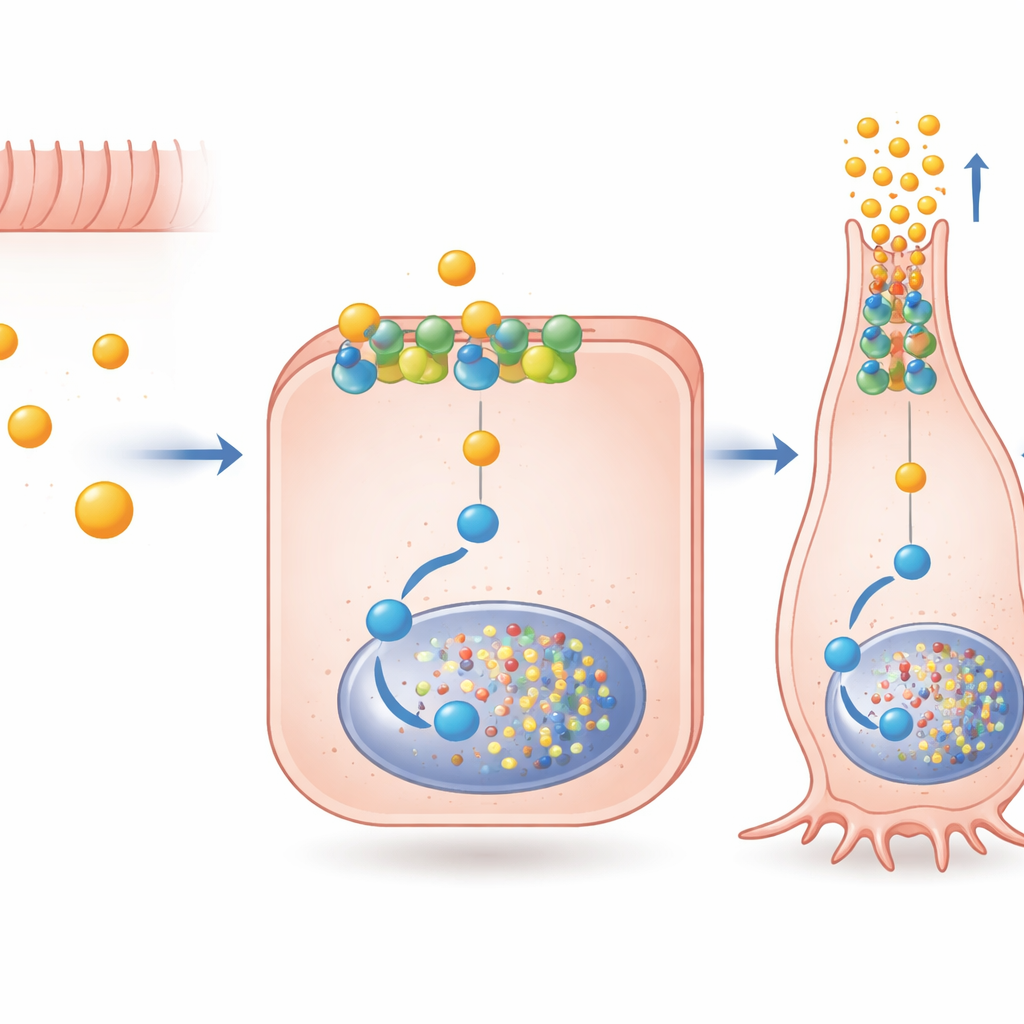
Specjalizowana ścieżka sygnałowa wewnątrz komórki
Autorzy pytali następnie, jak butyrat przekazuje tak precyzyjny komunikat przez FFAR2, receptor mogący łączyć się z więcej niż jedną wewnętrzną drogą sygnałową. Stwierdzili, że octan i propionian silnie aktywują obie główne ścieżki FFAR2, podczas gdy butyrat preferuje tę związaną z białkiem Gαi. Blokując tę drogę za pomocą ukierunkowanych leków, wykazali, że sygnalizacja Gαi przez FFAR2 jest wymagana dla dużej części wzrostu aktywności genu PYY wywołanego przez butyrat oraz dla włączenia Pax6 — czynnika transkrypcyjnego ważnego w późnych etapach dojrzewania komórek hormonalnych. Co istotne, ta sygnalizacja nie zależała od internalizacji receptora; mogła działać bezpośrednio z błony komórkowej. Molekuła eksperymentalna AZ‑1729, selektywnie wzmacniająca sygnalizację FFAR2–Gαi, dodatkowo potęgowała efekty butyratu na PYY i Pax6, sugerując, że farmakologiczne „wzmacniacze” mogłyby precyzyjnie modulować ten naturalny obwód.
Kierowanie komórek macierzystych ku komórkom wydzielniczym jelita
Aby sprawdzić, czy butyrat wpływa także na powstawanie nowych komórek wydzielających hormony, badacze sięgnęli po organoidy okrężnicy myszy — mini‑jelita hodowane ze komórek macierzystych. W tym systemie los komórkowy jest silnie kontrolowany przez szlak Notch, który ma skłonność do utrzymywania komórek w stanie proliferacyjnym lub ukierunkowanym na wchłanianie i blokuje przejście w kierunku komórek wydzielniczych, takich jak komórki L. Korzystając z fluorescencyjnego raportera aktywności Notch, zespół pokazał, że butyrat osłabiał aktywność Notch w różnych typach organoidów i w różnych punktach czasowych, a profilowanie ekspresji genów potwierdziło zahamowanie programów związanych z Notch. Zaobserwowano też wzrost rzadkich komórek pozytywnych w kierunku PYY w tych organoidach. W ludzkiej linii komórek L butyrat selektywnie zwiększał markery późnego dojrzewania endokrynnego, szczególnie NeuroD1 i Pax6, podkreślając jego rolę w popychaniu komórek ku w pełni rozwiniętej, produkującej PYY tożsamości.
Od metabolitu mikrobiologicznego do przyszłych terapii
Ta praca kreśli spójny obraz: butyrat, powszechny produkt fermentacji włókna w okrężnicy, może zarówno przeprogramować dojrzałe komórki L, jak i wpływać na ich drogę rozwojową, skłaniając je ku wydłużonym komórkom bogatym w PYY, przygotowanym do komunikacji z układem nerwowym i hamowania apetytu. Sygnał opiera się w dużej mierze na aktywowanym przez butyrat obwodzie FFAR2–Gαi na powierzchni komórki i można go dodatkowo wzmocnić za pomocą zaprojektowanej molekuły, która faworyzuje tę ścieżkę. Dla czytelnika nieprofesjonalnego kluczowy wniosek jest taki, że to, co mikroby jelitowe robią z błonnikiem, nie tylko wywołuje krótkotrwałe wyrzuty hormonów — może przekształcać sam skład i charakter komórek czujnych na apetyt w jelicie, co otwiera nowe strategie wykorzystania diety i ukierunkowanych leków do wspierania sytości i zdrowia metabolicznego.
Cytowanie: Hirdaramani, A., Cheng, CW., Hanyaloglu, A.C. et al. A selective and augmentable butyrate-FFAR2 signal circuitry programs the cellular identity of enteroendocrine L-cells. Commun Biol 9, 606 (2026). https://doi.org/10.1038/s42003-026-09830-5
Słowa kluczowe: butyrat, komórki enteroendokrynne L, peptyd YY, mikrobiom jelitowy, sygnalizacja FFAR2