Clear Sky Science · pt
Uma via de sinalização seletiva e aumentável butirato‑FFAR2 programa a identidade celular das células enteroendócrinas L
Como a fibra intestinal conversa com os hormônios da fome
Por que uma dieta rica em fibras ajuda as pessoas a se sentirem saciadas e a evitar ganho de peso? Este estudo investiga essa questão ao focar em um grupo especial de células intestinais que liberam hormônios que controlam o apetite. Os pesquisadores mostram como uma molécula produzida quando nossos microrganismos intestinais digerem a fibra pode reprogramar essas células para favorecer o peptídeo YY (PYY), um hormônio que reduz a fome, e sugerem maneiras de ampliar essa via natural para potenciais tratamentos futuros da obesidade.
Um ator-chave no circuito da fome do intestino
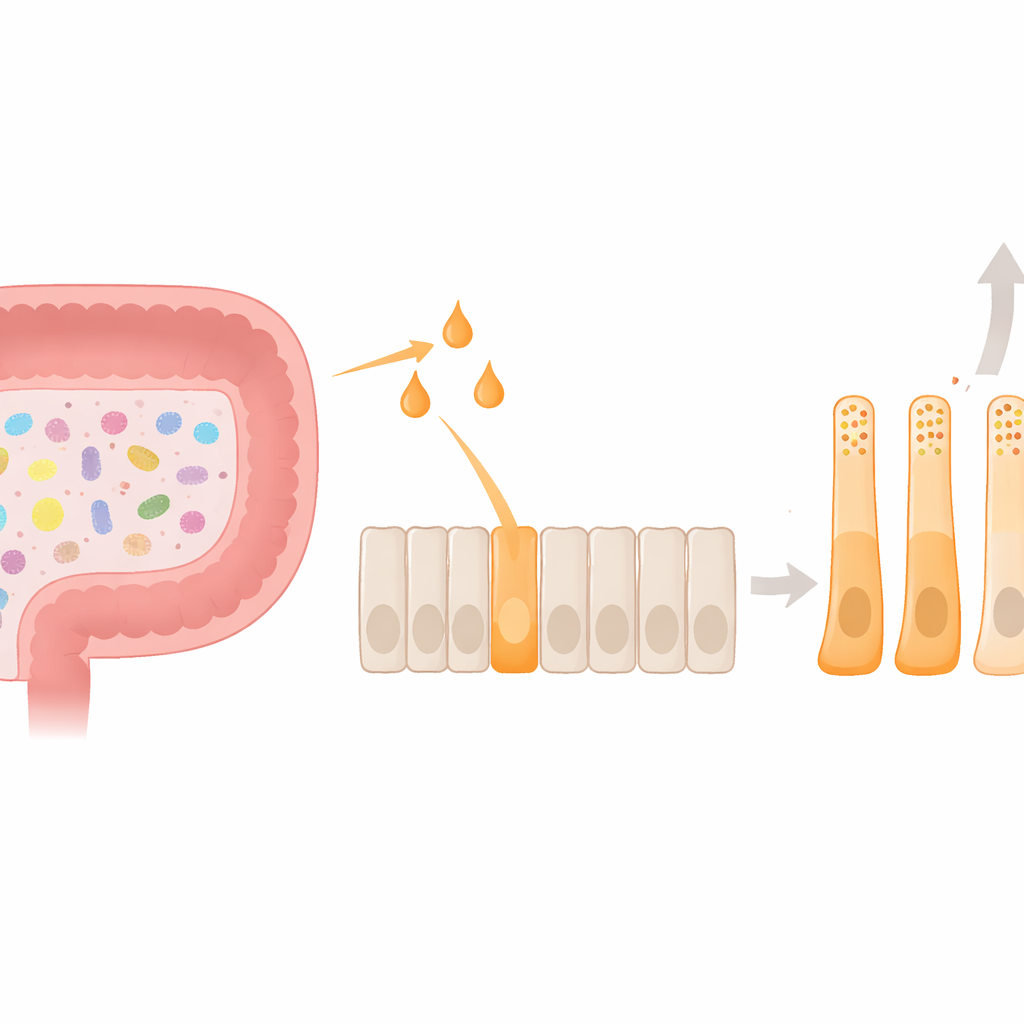
Nas camadas do cólon vivem as células enteroendócrinas L, pequenas fábricas hormonais que liberam o peptídeo‑1 semelhante ao glucagon (GLP‑1) e o PYY após comermos. Esses hormônios sinalizam ao cérebro para reduzir o apetite e ajudam a equilibrar a glicemia. O microbioma intestinal adiciona uma camada extra a esse sistema: quando as bactérias fermentam a fibra dietética, produzem ácidos graxos de cadeia curta, como acetato, propionato e butirato. Essas pequenas moléculas, por sua vez, ativam um receptor de superfície nas células L chamado FFAR2. Até agora, a maior parte do trabalho concentrou‑se em como essa sinalização desencadeia liberações rápidas de hormônio; sabia‑se muito menos sobre como ela poderia moldar de forma duradoura a identidade e o comportamento das próprias células L.
O butirato inclina as células para uma identidade rica em PYY
Usando um modelo humano de célula L, a equipe comparou como acetato, propionato e butirato afetam a produção de hormônios e a morfologia celular. As três moléculas aumentaram a atividade do gene PYY, mas o butirato teve de longe o efeito mais forte e foi o único a aumentar de forma consistente a secreção real de PYY. Ao mesmo tempo, o butirato reduziu a expressão do gene precursor do GLP‑1. Ao microscópio, as células tratadas com butirato alongaram‑se, formando processos longos que lembram de perto as células ricas em PYY observadas em tecido cólon humano. Internamente, seus grânulos de armazenamento hormonal mudaram: os grânulos de PYY tornaram‑se mais numerosos e passaram a representar uma fração maior do pool total de hormônios. Juntas, essas mudanças mostram que o butirato faz mais do que desencadear um pico hormonal rápido — ele direciona as células para um estado estável e enviesado para PYY, em função e forma.
Uma via de sinalização especializada dentro da célula
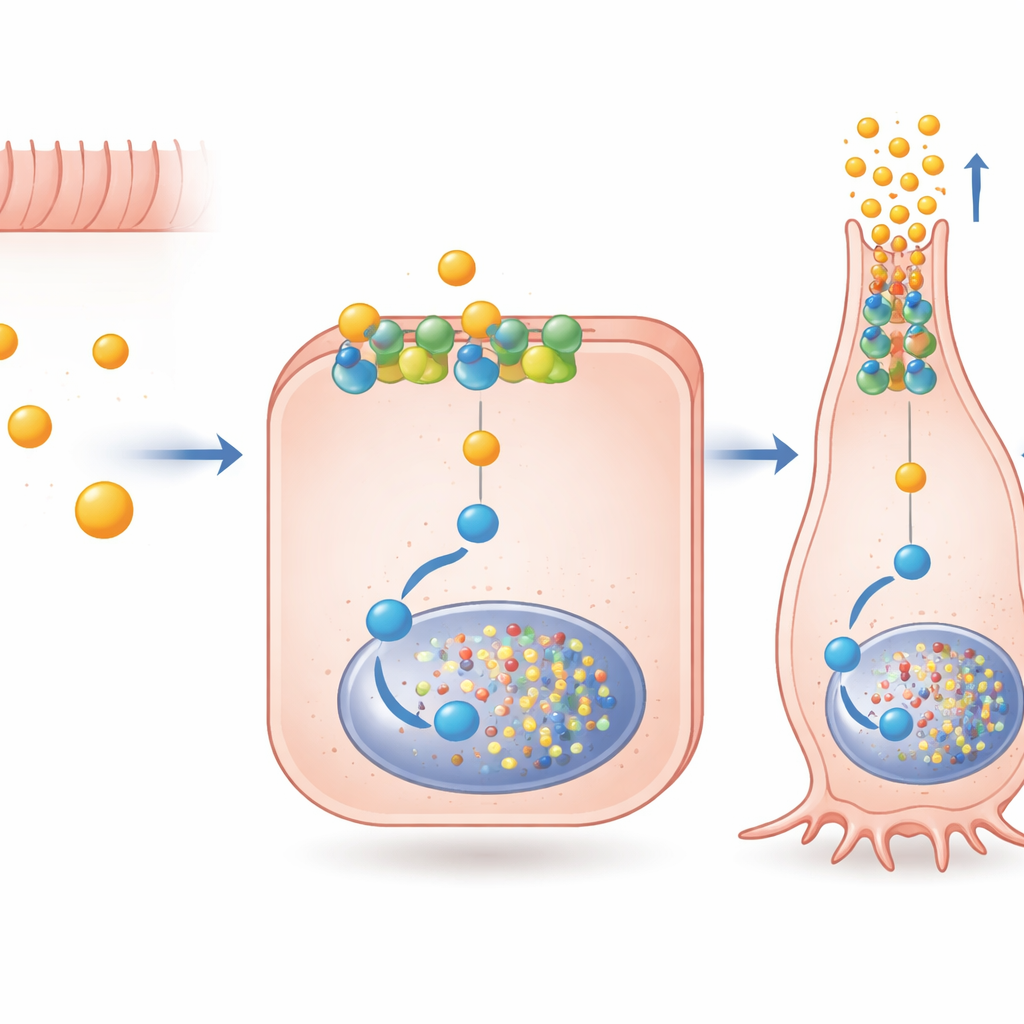
Os autores então investigaram como o butirato envia uma mensagem tão específica por meio do FFAR2, um receptor que pode se conectar a mais de uma via interna de sinalização. Eles descobriram que acetato e propionato ativam fortemente ambas as principais vias do FFAR2, enquanto o butirato prefere uma associada a uma proteína chamada Gαi. Ao bloquear essa via com fármacos direcionados, mostraram que a sinalização via Gαi através do FFAR2 é necessária para grande parte do aumento da atividade do gene PYY induzido pelo butirato e para a ativação de Pax6, um fator de transcrição importante para estágios tardios da maturação das células produtoras de hormônio. Importante, essa sinalização não dependia do receptor ser internalizado; ela podia atuar diretamente da membrana externa. Uma molécula experimental, AZ‑1729, que melhora seletivamente a sinalização FFAR2–Gαi, amplificou ainda mais os efeitos do butirato sobre PYY e Pax6, sugerindo que “potenciadores” farmacológicos poderiam ajustar finamente esse circuito natural.
Guiando células-tronco rumo a células secretoras intestinais
Para ver se o butirato também influencia como novas células secretoras de hormônio são geradas, os pesquisadores utilizaram organoides colônicos de camundongo — mini‑intestinos cultivados a partir de células‑tronco. Nesse sistema, o destino celular é fortemente controlado pela via Notch, que tende a manter as células em um estado proliferação ou voltado à absorção e impede que se tornem células secretoras como as L‑cells. Usando um repórter fluorescent de Notch, a equipe mostrou que o butirato reduziu a atividade de Notch em diferentes tipos de organoides e momentos, e o perfil de expressão gênica confirmou que programas relacionados a Notch foram suprimidos. Eles também observaram um aumento em células raras positivas para PYY dentro desses organoides. Na linhagem humana de células L, o butirato aumentou seletivamente marcadores de maturação endócrina tardia, especialmente NeuroD1 e Pax6, ressaltando seu papel em empurrar as células rumo a uma identidade totalmente desenvolvida e produtora de PYY.
Do metabólito microbiano a terapias futuras
Este trabalho desenha um quadro coerente: o butirato, um produto comum da fermentação de fibras no cólon, pode tanto redesenhar células L maduras quanto influenciar sua via de desenvolvimento para favorecer células alongadas ricas em PYY, prontas para comunicar‑se com o sistema nervoso e reduzir o apetite. A sinalização depende fortemente de um circuito FFAR2–Gαi ativado pelo butirato na superfície celular e pode ser reforçada por uma molécula projetada que polariza essa via. Para leitores leigos, a mensagem principal é que o que nossos micróbios intestinais fazem com a fibra não apenas dispara rajadas hormonais de curta duração — pode remodelar a própria composição das células sensoriais de apetite do intestino, sugerindo novas estratégias para aproveitar dieta e fármacos direcionados para favorecer saciedade e saúde metabólica.
Citação: Hirdaramani, A., Cheng, CW., Hanyaloglu, A.C. et al. A selective and augmentable butyrate-FFAR2 signal circuitry programs the cellular identity of enteroendocrine L-cells. Commun Biol 9, 606 (2026). https://doi.org/10.1038/s42003-026-09830-5
Palavras-chave: butirato, células enteroendócrinas L, peptídeo YY, microbioma intestinal, sinalização FFAR2