Clear Sky Science · de
Ein selektiver und verstärkbarer Butyrat‑FFAR2‑Signalweg programmiert die zelluläre Identität enteroendokriner L‑Zellen
Wie Darmfaser mit Hungershormonen spricht
Warum hilft eine ballaststoffreiche Ernährung Menschen, sich satt zu fühlen und einer Gewichtszunahme vorzubeugen? Diese Studie geht dieser Frage nach, indem sie eine spezielle Gruppe von Darmzellen ins Visier nimmt, die appetitregelnde Hormone freisetzen. Die Forschenden zeigen, wie ein Molekül, das entsteht, wenn Darmmikroben Ballaststoffe abbauen, diese Zellen so umprogrammiert, dass sie vermehrt Peptid YY (PYY) produzieren — ein Hormon, das den Hunger dämpft — und skizzieren Wege, wie dieser natürliche Signalweg für künftige Adipositas‑Therapien verstärkt werden könnte.
Ein Schlüsselspieler im Hunger‑Circuit des Darms
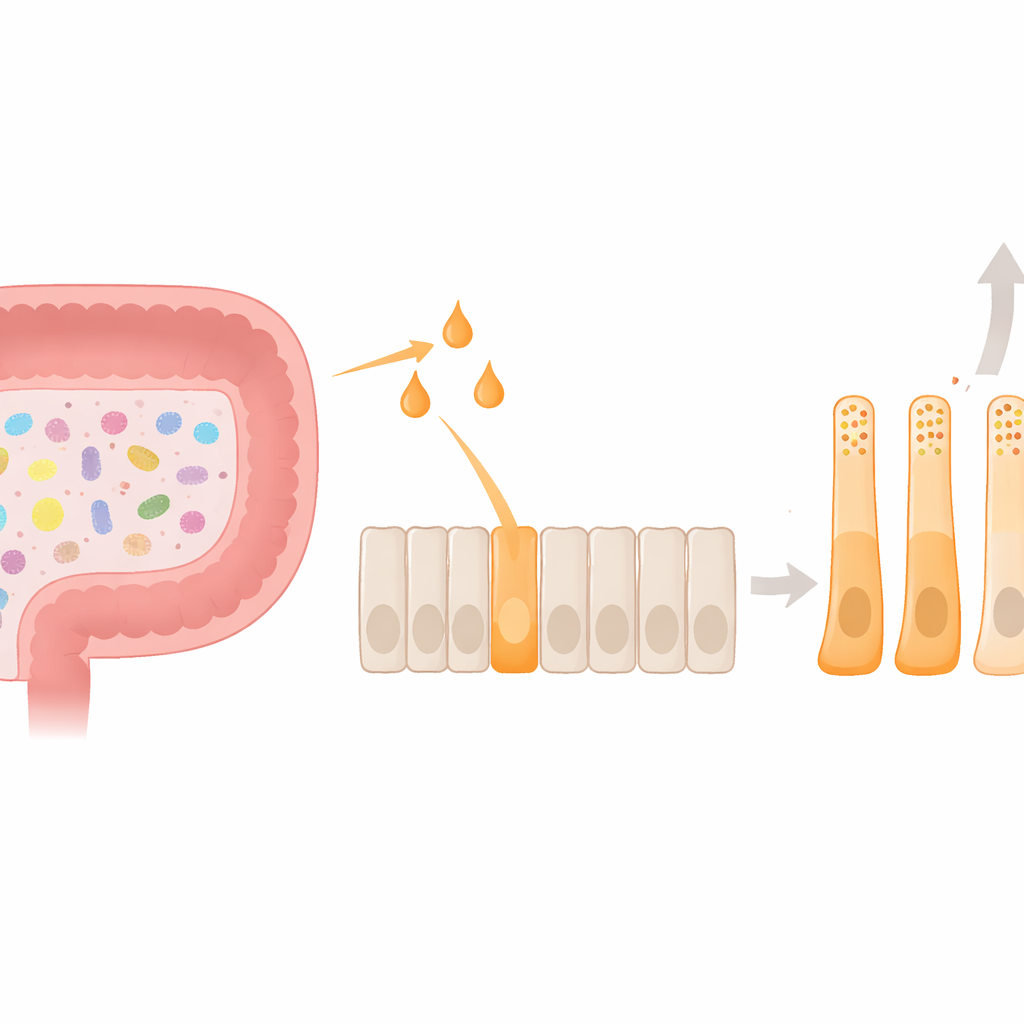
Tief in der Schleimhaut des Dickdarms liegen enteroendokrine L‑Zellen, kleine Hormonfabriken, die nach dem Essen glucagonähnliches Peptid‑1 (GLP‑1) und PYY freisetzen. Diese Hormone signalisieren dem Gehirn, den Appetit zu reduzieren, und helfen, den Blutzucker zu stabilisieren. Das Darmmikrobiom fügt diesem System eine zusätzliche Ebene hinzu: Wenn Bakterien Nahrungsfasern fermentieren, produzieren sie kurzkettige Fettsäuren wie Acetat, Propionat und Butyrat. Diese kleinen Moleküle aktivieren wiederum einen Oberflächenrezeptor auf L‑Zellen, genannt FFAR2. Bisher konzentrierte sich die Forschung größtenteils darauf, wie diese Signalgebung kurzzeitige Hormonfreisetzungen auslöst; deutlich weniger bekannt war, ob und wie sie die Identität und das Verhalten der L‑Zellen langfristig prägt.
Butyrat lenkt Zellen in eine PYY‑reiche Identität
Anhand eines menschlichen L‑Zell‑Modells verglich das Team, wie Acetat, Propionat und Butyrat die Hormonproduktion und Zellgestalt beeinflussen. Alle drei Moleküle erhöhten die PYY‑Genaktivität, doch Butyrat zeigte bei weitem den stärksten Effekt und steigerte außerdem einzigartig die tatsächliche PYY‑Sekretion. Gleichzeitig verringerte Butyrat die Expression des GLP‑1‑Vorläufergens. Unter dem Mikroskop dehnten sich butyratbehandelte Zellen zu länglichen Formen mit langen Fortsätzen aus, die den in menschlichem Kolongewebe beobachteten PYY‑reichen Zellen sehr ähneln. Im Inneren verschoben sich ihre Hormon‑Speichergranula: PYY‑Granula wurden zahlreicher und machten einen größeren Anteil des gesamten Hormonpools aus. Zusammengenommen zeigen diese Veränderungen, dass Butyrat mehr bewirkt als einen kurzen Hormonstoß — es steuert Zellen hin zu einem stabilen, funktional und strukturell auf PYY ausgerichteten Zustand.
Ein spezialisierter Signalweg innerhalb der Zelle
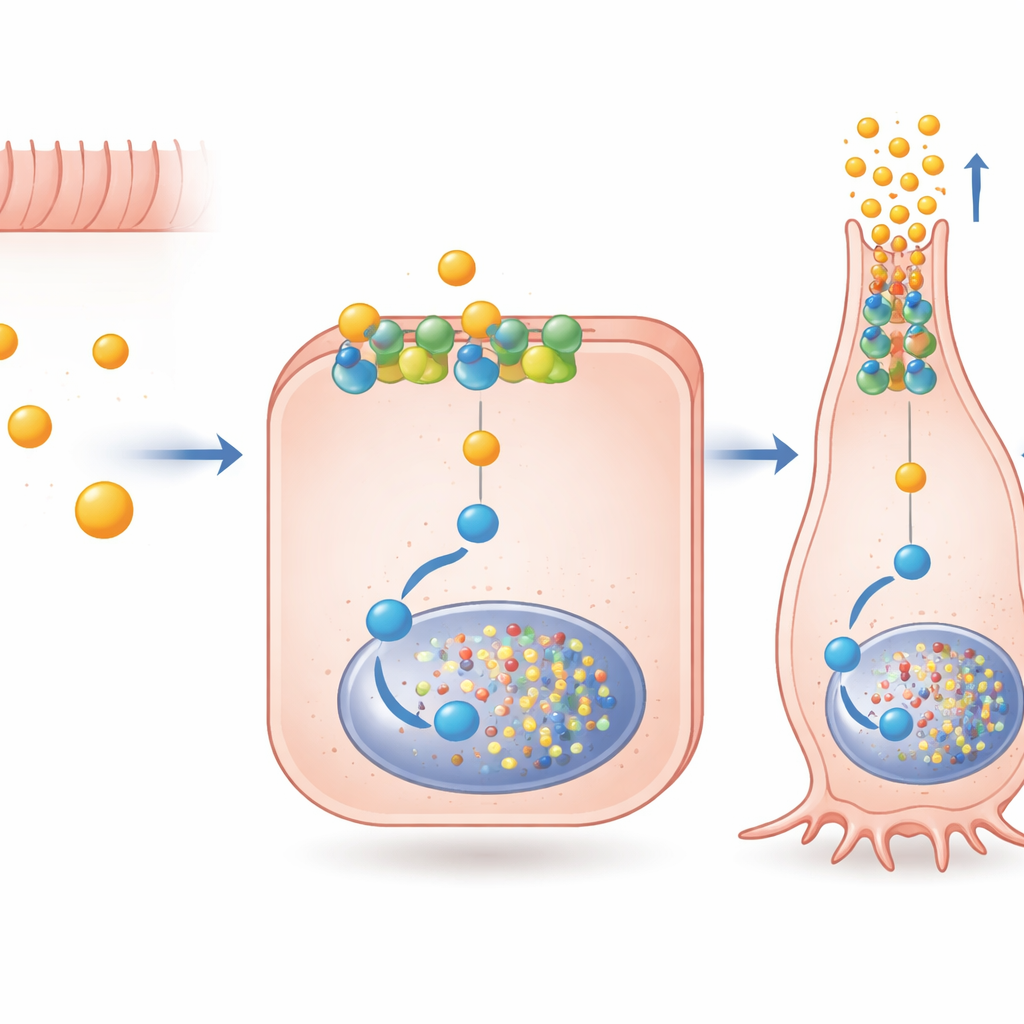
Die Autorinnen und Autoren fragten dann, wie Butyrat über FFAR2 eine so spezifische Botschaft übermittelt, da dieser Rezeptor an mehr als einen intrazellulären Signalweg koppeln kann. Sie fanden heraus, dass Acetat und Propionat beide großen FFAR2‑Wege stark aktivieren, während Butyrat einen Weg bevorzugt, der mit einem Protein namens Gαi verknüpft ist. Durch Blockade dieses Weges mit gezielten Wirkstoffen zeigten sie, dass Gαi‑Signalgebung über FFAR2 für einen Großteil der butyratbedingten Steigerung der PYY‑Genaktivität und für die Aktivierung von Pax6 — einem Transkriptionsfaktor, der für späte Stadien der Hormonzellreifung wichtig ist — erforderlich ist. Wichtig ist, dass diese Signalgebung nicht davon abhing, dass der Rezeptor in die Zelle eingeschleust wird; sie konnte direkt von der Außenseite der Membran aus wirken. Ein experimentelles Molekül, AZ‑1729, das selektiv die FFAR2‑Gαi‑Signalgebung verstärkt, verstärkte zudem die Effekte von Butyrat auf PYY und Pax6, was darauf hindeutet, dass pharmakologische „Booster“ diesen natürlichen Kreislauf feinjustieren könnten.
Stammzellen in Richtung sekretorischer Darmzellen lenken
Um zu prüfen, ob Butyrat auch die Entstehung neuer hormonfreisetzender Zellen beeinflusst, arbeiteten die Forschenden mit kolischen Organoiden aus Maus‑Stammzellen — Mini‑Därmen im Labor. In diesem System wird das Zellschicksal stark vom Notch‑Signalweg gesteuert, der Zellen tendenziell in einem proliferierenden oder auf Resorption ausgerichteten Zustand hält und sie daran hindert, sekretorische Zellen wie L‑Zellen zu werden. Mit einem fluoreszenten Notch‑Reporter zeigte das Team, dass Butyrat die Notch‑Aktivität über verschiedene Organoidtypen und Zeitpunkte hinweg dämpfte, und die Genexpressionsanalyse bestätigte, dass Notch‑verwandte Programme unterdrückt wurden. Außerdem stieg die Anzahl seltener PYY‑positiver Zellen in diesen Organoiden an. In der menschlichen L‑Zell‑Linie erhöhte Butyrat selektiv Marker für späte endokrine Reifung, insbesondere NeuroD1 und Pax6, was seine Rolle unterstreicht, Zellen zu einer voll entwickelten, PYY‑produzierenden Identität zu treiben.
Vom mikrobiellen Metaboliten zu zukünftigen Therapien
Diese Arbeit zeichnet ein stimmiges Bild: Butyrat, ein häufiges Produkt der Ballaststofffermentation im Kolon, kann sowohl ausgereifte L‑Zellen umprogrammieren als auch ihren Entwicklungsweg beeinflussen, sodass PYY‑reiche, längliche Zellen entstehen, die bereit sind, mit dem Nervensystem zu kommunizieren und den Appetit zu dämpfen. Die Signalübertragung beruht stark auf einem butyrataktivierten FFAR2–Gαi‑Kreislauf an der Zelloberfläche und kann durch ein Designer‑Molekül, das diesen Weg bevorzugt, weiter verstärkt werden. Für ein allgemeines Publikum lautet die Kernbotschaft: Was unsere Darmmikroben aus Ballaststoffen machen, löst nicht nur kurzlebige Hormonstöße aus — es kann die Zusammensetzung der appetitsteuernden Zellen im Darm nachhaltig verändern und legt nahe, dass sich Ernährung und gezielte Medikamente kombinieren lassen, um Sättigung und metabolische Gesundheit zu unterstützen.
Zitation: Hirdaramani, A., Cheng, CW., Hanyaloglu, A.C. et al. A selective and augmentable butyrate-FFAR2 signal circuitry programs the cellular identity of enteroendocrine L-cells. Commun Biol 9, 606 (2026). https://doi.org/10.1038/s42003-026-09830-5
Schlüsselwörter: Butyrat, enteroendokrine L‑Zellen, Peptid YY, Darmmikrobiom, FFAR2‑Signalgebung