Clear Sky Science · zh
鉴定抗菌肽EWAMP-R在细菌体内的靶点
为何一种来自小蠕虫的分子对应对超级细菌至关重要
随着抗生素耐药性的上升,医生可用来阻止危险细菌感染的手段日益减少。这项研究探索了一种有前景的替代方案:一种来自蚯蚓的天然小分子——抗菌肽EWAMP-R。研究人员表明,该肽不仅仅是刺破细菌膜——它还破坏了细菌生存所需的一个关键内部机器,指向了一类可能能领先于耐药性的全新治疗策略。
对细菌的双重打击
大多数抗生素通过作用于单一关键过程(如构建细胞壁)来发挥作用,细菌最终可以进化出绕过这些攻击的方法。抗菌肽则常常对细菌进行多点打击。此前已有证据显示EWAMP-R能损伤细菌膜并诱发类似于人类细胞凋亡的程序性死亡。本研究旨在弄清当EWAMP-R穿过膜进入细胞后会发生什么——具体来说,它在细胞内靶向哪个分子以及该相互作用如何导致细菌死亡。
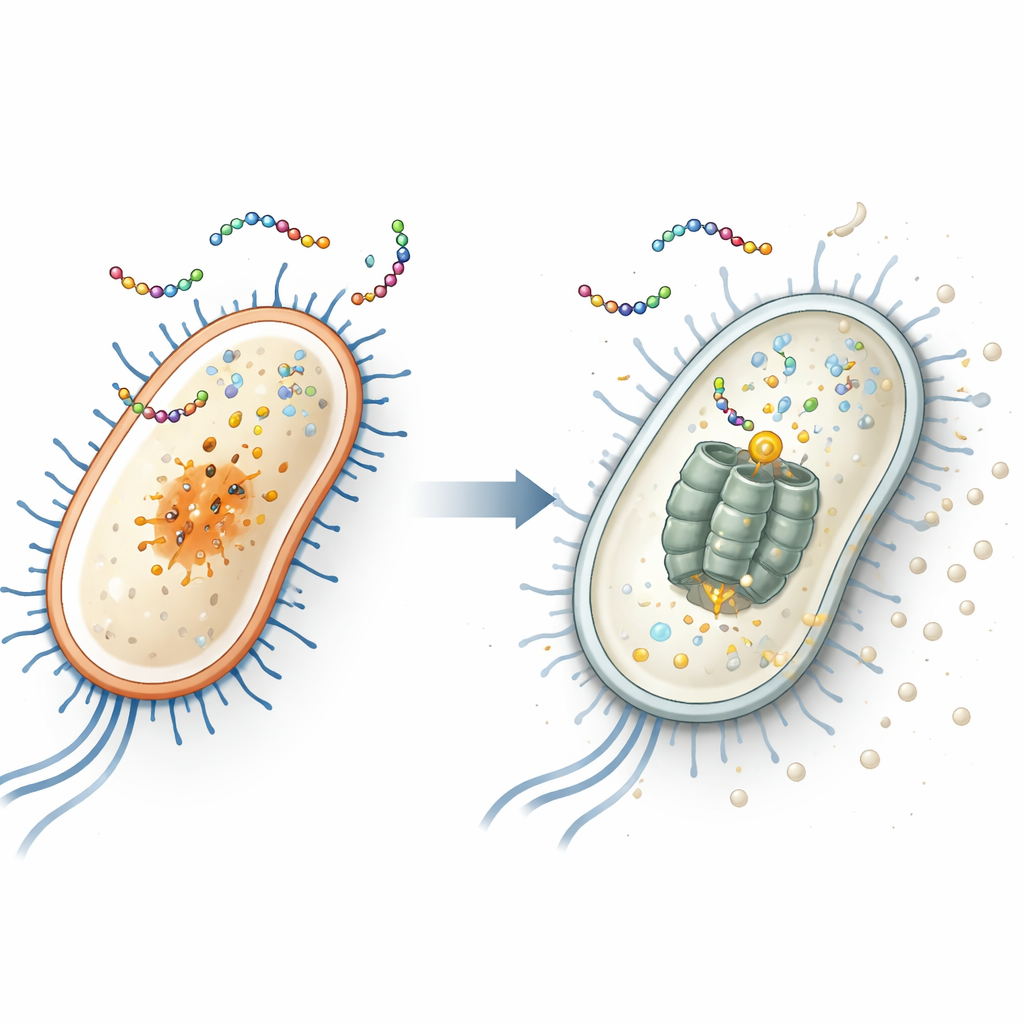
在大肠杆菌内部发现隐藏的靶点
为了识别该肽的细胞内靶点,研究人员反复将两种常见细菌——包括可能含有致病株的肠道细菌大肠杆菌(Escherichia coli)和常见的皮肤及医院感染病原金黄色葡萄球菌(Staphylococcus aureus)——暴露于EWAMP-R,直到出现耐药菌株。通过测序存活者的基因组,他们发现耐药的大肠杆菌在名为clpX的基因中携带特定突变。该基因编码分解受损或调节性蛋白的分子“粉碎机”的一部分。当研究者使用CRISPR基因编辑重建这一精确突变时,大肠杆菌对EWAMP-R的敏感性下降,这强烈暗示ClpX蛋白是该肽的关键体内靶点。
干扰细菌的蛋白质粉碎机
进一步的实验证明了EWAMP-R如何干扰这一蛋白机器。通过结合测试、计算对接和分子模拟,作者发现该肽嵌入ClpX的一个区域,该区域通常结合并利用ATP(细胞的能量货币)来驱动蛋白质降解。当EWAMP-R与此处结合时,它限制了ClpX为正常工作所需的构象变化,并显著降低其ATP驱动的活性。ClpX系统通常处理的一个重要蛋白是名为LexA的总调控因子的片段,LexA控制细菌的SOS反应——一组启动DNA修复基因的应激程序。当ClpX被阻断时,该LexA片段累积并持续抑制SOS基因,阻碍正常的DNA修复,推动细胞走向不可逆的、类似凋亡的死亡。
细菌生活方式出现意想不到的改变
研究团队还发现,耐药伴随着代价。进化出对EWAMP-R耐药的大肠杆菌不仅携带clpX突变,还产生异常长且数量众多的鞭毛——细菌用于运动的鞭状结构。基因表达模式证实,与鞭毛相关的基因被强烈过度激活。以往研究表明,此类“超鞭毛化”细菌可能反而降低附着宿主组织的能力,并更易被免疫系统识别,从而可能降低其致病能力。相比之下,在金黄色葡萄球菌中,耐药并不以ClpX为中心。相反,耐药细胞放慢了代谢速度,特别是在氨基酸及其他构建模块的通路上,生长更慢,可能作为病原体的攻击性也随之降低。
为未来药物设计更聪明的肽类分子
由于EWAMP-R既干扰细菌膜又堵塞体内的蛋白机器,它迫使细菌在多个层面同时适应——这是一项能量代价高昂的挑战。现有药物中很少有直接针对ClpX系统的,而这项工作将其识别为影响人类的细菌的一个新弱点。作者概述了进一步改造EWAMP-R的方法,例如调整特定氨基酸以更紧密地结合ClpX,或帮助肽更容易穿透不同的细菌膜,以及使用非天然构件提高其在体内的稳定性。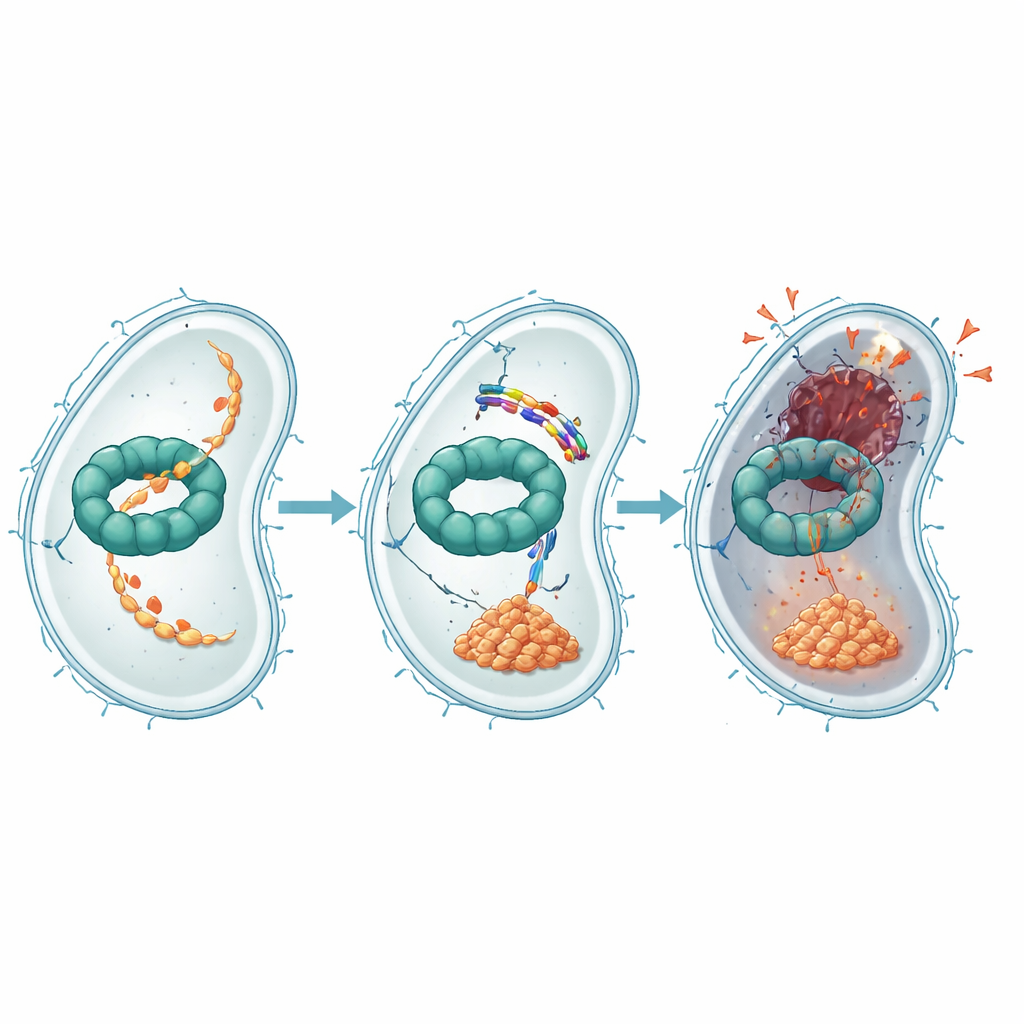
这对抗击耐药感染意味着什么
简单来说,这项研究表明一种来自蠕虫的小型肽能够潜入细菌并堵塞关键的内部机器,同时也破坏其外层结构。通过阻断通常清除关键应激调控因子的系统,EWAMP-R将大肠杆菌困在一种无法正确修复DNA的自毁状态。即便细菌进化出某种耐药性,它们也要付出生长变慢或致病能力可能下降的代价。综合来看,这些发现表明EWAMP-R及其为蓝本的分子,可能为一代更难被病原体轻易破解的多面向抗菌剂提供灵感。
引用: Wu, Y., Tang, H., Hao, P. et al. Identification of intracellular target of antimicrobial peptide EWAMP-R in bacteria. Commun Biol 9, 564 (2026). https://doi.org/10.1038/s42003-026-09822-5
关键词: 抗菌肽, 抗生素耐药性, 细菌应激反应, 蛋白质质量控制, ClpX蛋白酶