Clear Sky Science · pl
Identyfikacja wewnątrzkomórkowego celu peptydu przeciwbakteryjnego EWAMP-R w bakteriach
Dlaczego cząsteczka z małego robaka ma znaczenie dla superbakterii
W miarę jak rośnie oporność na antybiotyki, lekarzom kończą się sposoby na zatrzymanie niebezpiecznych zakażeń bakteryjnych. To badanie bada obiecującą alternatywę: małą naturalną cząsteczkę, peptyd przeciwbakteryjny o nazwie EWAMP-R, po raz pierwszy wykrytą w dżdżownicach. Naukowcy pokazują, że peptyd ten robi więcej niż tylko tworzy pory w błonach bakterii — sabotuje także kluczową wewnętrzną maszynerię, której bakterie potrzebują do przetrwania, co wskazuje na nową klasę terapii mogących wyprzedzić rozwój oporności.
Atak na dwóch frontach
Większość antybiotyków działa, atakując pojedynczy ważny proces, na przykład syntezę ściany komórkowej. Bakterie mogą w końcu ewoluować, by obejść taki atak. Peptydy przeciwbakteryjne często jednak uderzają w bakterie na wielu frontach. Wcześniej wykazano, że EWAMP-R uszkadza błony bakteryjne i wywołuje rodzaj zaprogramowanej śmierci komórki u bakterii, podobnej do apoptozy w komórkach ludzkich. W tym badaniu zespół postanowił zrozumieć, co dzieje się wewnątrz komórki po tym, jak EWAMP-R przekroczy błonę — konkretnie, który wewnętrzny element jest celem i jak ta interakcja prowadzi do śmierci bakterii.
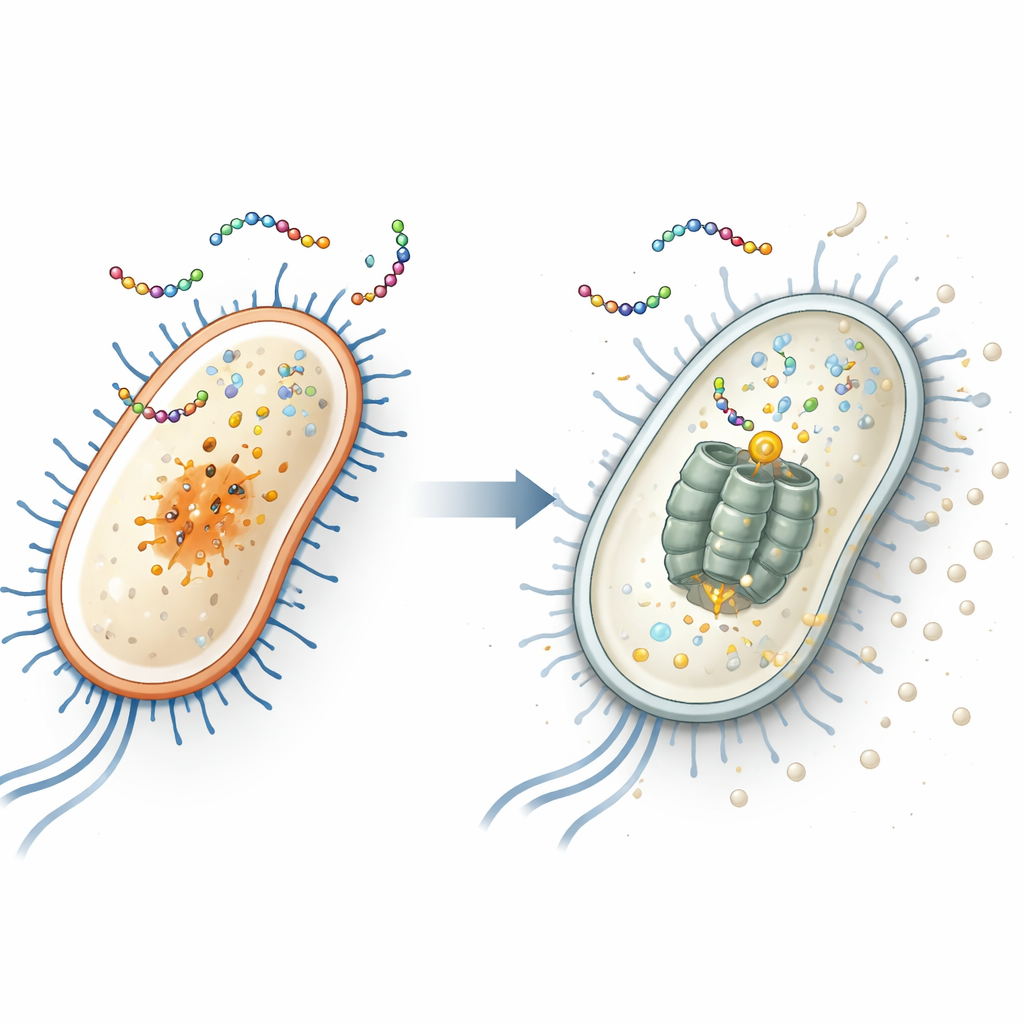
Odkrycie ukrytego celu w E. coli
Aby odkryć wewnątrzkomórkowy cel peptydu, badacze wielokrotnie eksponowali dwa powszechne gatunki bakterii — Escherichia coli (bakteria jelitowa obejmująca szczepy niebezpieczne) i Staphylococcus aureus (częsta przyczyna zakażeń skóry i zakażeń szpitalnych) — na EWAMP-R, aż pojawiły się szczepy oporne. Sekwencjonując genomy tych ocalałych, stwierdzili, że oporne E. coli miały specyficzną mutację w genie o nazwie clpX. Gen ten koduje część molekularnej „szatkownicy”, która rozkłada uszkodzone lub regulacyjne białka. Gdy odtworzyli tę dokładną mutację za pomocą edycji genów CRISPR, E. coli stała się mniej wrażliwa na EWAMP-R, co silnie sugeruje, że białko ClpX jest kluczowym wewnętrznym celem peptydu.
Zablokowanie bakteryjnej „szatkownicy” białek
Dalsze eksperymenty pokazały, jak EWAMP-R zakłóca działanie tej maszynerii białkowej. Przy użyciu testów wiązania, dokowania komputerowego i symulacji molekularnych autorzy stwierdzili, że peptyd umieszcza się w obszarze ClpX, który normalnie wiąże i wykorzystuje ATP — walutę energetyczną komórki — do napędzania rozkładu białek. Gdy EWAMP-R wiąże się w tym miejscu, ogranicza zmiany konformacyjne potrzebne ClpX do prawidłowej pracy i ostro zmniejsza jego aktywność napędzaną ATP. Jednym z ważnych białek normalnie przetwarzanych przez system ClpX jest fragment głównego regulatora zwanego LexA, który kontroluje bakteryjną odpowiedź SOS — program stresowy włączający geny naprawy DNA. Kiedy ClpX jest zablokowany, ten fragment LexA się gromadzi i dalej hamuje geny SOS, uniemożliwiając właściwą naprawę DNA i popychając komórkę w kierunku nieodwracalnej, przypominającej apoptozę śmierci.
Niespodziewane zmiany w stylu życia bakterii
Zespół odkrył również, że oporność niesie ze sobą koszty. E. coli, które wyewoluowały oporność na EWAMP-R, nie tylko miały mutację w clpX, lecz także produkowały wyjątkowo długie i liczne rzęski — biczykowate ogonki, których bakterie używają do ruchu. Wzorce ekspresji genów potwierdziły, że geny związane z rzęskami były silnie nadaktywne. Wcześniejsze badania sugerują, że takie „hiperrzęsiste” bakterie mogą w rzeczywistości gorzej przylegać do tkanek gospodarza i stać się bardziej widoczne dla układu odpornościowego, co może zmniejszyć ich zdolność do wywoływania choroby. W S. aureus natomiast oporność nie skupiała się na ClpX. Zamiast tego komórki oporne zwolniły metabolizm, szczególnie w ścieżkach związanych z aminokwasami i innymi blokami budulcowymi, rosnąc wolniej i prawdopodobnie stając się mniej agresywne jako patogeny.
Projektowanie sprytniejszych peptydów dla przyszłych leków
Ponieważ EWAMP-R jednocześnie zaburza błony bakterii i blokuje wewnętrzną maszynerię białkową, zmusza bakterie do adaptacji na wielu poziomach naraz — co jest energetycznie kosztownym wyzwaniem. Niewiele istniejących leków celuje bezpośrednio w system ClpX, a ta praca identyfikuje go jako nowe słabe ogniwo w bakteriach wpływających na ludzi. Autorzy wskazują sposoby dalszego udoskonalenia EWAMP-R, takie jak modyfikacja konkretnych aminokwasów by silniej wiązać ClpX lub ułatwić peptydowi przenikanie przez różne błony bakteryjne, oraz użycie nienaturalnych bloków budulcowych, by zwiększyć jego stabilność w organizmie.
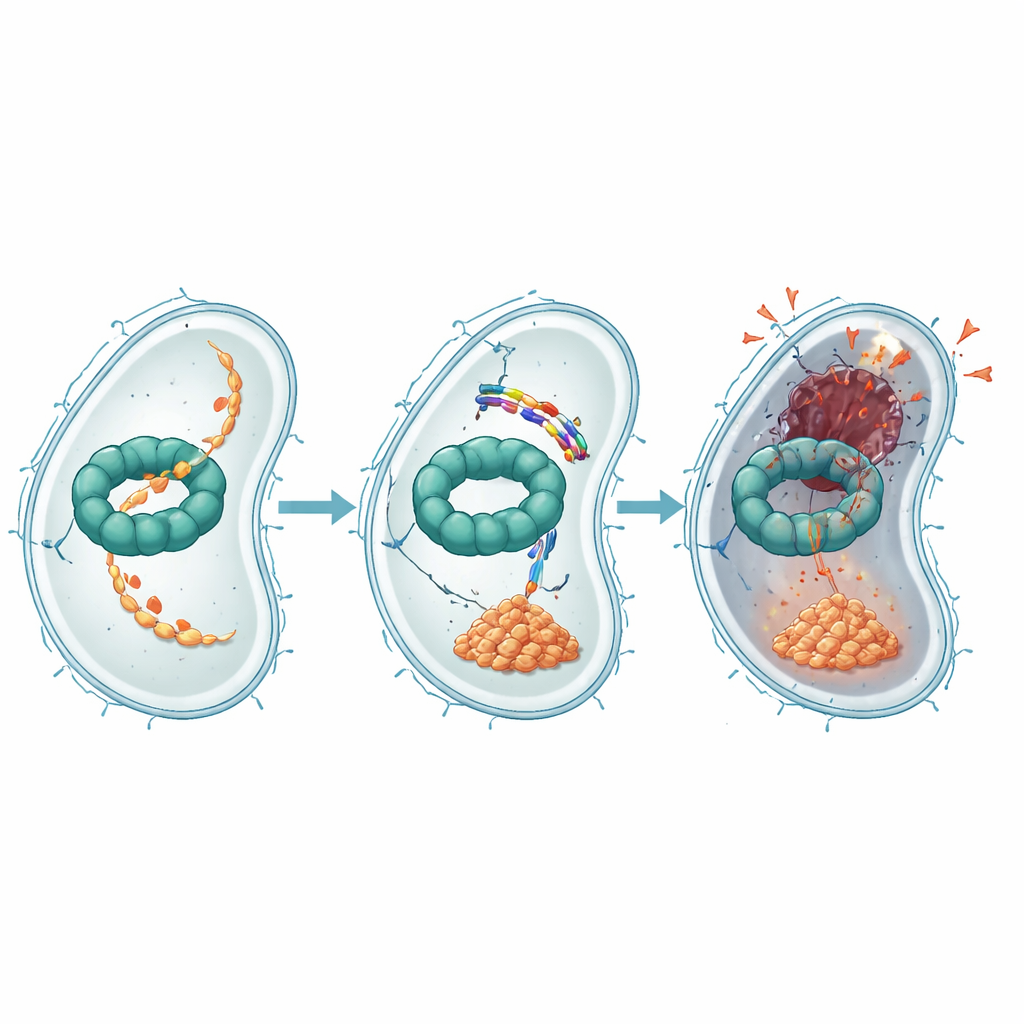
Co to oznacza dla walki z opornymi zakażeniami
Mówiąc najprościej, badanie pokazuje, że mały peptyd pochodzący od robaka może wślizgnąć się do bakterii i zablokować istotną wewnętrzną maszynę, równocześnie tworząc dziury w ich zewnętrznej powłoce. Poprzez zablokowanie systemu, który zwykle usuwa kluczowego regulatora stresu, EWAMP-R uwięzi E. coli w autodestrukcyjnym stanie, w którym nie potrafi prawidłowo naprawiać DNA. Nawet gdy bakterie rozwijają pewną oporność, płacą za to wolniejszym wzrostem lub potencjalnie zmniejszoną zdolnością do wywoływania choroby. Razem te ustalenia sugerują, że EWAMP-R i cząsteczki wzorowane na nim mogą zainspirować nową generację wielotorowych środków przeciwbakteryjnych, których patogeny trudniej będzie przechytrzyć.
Cytowanie: Wu, Y., Tang, H., Hao, P. et al. Identification of intracellular target of antimicrobial peptide EWAMP-R in bacteria. Commun Biol 9, 564 (2026). https://doi.org/10.1038/s42003-026-09822-5
Słowa kluczowe: peptydy przeciwbakteryjne, oporność na antybiotyki, odpowiedź stresowa bakterii, kontrola jakości białek, proteaza ClpX