Clear Sky Science · he
זיהוי המטרה התוך-תאית של הפפטיד האנטימיקרוביאלי EWAMP-R בחיידקים
למה מולקולה זעירה של תולעת חשובה לגבי חיידקים-על
עם עליית העמידות לאנטיביוטיקה, לרופאים מאוזלים האמצעים לעצור זיהומים חיידקיים מסוכנים. מחקר זה חוקר אלטרנטיבה מבטיחה: מולקולה טבעית קטנה, פפטיד אנטימיקרוביאלי בשם EWAMP-R, שמקורה בתולעי אדמה. החוקרים מראים כי הפפטיד עושה יותר מאשר ליצור נקבים בממברנת החיידק — הוא גם משבית מכונה פנימית חשובה שהחיידקים זקוקים לה כדי לשרוד, ומצביע על כיוון טיפולים חדש שעשוי להקדים את עקומת העמידות.
מתקפה על שני חזיתות מול החיידק
מרבית האנטיביוטיקות פועלות על ידי פגיעה בתהליך חיוני יחיד, כמו בניית דופן התא. חיידקים בסופו של דבר יכולים להתאים עצמם להתקפות אלה. פפטידים אנטימיקרוביאליים, לעומת זאת, נוטים לפגוע בחיידקים במספר חזיתות. כבר הוכח כי EWAMP-R פוגע בממברנות החיידק ומפעיל סוג של מוות מתוכנת בחיידקים, דומה לאפופטוזיס בתאים של בעלי חיים. במחקר זה קיבעה הקבוצה להבין מה מתרחש בתוך התא לאחר ש-EWAMP-R חוצה את הממברנה — ובפרט, איזו מולקולה פנימית היא המטרה וכיצד האינטראקציה הזו מביאה למות החיידק.
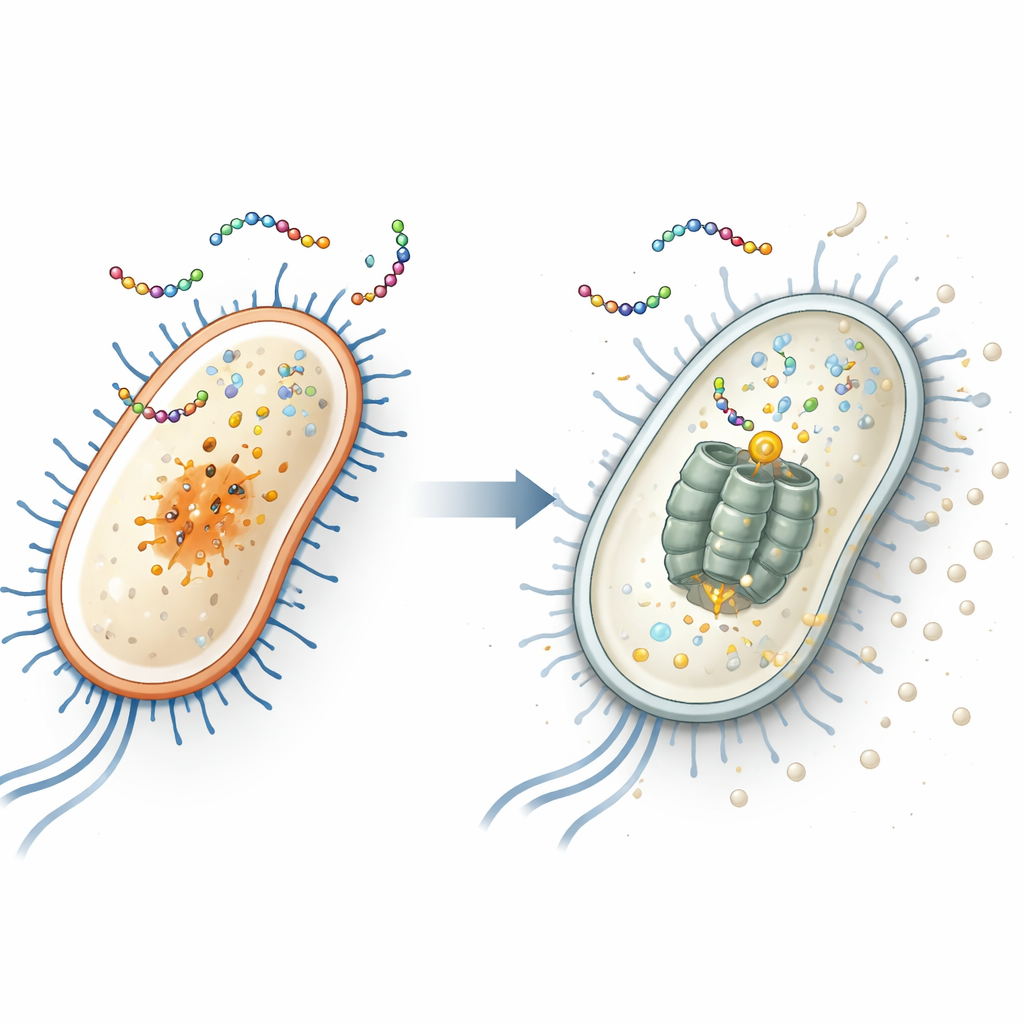
מציאת המטרה החבויה בתוך E. coli
כדי לגלות את המטרה הפנימית של הפפטיד, החוקרים חשפו שוב ושוב שני חיידקים נפוצים — Escherichia coli (חיידק מעי שכולל זנים מסוכנים) ו-Staphylococcus aureus (גורם שכיח לזיהומי עור ובתי חולים) — ל-EWAMP-R עד שבקעו זני עמידים. באמצעות רצפי הגנום של שורדים אלה הם גילו כי ב-E. coli העמידה נשא מוטציה ספציפית בגֶן בשם clpX. גן זה מקודד חלק ממערכת “המגרסה” המולקולרית שמפורקת חלבונים פגומים או רגולטוריים. כשהחוקרים שיחזרו את המוטציה המדויקת באמצעות עריכת גנים CRISPR, E. coli הפכו לפחות רגישים ל-EWAMP-R, מה שמרמז בחוזקה כי חלבון ClpX הוא המטרה הפנימית המרכזית של הפפטיד.
חסימת מגרסת החלבונים החיידקית
ניסויים נוספים הראו כיצד EWAMP-R מפריע למכונה החלבונית הזו. באמצעות מבחני קשירה, דוקינג חישובי וסימולציות מולקולריות מצאו המחברים שהפפטיד מתמקם באזור של ClpX שבמידה רגילה קושר ומנצל ATP — מטבע האנרגיה של התא — כדי להניע את פירוק החלבונים. כאשר EWAMP-R נקשר שם, הוא מגביל את השינויים הצורתיים ש-ClpX זקוק להם לפעולה תקינה ומצמצם באופן חד את פעילות ה-ATP המונעת. חלבון חשוב שעבר בדרך כלל עיבוד על ידי מערכת ClpX הוא שבר של רגולטור ראשי בשם LexA, השולט בתוכנית ה-SOS של החיידק — תוכנית לחץ שמפעילה גנים לתיקון DNA. כשה-ClpX נחסם, שבר ה-LexA מצטבר וממשיך לדכא את גני ה-SOS, מונע תיקון DNA תקין ודוחף את התא למצב בלתי-הפיך של מוות בדומה לאפופטוזיס.
שינויים בלתי צפויים בסגנון החיים החיידקי
הצוות גילה גם שלעמידות יש מחיר. ב-E. coli שהתפתחו לעמידות ל-EWAMP-R נמצאה לא רק מוטציית clpX אלא גם ייצור יוצא דופן של שוטונים (flagella) ארוכים ורבים — זנבות שוט כמו המשמשים לתנועה. דפוסי ביטוי גנטי אישרו כי גנים הקשורים לשוטונים היו פעילים באופן מוגבר. עבודות קודמות מציעות כי חיידקים “היפר-שוטונאיים” כאלה עלולים דווקא להפוך לפחות מסוגלים להיצמד לרקמות המאכסן ולקלות יותר לזיהוי על ידי מערכת החיסון, מה שעשוי לצמצם את יכולתם לגרום מחלה. ב-S. aureus, לעומת זאת, העמידות לא התרכזה ב-ClpX. במקום זאת, תאים עמידים האטו את המטבוליזם שלהם, במיוחד בדרכי החומצות האמיניות ושאר מסלולי הבנייה — גדלו לאט יותר וסביר שבכך נעשו פחות אגרסיביים כפתוגנים.
עיצוב פפטידים חכמים יותר לתרופות עתידיות
מכיוון ש-EWAMP-R מפר את הממברנות החיידקיות וחוסם גם מכונה חלבונית פנימית, הוא מאלץ את החיידקים להסתגל במספר רמות בו־זמנית — אתגר שדורש משאבים אנרגטיים ניכרים. תרופות מועטות כעת מפעילות ישירות את מערכת ClpX, ומחקר זה מזהה אותה כנקודת תורפה חדשה בחיידקים הפוגעים בבני אדם. המחברים מפרטים דרכים לשכלל עוד את EWAMP-R, כגון כיוונון חומצות אמינו ספציפיות לחיזוק הקשירה ל-ClpX או לסייע לפפטיד לחדור בקלות רבה יותר דרך ממברנות חיידקיות שונות, וכן שימוש בבוני-אבנים לא טבעיים כדי להפוך אותו יציב יותר בגוף.
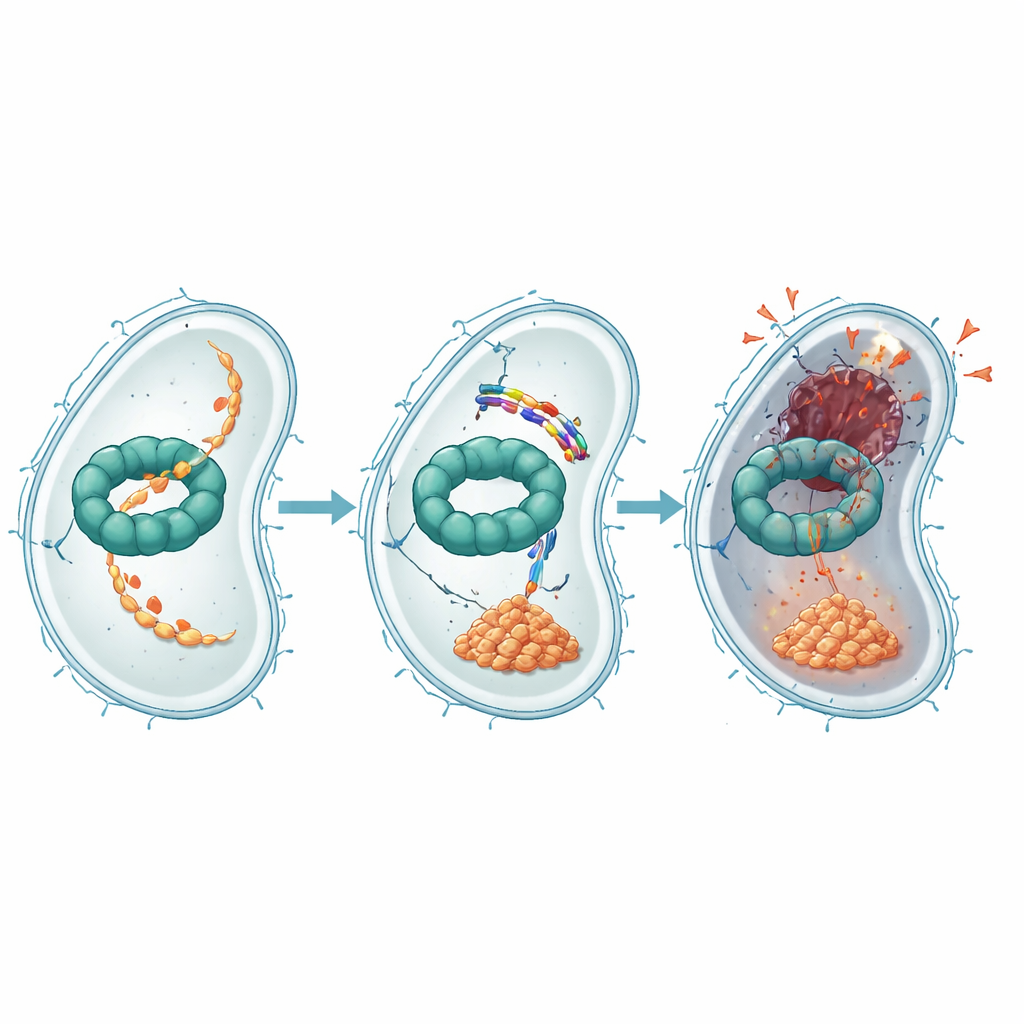
מה המשמעות של זה במאבק בזיהומים עמידים
במילים פשוטות, מחקר זה מראה שפפטיד קטן שמוצאו בתולעת יכול להחליק לתוך חיידקים ולחסום מכונה פנימית חיונית, ובו־זמנית ליצור חורים במעטפת החיצונית שלהם. על ידי חסימת המערכת שמנקה רגולטור לחץ מרכזי, EWAMP-R לוכד את E. coli במצב של הרס עצמי שבו הם אינם יכולים לתקן את ה-DNA כראוי. אפילו כאשר החיידקים מפתחים מעט עמידות, הם משלמים במחיר של גידול איטי יותר או ביכולתם המופחתת ככל הנראה לגרום למחלה. יחד, ממצאים אלה מציעים כי EWAMP-R ומולקולות המחקות אותו עשויות לשמש השראה לדור חדש של סוכנים אנטיבקטריאלים מרובי-מערך שקשה יותר לפתוגנים להערים עליהם.
ציטוט: Wu, Y., Tang, H., Hao, P. et al. Identification of intracellular target of antimicrobial peptide EWAMP-R in bacteria. Commun Biol 9, 564 (2026). https://doi.org/10.1038/s42003-026-09822-5
מילות מפתח: פפטידים אנטימיקרוביאליים, עמידות לאנטיביוטיקה, תגובה ללחץ בחיידקים, בקרת איכות של חלבונים, פרוטאז ClpX