Clear Sky Science · ru
Идентификация внутриклеточной мишени антимикробного пептида EWAMP-R в бактериях
Почему молекула крошечного червя важна для супербактерий
По мере роста антибиотикорезистентности врачам всё сложнее сдерживать опасные бактериальные инфекции. В этом исследовании рассматривается перспективная альтернатива: небольшая природная молекула, антимикробный пептид EWAMP-R, впервые обнаруженная в дождевых червях. Авторы показывают, что пептид делает не только «дыры» в мембранах бактерий — он также саботирует важный внутриклеточный механизм, необходимый для выживания бактерий, указывая на новый класс препаратов, который может опережать развитие резистентности.
Атака по двум направлениям
Большинство антибиотиков действуют, нацеливаясь на один жизненно важный процесс, например на синтез клеточной стенки. Бактерии в конечном счёте могут эволюционировать в обход таких атак. Антимикробные пептиды, однако, часто поражают бактерии по нескольким фронтам одновременно. Ранее было показано, что EWAMP-R повреждает бактериальные мембраны и вызывает у бактерий некое программируемое разрушение, отчасти похожее на апоптоз у эукариот. В этом исследовании команда попыталась выяснить, что происходит внутри клетки после того, как EWAMP-R проходит через мембрану — в частности, какую внутреннюю молекулу он нацеливает и как это взаимодействие приводит к гибели бактерии.
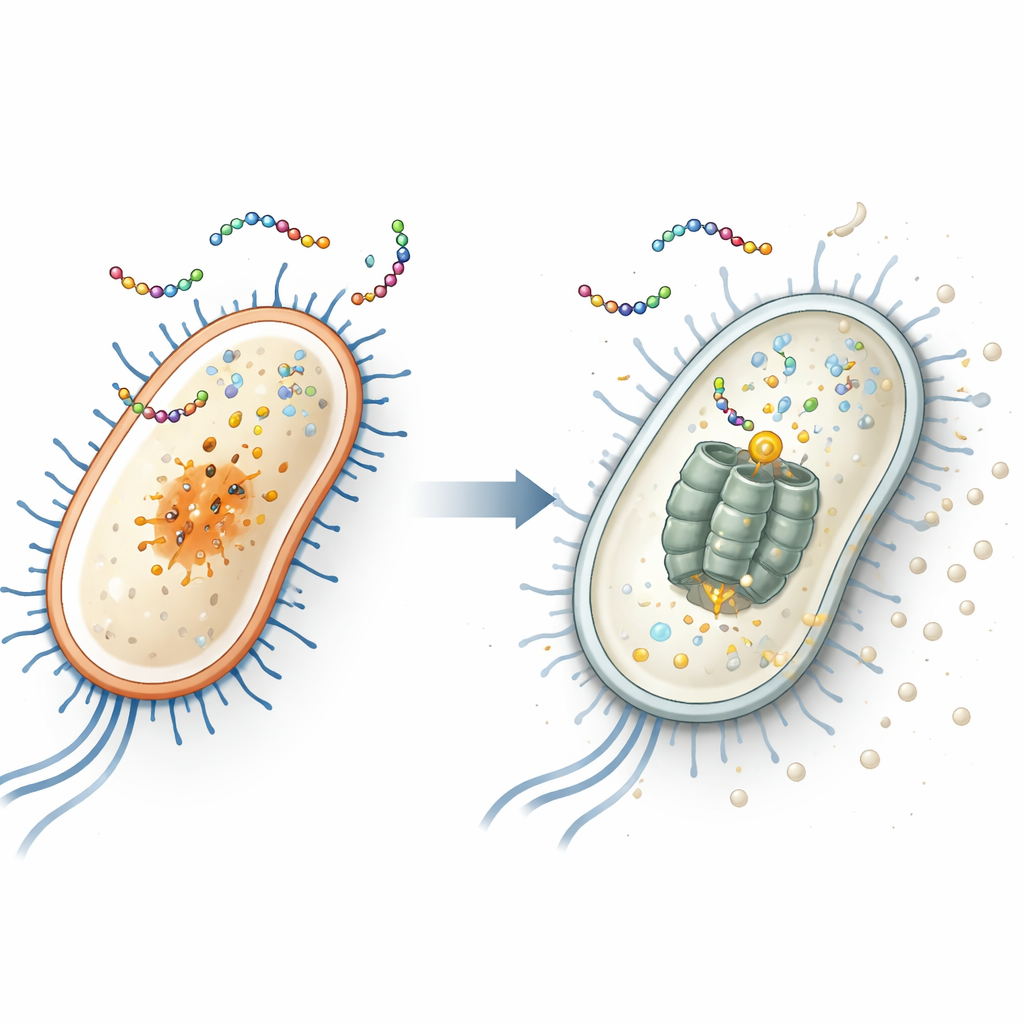
Поиск скрытой мишени внутри E. coli
Чтобы обнаружить внутриклеточную мишень пептида, исследователи многократно подвергали двух распространённых бактерий — Escherichia coli (кишечная бактерия, включающая опасные штаммы) и Staphylococcus aureus (частая причина кожных и внутрибольничных инфекций) — воздействию EWAMP-R до появления резистентных штаммов. Последовавшее секвенирование геномов выживших показало, что у резистентных штаммов E. coli обнаруживалась специфическая мутация в гене clpX. Этот ген кодирует часть молекулярного «шредера», разрушающего повреждённые или регуляторные белки. Воссоздав эту точную мутацию с помощью редактирования CRISPR, учёные сделали E. coli менее чувствительной к EWAMP-R, что убедительно указывает на белок ClpX в качестве ключевой внутриклеточной мишени пептида.
Заклинивание бактериального белкового шредера
Дальнейшие эксперименты показали, как именно EWAMP-R мешает работе этого белкового комплекса. С помощью тестов связывания, компьютерного докинга и молекулярного моделирования авторы обнаружили, что пептид встраивается в участок ClpX, который обычно связывает и использует АТФ — энергетическую «валюту» клетки — для приведения в действие протеолиза. Когда EWAMP-R связывается с этим участком, он ограничивает необходимые для работы конформационные изменения ClpX и резко снижает его АТФ-зависимую активность. Один важный белок, обычно обрабатываемый системой ClpX, — это фрагмент главного регулятора LexA, который контролирует SOS-ответ бактерии — стрессовую программу включения генов ремонта ДНК. При блокировке ClpX этот фрагмент LexA накапливается и продолжает подавлять гены SOS, препятствуя адекватному ремонту ДНК и толкая клетку к необратимой, подобной апоптозу гибели.
Неожиданные изменения в образе жизни бактерий
Команда также обнаружила, что приобретение резистентности связано с ценой. E. coli, эволюционировавшие к резистентности к EWAMP-R, не только несли мутацию в clpX, но и производили необычно длинные и многочисленные жгутики — хлыстообразные хвосты, которые бактерии используют для движения. Анализ экспрессии генов подтвердил сильную гиперактивность генов, связанных с жгутиками. Предыдущие исследования предполагают, что такие «гипержгутиковые» бактерии могут хуже прикрепляться к тканям хозяина и лучше заметны иммунной системе, что потенциально снижает их патогенность. У S. aureus, напротив, резистентность не была связана с ClpX: устойчивые клетки замедляли метаболизм, особенно в путях синтеза аминокислот и других строительных блоков, росли медленнее и, вероятно, становились менее агрессивными как патогены.
Проектирование более умных пептидов для медицины будущего
Поскольку EWAMP-R одновременно нарушает бактериальные мембраны и заклинивает внутриклеточный белковый механизм, он вынуждает бактерии приспосабливаться на нескольких уровнях сразу — энергозатратный вызов. Мало какие существующие препараты прямо нацелены на систему ClpX, и это исследование выделяет её как новую уязвимость у бактерий, поражающих человека. Авторы намечают пути для дальнейшей оптимизации EWAMP-R, например изменение отдельных аминокислот для более плотного связывания с ClpX или облегчения прохождения пептида через разные бактериальные мембраны, а также использование неестественных строительных блоков для повышения стабильности в организме. 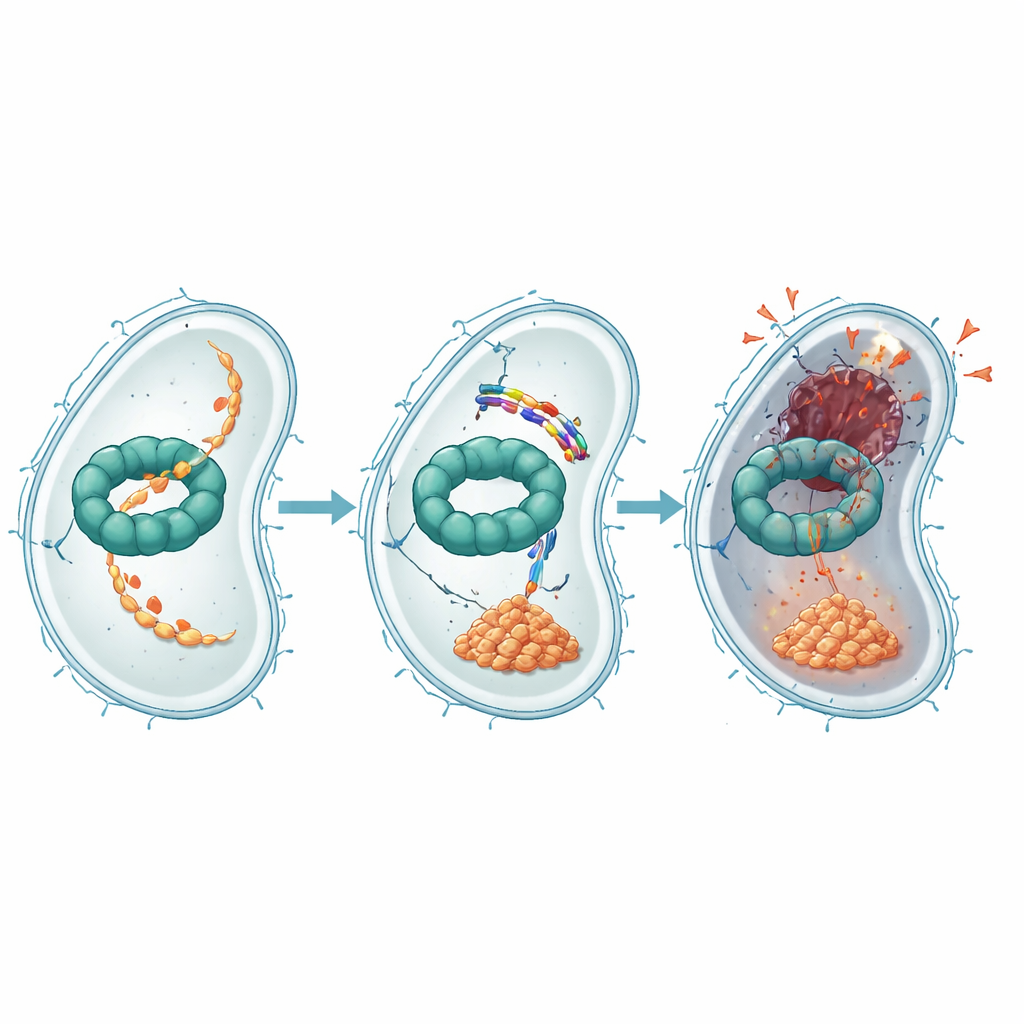
Что это означает для борьбы с резистентными инфекциями
Проще говоря, это исследование показывает, что небольшой пептид, полученный от червя, может проникать в бактерии и блокировать жизненно важный внутриклеточный механизм, одновременно проделывая дыры в их наружной оболочке. Блокируя систему, которая обычно удаляет ключевой регулятор стресса, EWAMP-R запирает E. coli в самоуничтожительном состоянии, при котором она не может адекватно ремонтировать ДНК. Даже когда бактерии вырабатывают некоторую резистентность, им приходится расплачиваться замедленным ростом или потенциально сниженной способностью вызывать заболевание. В совокупности эти результаты указывают на то, что EWAMP-R и молекулы, смоделированные по его образцу, могут послужить источником идеи для нового поколения многоцелевых антибактериальных средств, которые труднее обойти патогенам.
Цитирование: Wu, Y., Tang, H., Hao, P. et al. Identification of intracellular target of antimicrobial peptide EWAMP-R in bacteria. Commun Biol 9, 564 (2026). https://doi.org/10.1038/s42003-026-09822-5
Ключевые слова: антимикробные пептиды, антибактериальная резистентность, бактериальный стрессовый ответ, контроль качества белков, протеаза ClpX