Clear Sky Science · fr
Identification de la cible intracellulaire du peptide antimicrobien EWAMP-R chez les bactéries
Pourquoi une petite molécule de ver compte pour les super‑bactéries
Alors que la résistance aux antibiotiques augmente, les médecins manquent de moyens pour stopper les infections bactériennes dangereuses. Cette étude explore une alternative prometteuse : une petite molécule naturelle, un peptide antimicrobien appelé EWAMP-R, initialement isolé chez les vers de terre. Les chercheurs montrent que ce peptide ne se contente pas de percer les membranes bactériennes : il sabote aussi une machine interne cruciale pour la survie bactérienne, ouvrant la voie à une nouvelle classe de traitements susceptibles de garder une longueur d’avance sur la résistance.
Une attaque bactérienne sur deux fronts
La plupart des antibiotiques agissent en ciblant un seul processus vital, comme la synthèse de la paroi cellulaire. Les bactéries peuvent finir par évoluer pour contourner ces attaques. Les peptides antimicrobiens, en revanche, frappent souvent les bactéries sur plusieurs fronts. On savait déjà que EWAMP-R endommageait les membranes bactériennes et déclenchait une sorte de mort programmée chez les bactéries, un peu analogue à l’apoptose des cellules humaines. Dans cette étude, l’équipe a cherché à comprendre ce qui se passe à l’intérieur de la cellule après que EWAMP-R a franchi la membrane — en particulier quelle molécule intracellulaire il cible et comment cette interaction conduit à la mort bactérienne.
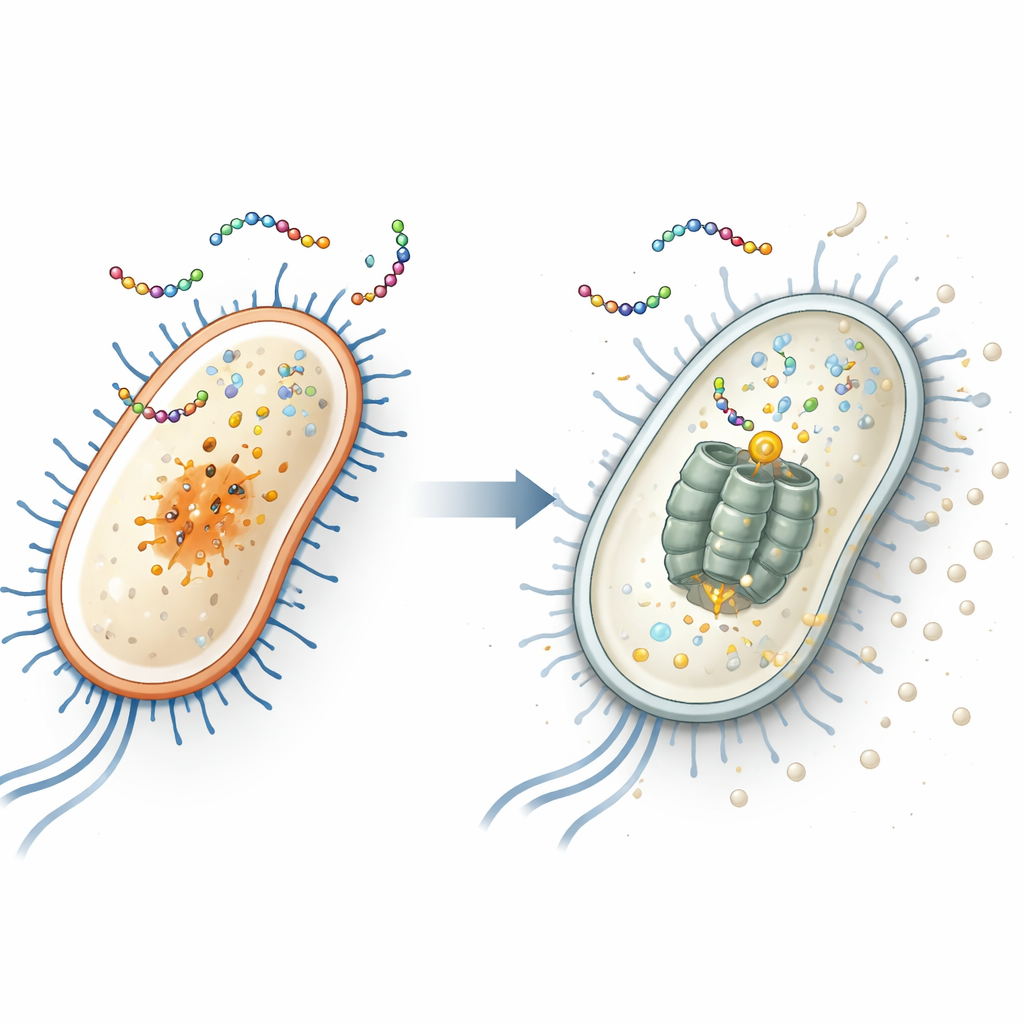
Trouver la cible cachée à l’intérieur d’E. coli
Pour identifier la cible intracellulaire du peptide, les chercheurs ont exposé de façon répétée deux bactéries courantes — Escherichia coli (une bactérie intestinale qui comprend des souches dangereuses) et Staphylococcus aureus (une cause fréquente d’infections cutanées et nosocomiales) — à EWAMP-R jusqu’à l’émergence de souches résistantes. En séquençant les génomes de ces survivants, ils ont découvert que les E. coli résistantes portaient une mutation spécifique dans un gène appelé clpX. Ce gène code pour une partie d’un « broyeur » moléculaire qui dégrade les protéines endommagées ou régulatrices. Lorsqu’ils ont recréé exactement cette mutation par édition génétique CRISPR, E. coli est devenue moins sensible à EWAMP-R, ce qui implique fortement que la protéine ClpX est la cible intracellulaire clé du peptide.
Gripper le broyeur protéique bactérien
Des expériences supplémentaires ont montré comment EWAMP-R perturbe cette machinerie protéique. Grâce à des tests de liaison, du docking informatique et des simulations moléculaires, les auteurs ont constaté que le peptide s’insinue dans une région de ClpX qui lie normalement l’ATP, la monnaie énergétique de la cellule, pour alimenter la dégradation protéique. Quand EWAMP-R se lie à cet endroit, il restreint les changements de conformation nécessaires au fonctionnement de ClpX et réduit fortement son activité dépendante de l’ATP. Une protéine importante habituellement traitée par le système ClpX est un fragment d’un régulateur maître appelé LexA, qui contrôle la réponse SOS bactérienne — un programme de stress qui active les gènes de réparation de l’ADN. Quand ClpX est bloqué, ce fragment de LexA s’accumule et continue à réprimer les gènes SOS, empêchant une réparation adéquate de l’ADN et poussant la cellule vers une mort irréversible de type apoptotique.
Modifications inattendues du mode de vie bactérien
L’équipe a aussi découvert que la résistance a un coût. Les E. coli qui avaient évolué une résistance à EWAMP-R ne présentaient pas seulement la mutation de clpX, elles produisaient également des flagelles exceptionnellement longs et nombreux — ces queues fouettées que les bactéries utilisent pour se déplacer. Les profils d’expression génique ont confirmé que les gènes liés aux flagelles étaient fortement surexprimés. Des travaux antérieurs suggèrent que de telles bactéries « hyperflagellées » peuvent en réalité perdre une partie de leur capacité à adhérer aux tissus hôtes et devenir plus visibles pour le système immunitaire, réduisant potentiellement leur pouvoir pathogène. En revanche, chez S. aureus, la résistance ne portait pas sur ClpX. Les cellules résistantes avaient plutôt ralenti leur métabolisme, en particulier dans les voies des acides aminés et d’autres éléments constitutifs, croissant plus lentement et devenant probablement moins agressives en tant qu’agents pathogènes.
Concevoir des peptides plus intelligents pour des médicaments futurs
Parce qu’EWAMP-R perturbe à la fois les membranes bactériennes et grippe une machinerie protéique interne, il contraint les bactéries à s’adapter sur plusieurs niveaux à la fois — un défi coûteux sur le plan énergétique. Peu de médicaments actuels ciblent directement le système ClpX, et ce travail l’identifie comme une nouvelle faiblesse chez les bactéries qui affectent l’homme. Les auteurs proposent des voies d’optimisation d’EWAMP-R, comme modifier certains acides aminés pour augmenter l’affinité pour ClpX ou faciliter la traversée des différentes membranes bactériennes, et utiliser des éléments non naturels pour rendre le peptide plus stable dans l’organisme. 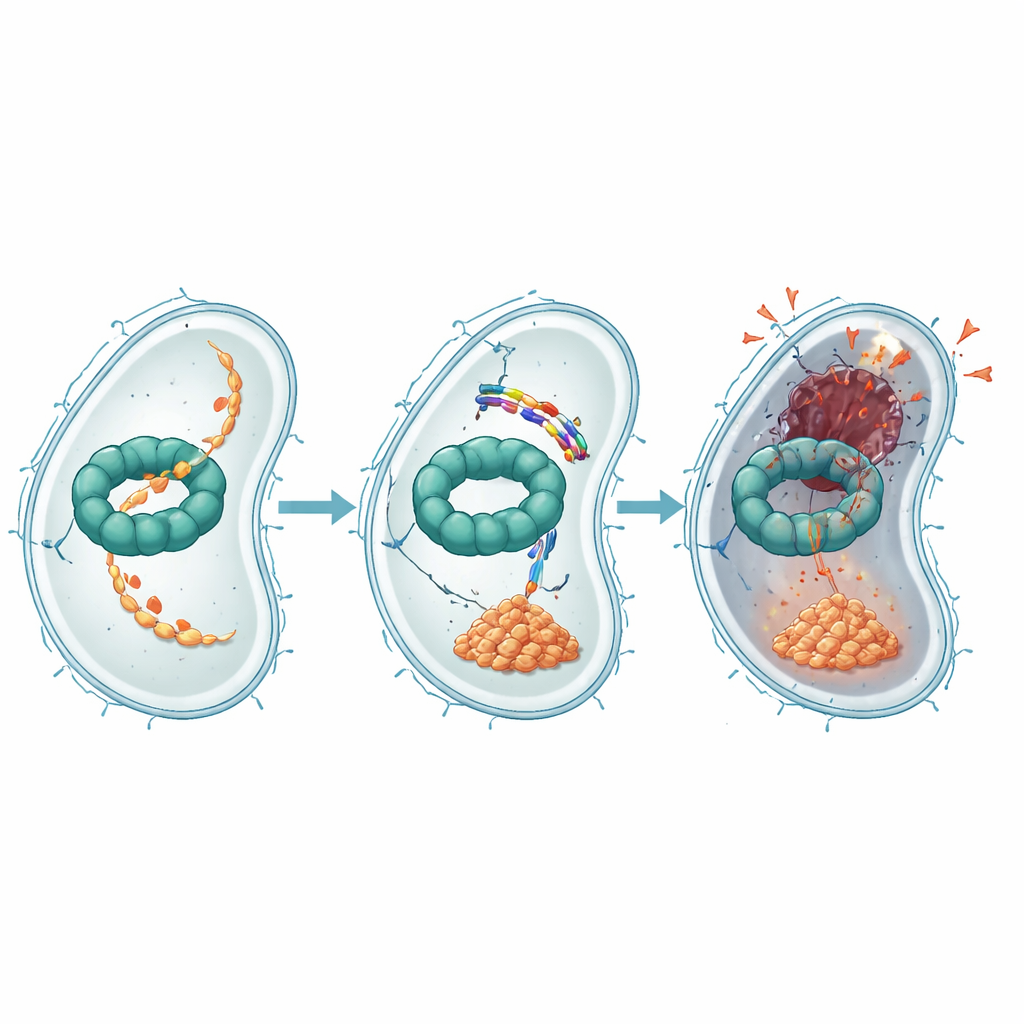
Ce que cela signifie pour la lutte contre les infections résistantes
En termes simples, cette étude montre qu’un petit peptide dérivé de ver peut s’introduire dans les bactéries et gripper une machine interne vitale, tout en perforant leur enveloppe externe. En bloquant le système qui élimine un régulateur clé du stress, EWAMP-R piège E. coli dans un état autodestructeur où elle ne peut pas réparer correctement son ADN. Même lorsque les bactéries développent une certaine résistance, elles en paient le prix par une croissance plus lente ou une capacité réduite à provoquer une maladie. Pris ensemble, ces résultats suggèrent qu’EWAMP-R, et des molécules inspirées par lui, pourraient inspirer une nouvelle génération d’agents antibactériens à actions multiples, plus difficiles à déjouer pour les agents pathogènes.
Citation: Wu, Y., Tang, H., Hao, P. et al. Identification of intracellular target of antimicrobial peptide EWAMP-R in bacteria. Commun Biol 9, 564 (2026). https://doi.org/10.1038/s42003-026-09822-5
Mots-clés: peptides antimicrobiens, résistance aux antibiotiques, réponse au stress bactérien, contrôle de la qualité des protéines, protéase ClpX