Clear Sky Science · es
Identificación del objetivo intracelular del péptido antimicrobiano EWAMP-R en bacterias
Por qué importa una molécula diminuta de lombriz frente a los supermicrobios
A medida que aumenta la resistencia a los antibióticos, los médicos se quedan sin herramientas para detener infecciones bacterianas peligrosas. Este estudio explora una alternativa prometedora: una pequeña molécula natural, un péptido antimicrobiano llamado EWAMP-R, originalmente hallado en lombrices de tierra. Los investigadores muestran que este péptido hace más que perforar las membranas bacterianas: también sabotea una máquina interna crucial que las bacterias necesitan para sobrevivir, lo que señala hacia una nueva clase de tratamientos que podrían adelantarse a la resistencia.
Un ataque a dos frentes contra las bacterias
La mayoría de los antibióticos actúan sobre un único proceso vital, como la construcción de la pared celular. Las bacterias pueden acabar evolucionando para sortear esos ataques. Los péptidos antimicrobianos, sin embargo, suelen golpear a las bacterias en múltiples frentes. Se había demostrado que EWAMP-R dañaba ya las membranas bacterianas y desencadenaba un tipo de muerte programada en bacterias, algo similar a la apoptosis en células humanas. En este estudio, el equipo se propuso comprender qué ocurre dentro de la célula después de que EWAMP-R atraviesa la membrana: en concreto, qué molécula interna apunta y cómo esa interacción conduce a la muerte bacteriana.
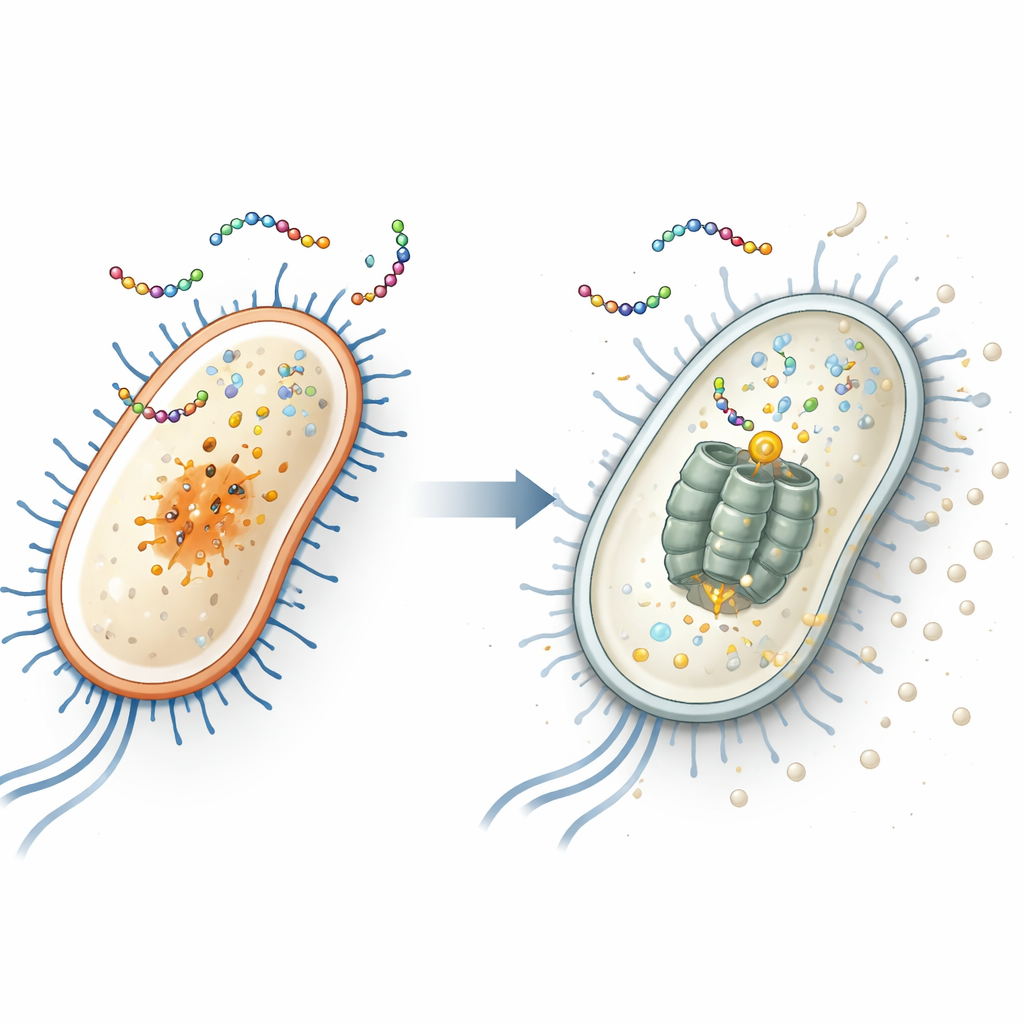
Encontrar el objetivo oculto dentro de E. coli
Para descubrir el blanco interno del péptido, los investigadores expusieron repetidamente a dos bacterias comunes —Escherichia coli (una bacteria intestinal que incluye cepas peligrosas) y Staphylococcus aureus (una causa frecuente de infecciones cutáneas y nosocomiales)— a EWAMP-R hasta que surgieron cepas resistentes. Al secuenciar los genomas de estos supervivientes, hallaron que E. coli resistente portaba una mutación específica en un gen llamado clpX. Este gen codifica parte de una “trituradora” molecular que degrada proteínas dañadas o reguladoras. Cuando recrearon exactamente esa mutación mediante edición genética CRISPR, E. coli se volvió menos sensible a EWAMP-R, lo que implica con fuerza que la proteína ClpX es el objetivo interno clave del péptido.
Atascando la trituradora de proteínas bacteriana
Experimentos adicionales mostraron cómo EWAMP-R interfiere con esta máquina proteica. Mediante ensayos de unión, acoplamientos por ordenador y simulaciones moleculares, los autores descubrieron que el péptido se instala en una región de ClpX que normalmente se une y usa ATP, la moneda energética de la célula, para impulsar la degradación de proteínas. Cuando EWAMP-R se une ahí, restringe los cambios de forma que ClpX necesita para funcionar correctamente y reduce drásticamente su actividad dependiente de ATP. Una proteína importante normalmente procesada por el sistema ClpX es un fragmento de un regulador maestro llamado LexA, que controla la respuesta SOS bacteriana —un programa de estrés que activa genes de reparación del ADN. Cuando ClpX queda bloqueado, este fragmento de LexA se acumula y continúa reprimiendo los genes SOS, impidiendo la reparación adecuada del ADN y empujando a la célula hacia una muerte irreversible, semejante a la apoptosis.
Cambios inesperados en el estilo de vida bacteriano
El equipo también descubrió que la resistencia tiene un coste. E. coli que había evolucionado resistencia a EWAMP-R no solo presentaba la mutación en clpX, sino que además producía flagelos inusualmente largos y numerosos —las colas en forma de látigo que las bacterias usan para moverse. Los patrones de expresión génica confirmaron que los genes relacionados con los flagelos estaban fuertemente sobreactivados. Trabajos previos sugieren que esas bacterias “hiperflageladas” pueden volverse en realidad menos capaces de adherirse a tejidos del huésped y más visibles para el sistema inmune, lo que podría reducir su capacidad para causar enfermedad. En S. aureus, en cambio, la resistencia no se centró en ClpX. En su lugar, las células resistentes ralentizaron su metabolismo, particularmente en rutas de aminoácidos y otros bloques de construcción, creciendo más despacio y probablemente volviéndose menos agresivas como patógenos.
Diseñar péptidos más inteligentes para futuros fármacos
Puesto que EWAMP-R tanto perturba las membranas bacterianas como atasca una máquina proteica interna, obliga a las bacterias a adaptarse en varios niveles a la vez —un desafío energéticamente costoso. Pocos fármacos existentes atacan el sistema ClpX directamente, y este trabajo lo identifica como una nueva debilidad en las bacterias que afectan a los humanos. Los autores describen maneras de refinar EWAMP-R, como ajustar aminoácidos específicos para unirse con más fuerza a ClpX o ayudar al péptido a atravesar más fácilmente distintas membranas bacterianas, y usar bloques constructores no naturales para hacerlo más estable en el organismo. 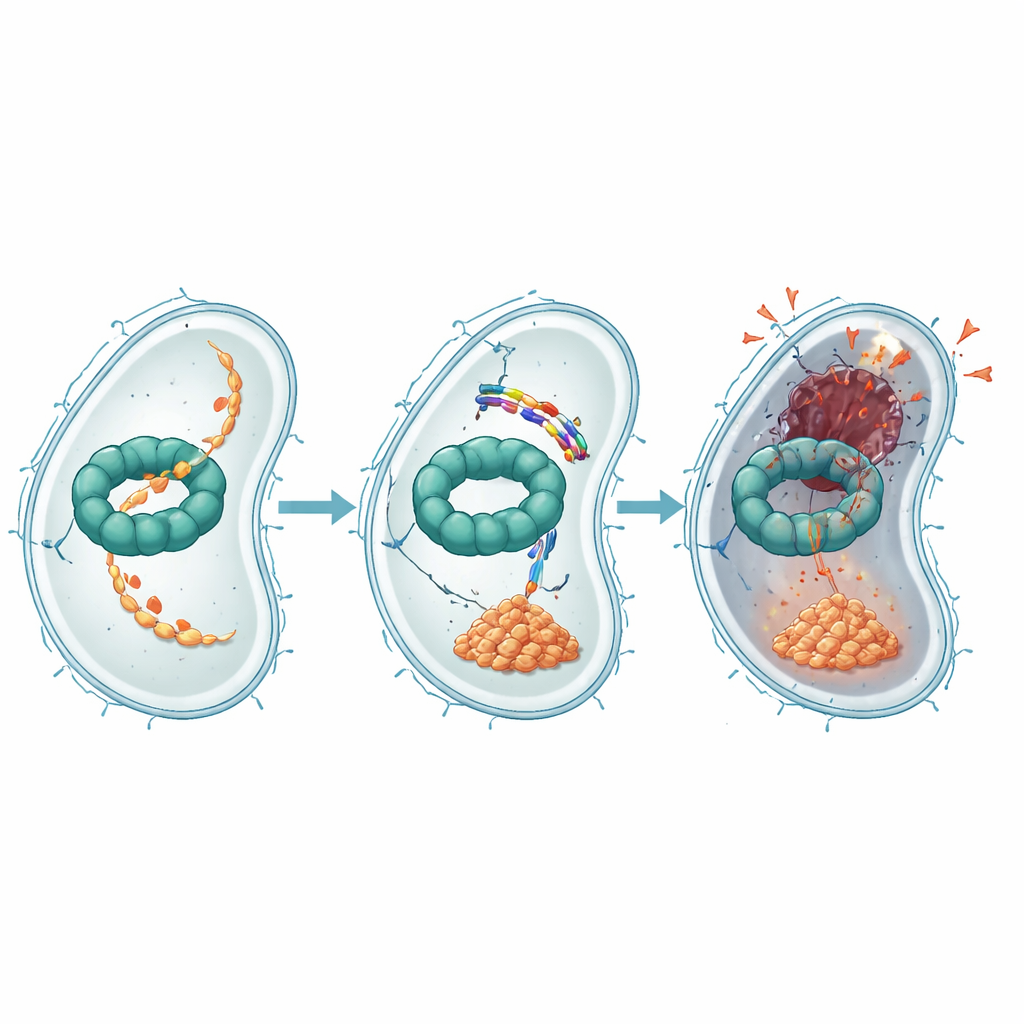
Qué significa esto para combatir infecciones resistentes
En términos sencillos, este estudio muestra que un pequeño péptido derivado de lombriz puede infiltrarse en bacterias y atascar una máquina interna vital, mientras también perfora su membrana externa. Al bloquear el sistema que normalmente elimina un regulador clave del estrés, EWAMP-R atrapa a E. coli en un estado autodestructivo en el que no puede reparar adecuadamente su ADN. Incluso cuando las bacterias desarrollan cierta resistencia, la pagan con un crecimiento más lento o con una capacidad reducida para causar enfermedad. En conjunto, estos hallazgos sugieren que EWAMP-R, y las moléculas modeladas a partir de él, podrían inspirar una nueva generación de agentes antibacterianos de múltiples frentes que sean más difíciles de sortear para los patógenos.
Cita: Wu, Y., Tang, H., Hao, P. et al. Identification of intracellular target of antimicrobial peptide EWAMP-R in bacteria. Commun Biol 9, 564 (2026). https://doi.org/10.1038/s42003-026-09822-5
Palabras clave: péptidos antimicrobianos, resistencia a los antibióticos, respuesta al estrés bacteriano, control de calidad de proteínas, proteasa ClpX