Clear Sky Science · it
Identificazione del bersaglio intracellulare del peptide antimicrobico EWAMP-R nei batteri
Perché una minuscola molecola del verme conta per i superbatteri
Con l’aumento della resistenza agli antibiotici, i medici stanno esaurendo gli strumenti per fermare le infezioni batteriche pericolose. Questo studio esplora un’alternativa promettente: una piccola molecola naturale, un peptide antimicrobico chiamato EWAMP-R, originariamente isolata da lombrichi. I ricercatori dimostrano che questo peptide fa più che forare le membrane batteriche: sabota anche una macchina interna cruciale di cui i batteri hanno bisogno per sopravvivere, indicando una nuova classe di trattamenti che potrebbe restare avanti alla resistenza.
Un attacco su due fronti contro i batteri
La maggior parte degli antibiotici agisce mirando a un singolo processo vitale, come la costruzione della parete cellulare. I batteri possono alla fine evolversi per aggirare questi attacchi. I peptidi antimicrobici, però, spesso colpiscono i batteri su più fronti. Era già stato dimostrato che EWAMP-R danneggia le membrane batteriche e innesca una forma di morte programmata nei batteri, in qualche modo simile all’apoptosi nelle cellule umane. In questo studio, il gruppo ha voluto capire cosa accade all’interno della cellula dopo che EWAMP-R ha oltrepassato la membrana — in particolare, quale molecola interna prende di mira e come quell’interazione porta alla morte batterica.
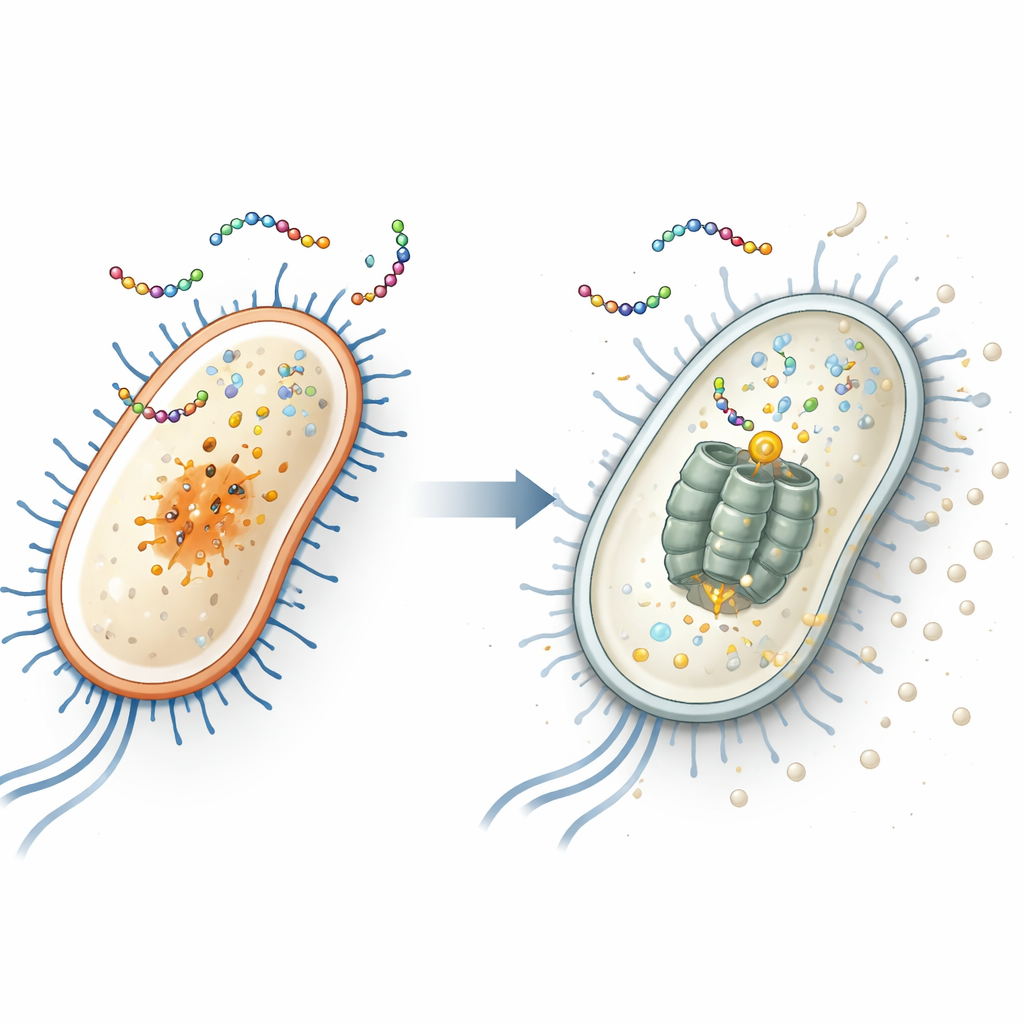
Scoprire il bersaglio nascosto all’interno di E. coli
Per individuare il bersaglio intracellulare del peptide, i ricercatori hanno esposto ripetutamente due batteri comuni — Escherichia coli (un batterio intestinale che comprende ceppi pericolosi) e Staphylococcus aureus (una causa frequente di infezioni cutanee e ospedaliere) — a EWAMP-R fino a che non sono emersi ceppi resistenti. Sequenziando i genomi di questi sopravvissuti, hanno scoperto che gli E. coli resistenti portavano una mutazione specifica in un gene chiamato clpX. Questo gene codifica una parte di un “trituratore” molecolare che degrada proteine danneggiate o regolatorie. Quando hanno ricreato esattamente questa mutazione con l’editing genico CRISPR, E. coli è diventato meno sensibile a EWAMP-R, implicando con forza che la proteina ClpX sia il bersaglio interno principale del peptide.
Bloccando il trituratore proteico batterico
Ulteriori esperimenti hanno mostrato come EWAMP-R interferisca con questa macchina proteica. Utilizzando test di legame, docking computazionale e simulazioni molecolari, gli autori hanno scoperto che il peptide si inserisce in una regione di ClpX che normalmente lega e utilizza ATP, la valuta energetica della cellula, per alimentare la degradazione delle proteine. Quando EWAMP-R si lega a questa sede, limita i cambiamenti conformazionali necessari a ClpX per funzionare correttamente e riduce drasticamente la sua attività dipendente da ATP. Una proteina importante normalmente processata dal sistema ClpX è un frammento di un regolatore master chiamato LexA, che controlla la risposta SOS batterica — un programma di stress che attiva geni per la riparazione del DNA. Quando ClpX è bloccato, questo frammento di LexA si accumula e continua a reprimere i geni SOS, impedendo una corretta riparazione del DNA e spingendo la cellula verso una morte irreversibile simile all’apoptosi.
Cambiamenti imprevisti nello stile di vita batterico
Il gruppo ha anche scoperto che la resistenza comporta un costo. Gli E. coli che avevano evoluto resistenza a EWAMP-R non solo portavano la mutazione di clpX, ma producevano anche flagelli insolitamente lunghi e numerosi — le code con cui i batteri si muovono. I profili di espressione genica hanno confermato che i geni correlati ai flagelli risultavano fortemente iperattivati. Studi precedenti suggeriscono che batteri “iperflagellati” di questo tipo possono effettivamente diventare meno capaci di aderire ai tessuti dell’ospite e più visibili al sistema immunitario, riducendo potenzialmente la loro abilità di causare malattia. In S. aureus, al contrario, la resistenza non si è concentrata su ClpX. Le cellule resistenti hanno invece rallentato il loro metabolismo, in particolare nelle vie degli amminoacidi e di altri mattoni di costruzione, crescendo più lentamente e probabilmente diventando meno aggressive come patogeni.
Progettare peptidi più intelligenti per medicine future
Poiché EWAMP-R sia perturba le membrane batteriche sia blocca una macchina proteica interna, costringe i batteri ad adattarsi su più livelli contemporaneamente — una sfida energeticamente onerosa. Pochi farmaci esistenti mirano direttamente al sistema ClpX, e questo lavoro lo identifica come un nuovo punto debole nei batteri che infettano gli esseri umani. Gli autori delineano modi per affinare ulteriormente EWAMP-R, come modificare specifici amminoacidi per legare ClpX più saldamente o aiutare il peptide a attraversare più facilmente membrane batteriche diverse, e usare blocchi costitutivi non naturali per renderlo più stabile nell’organismo. 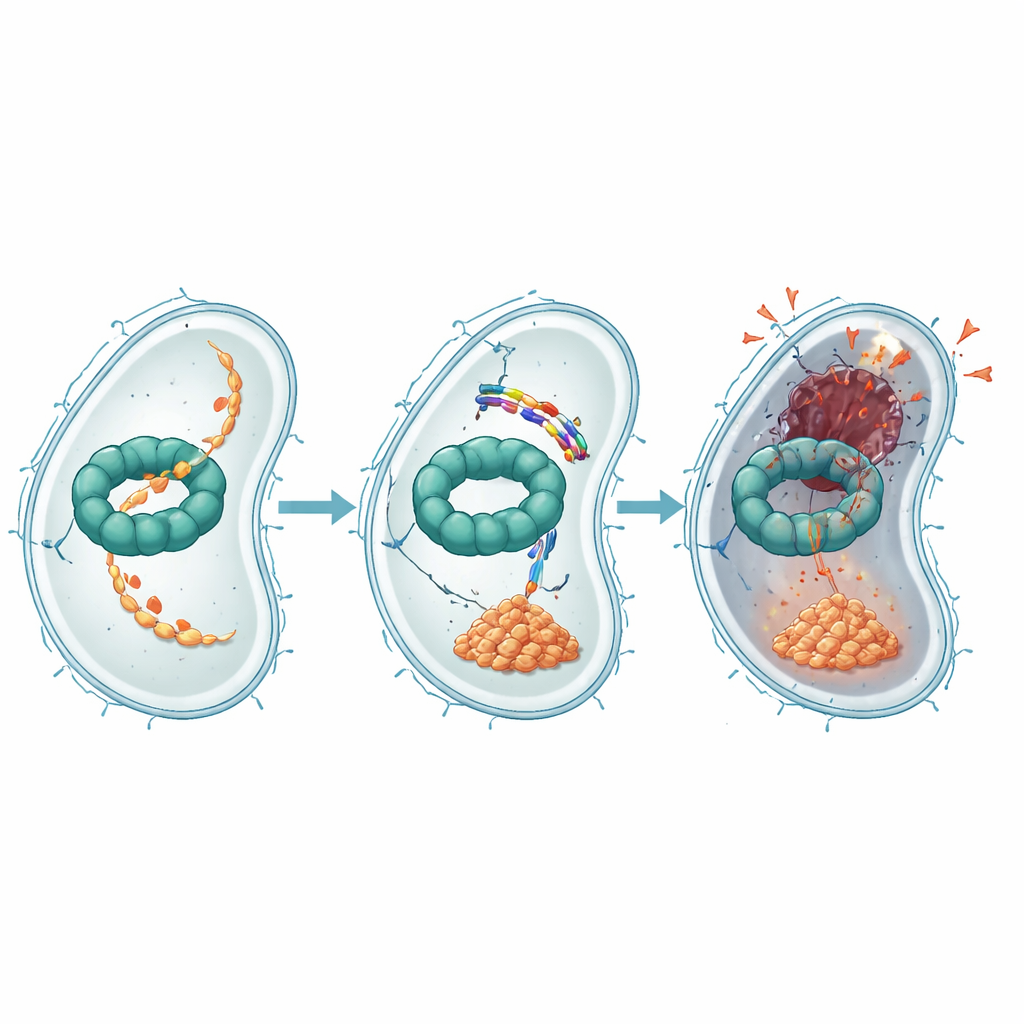
Cosa significa questo per la lotta contro le infezioni resistenti
In termini semplici, questo studio dimostra che un piccolo peptide derivato da un verme può infiltrarsi nei batteri e bloccare una macchina interna vitale, oltre a creare fori nel loro involucro esterno. Bloccando il sistema che normalmente elimina un regolatore chiave dello stress, EWAMP-R intrappola E. coli in uno stato autodistruttivo in cui non può riparare adeguatamente il proprio DNA. Anche quando i batteri evolvono una certa resistenza, pagano un prezzo in crescita più lenta o in una potenziale ridotta capacità di causare malattia. Nel complesso, questi risultati suggeriscono che EWAMP-R e molecole modellate su di esso potrebbero ispirare una nuova generazione di agenti antibatterici multipli che è più difficile per i patogeni superare.
Citazione: Wu, Y., Tang, H., Hao, P. et al. Identification of intracellular target of antimicrobial peptide EWAMP-R in bacteria. Commun Biol 9, 564 (2026). https://doi.org/10.1038/s42003-026-09822-5
Parole chiave: peptidi antimicrobici, resistenza agli antibiotici, risposta allo stress batterico, controllo della qualità delle proteine, proteasi ClpX