Clear Sky Science · nl
Identificatie van het intracellulaire doelwit van het antimicrobieel peptide EWAMP-R in bacteriën
Waarom een klein wormmolecuul belangrijk is voor superbugs
Naarmate antibioticaresistentie toeneemt, raken artsen uitgeput in hun mogelijkheden om gevaarlijke bacteriële infecties te bestrijden. Deze studie onderzoekt een veelbelovend alternatief: een klein natuurlijk molecuul, een antimicrobieel peptide genaamd EWAMP-R, oorspronkelijk gevonden in regenwormen. De onderzoekers tonen aan dat dit peptide meer doet dan alleen gaten prikken in bacteriële membranen—het saboteert ook een cruciale interne machine die bacteriën nodig hebben om te overleven, wat wijst op een nieuwe klasse behandelingen die mogelijk voorop kunnen blijven lopen ten opzichte van resistentie.
Een aanval op twee fronten tegen bacteriën
De meeste antibiotica werken door een enkel vitaal proces te remmen, zoals de opbouw van de celwand. Bacteriën kunnen uiteindelijk om deze aanvallen heen evolueren. Antimicrobiële peptiden raken bacteriën echter vaak op meerdere fronten. Van EWAMP-R was al aangetoond dat het bacteriële membranen beschadigt en een soort geprogrammeerde celdood in bacteriën activeert, enigszins vergelijkbaar met apoptose in menselijke cellen. In deze studie wilde het team begrijpen wat er in de cel gebeurt nadat EWAMP-R het membraan is gepasseerd—specifiek welk intern molecuul het target is en hoe die interactie leidt tot bacteriële dood.
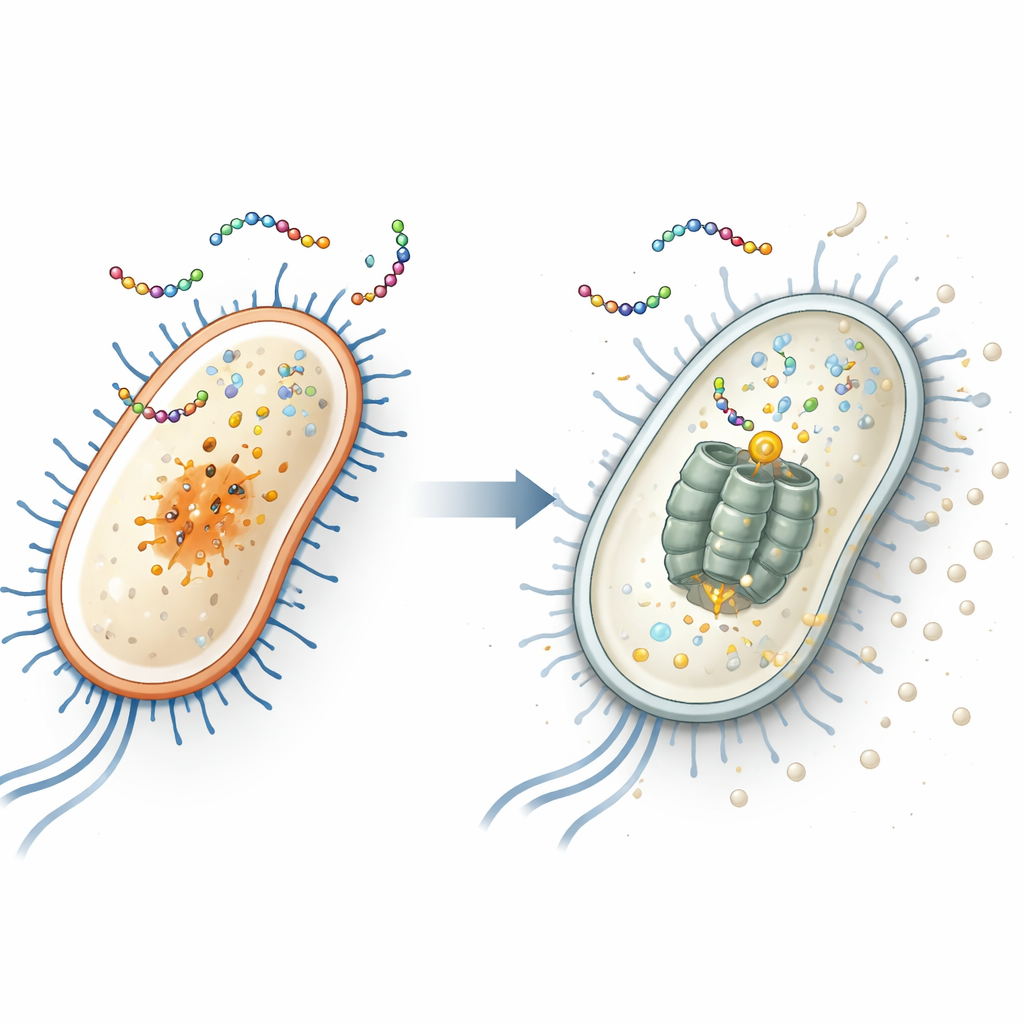
Het verborgen doelwit binnen E. coli opsporen
Om het intracellulaire doelwit van het peptide te achterhalen, zetten de onderzoekers herhaaldelijk twee veelvoorkomende bacteriën—Escherichia coli (een darmbacterie met ook gevaarlijke stammen) en Staphylococcus aureus (een frequent veroorzaker van huid- en ziekenhuisinfecties)—bloot aan EWAMP-R totdat resistente stammen verschenen. Door het genoom van deze overlevenden te sequencen, vonden ze dat resistente E. coli een specifieke mutatie droegen in een gen genaamd clpX. Dit gen codeert voor een deel van een moleculaire “versnipperaar” die beschadigde of regulerende eiwitten afbreekt. Wanneer ze deze exacte mutatie opnieuw inbrachten met CRISPR-genbewerking, werd E. coli minder gevoelig voor EWAMP-R, wat sterk suggereert dat het ClpX-eiwit het belangrijkste intracellulaire doelwit van het peptide is.
De bacteriële eiwitversnipperaar blokkeren
Verdere experimenten toonden aan hoe EWAMP-R deze eiwitmachine verstoort. Met bindingsproeven, computerdocking en moleculaire simulaties vonden de auteurs dat het peptide zich nestelt in een regio van ClpX die normaal ATP bindt en gebruikt—de energievaluta van de cel—om eiwitten af te breken. Wanneer EWAMP-R hier bindt, beperkt het de noodzakelijke vormveranderingen van ClpX en vermindert het sterk de ATP-gedreven activiteit. Een belangrijk eiwit dat normaal door het ClpX-systeem wordt verwerkt is een fragment van een hoofdregelaar genaamd LexA, die de bacteriële SOS-respons controleert—een stressprogramma dat DNA-herstelgenen inschakelt. Wanneer ClpX wordt geblokkeerd, hoopt dit LexA-fragment zich op en blijft het de SOS-genen onderdrukken, waardoor correct DNA-herstel uitblijft en de cel naar een onomkeerbare, apoptose-achtige dood wordt geduwd.
Onverwachte veranderingen in bacteriële levensstijl
Het team ontdekte ook dat resistentie een prijs heeft. E. coli die resistentie tegen EWAMP-R hadden ontwikkeld droegen niet alleen de clpX-mutatie, maar produceerden ook uitzonderlijk lange en talrijke flagellen—de zweepachtige staarten die bacteriën gebruiken om te bewegen. Genexpressiepatronen bevestigden dat flagella-gerelateerde genen sterk overactief waren. Eerder werk suggereert dat dergelijke “hyperflagellate” bacteriën juist minder goed aan gastweefsels kunnen hechten en beter zichtbaar worden voor het immuunsysteem, wat hun vermogen om ziekte te veroorzaken mogelijk vermindert. Bij S. aureus lag resistentie daarentegen niet bij ClpX. In plaats daarvan vertraagden resistente cellen hun stofwisseling, met name in aminozuur- en andere bouwsteenroutes, waardoor ze langzamer groeiden en waarschijnlijk minder agressief werden als pathogenen.
Slimmere peptiden ontwerpen voor toekomstige medicijnen
Omdat EWAMP-R zowel bacteriële membranen verstoort als een interne eiwitmachine blokkeert, dwingt het bacteriën om zich op meerdere niveaus tegelijk aan te passen—een energetisch kostbare opgave. Weinig bestaande medicijnen richten zich rechtstreeks op het ClpX-systeem, en dit werk identificeert het als een nieuw zwak punt in bacteriën die mensen treffen. De auteurs schetsen manieren om EWAMP-R verder te verfijnen, zoals het aanpassen van specifieke aminozuren om beter aan ClpX te binden of het peptide gemakkelijker door verschillende bacteriële membranen te laten glippen, en het gebruik van niet-natuurlijke bouwstenen om het stabieler in het lichaam te maken. 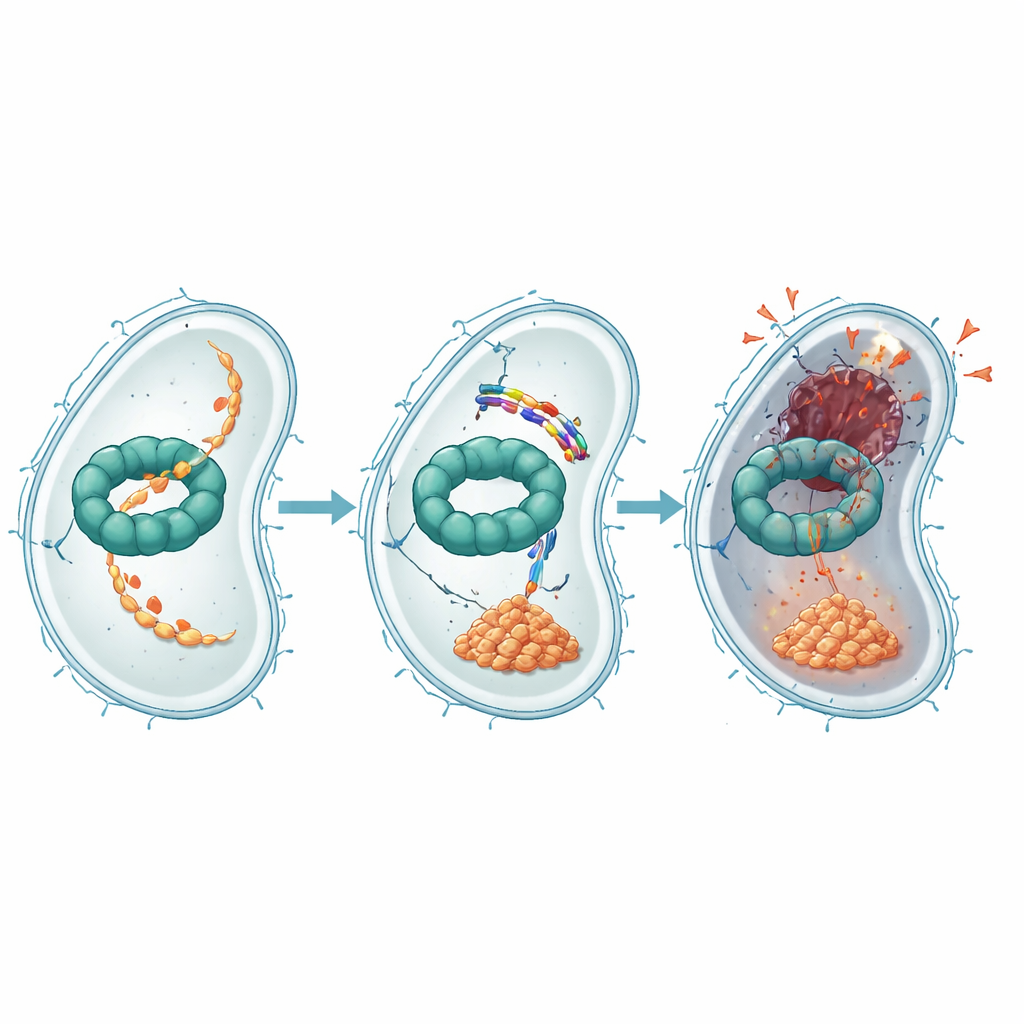
Wat dit betekent voor de strijd tegen resistente infecties
In eenvoudige bewoordingen toont deze studie aan dat een klein peptide afkomstig van een worm bacteriën kan binnensluipen en een essentiële interne machine kan blokkeren, terwijl het ook gaten slaat in hun buitenste laag. Door het systeem te blokkeren dat normaal een belangrijke stressregelaar opruimt, houdt EWAMP-R E. coli gevangen in een zelfdestructieve staat waarin het zijn DNA niet goed kan herstellen. Zelfs wanneer bacteriën enige resistentie ontwikkelen, betalen ze daar een prijs voor in langzamere groei of mogelijk verminderde ziektelijkheid. Gezamenlijk suggereren deze bevindingen dat EWAMP-R, en moleculen die daarop zijn gebaseerd, een nieuwe generatie veelzijdige antibacteriële middelen kunnen inspireren die moeilijker door ziekteverwekkers te slim af zijn.
Bronvermelding: Wu, Y., Tang, H., Hao, P. et al. Identification of intracellular target of antimicrobial peptide EWAMP-R in bacteria. Commun Biol 9, 564 (2026). https://doi.org/10.1038/s42003-026-09822-5
Trefwoorden: antimicrobiële peptiden, antibioticaresistentie, bacteriële stressrespons, eiwitkwaliteitscontrole, ClpX-protease