Clear Sky Science · sv
Identifiering av intracellulärt mål för det antimikrobiella peptidet EWAMP-R i bakterier
Varför en liten maskmolekyl spelar roll för superbakterier
När antibiotikaresistensen ökar har kliniker färre verktyg för att stoppa farliga bakterieinfektioner. Denna studie undersöker ett lovande alternativ: en liten naturlig molekyl, ett antimikrobiellt peptid kallat EWAMP-R, ursprungligen funnet i daggmaskar. Forskarna visar att peptiden gör mer än att bara göra hål i bakteriens membran — den saboterar också en central intern maskin som bakterier behöver för att överleva, vilket pekar mot en ny klass av behandlingar som kan ligga steget före resistens.
En tvåfrontsattack mot bakterier
De flesta antibiotika verkar genom att rikta in sig på en enda vital process, till exempel byggandet av cellväggen. Bakterier kan så småningom utveckla motstånd mot dessa angrepp. Antimikrobiella peptider träffar emellertid ofta bakterier på flera fronter. EWAMP-R hade redan visats skada bakteriella membran och utlösa en form av programmerad celldöd i bakterier, något som liknar apoptos i humana celler. I denna studie ville teamet förstå vad som händer inne i cellen efter att EWAMP-R tagit sig förbi membranet — närmare bestämt vilken intern molekyl den riktar in sig på och hur den interaktionen leder till bakteriedöd.
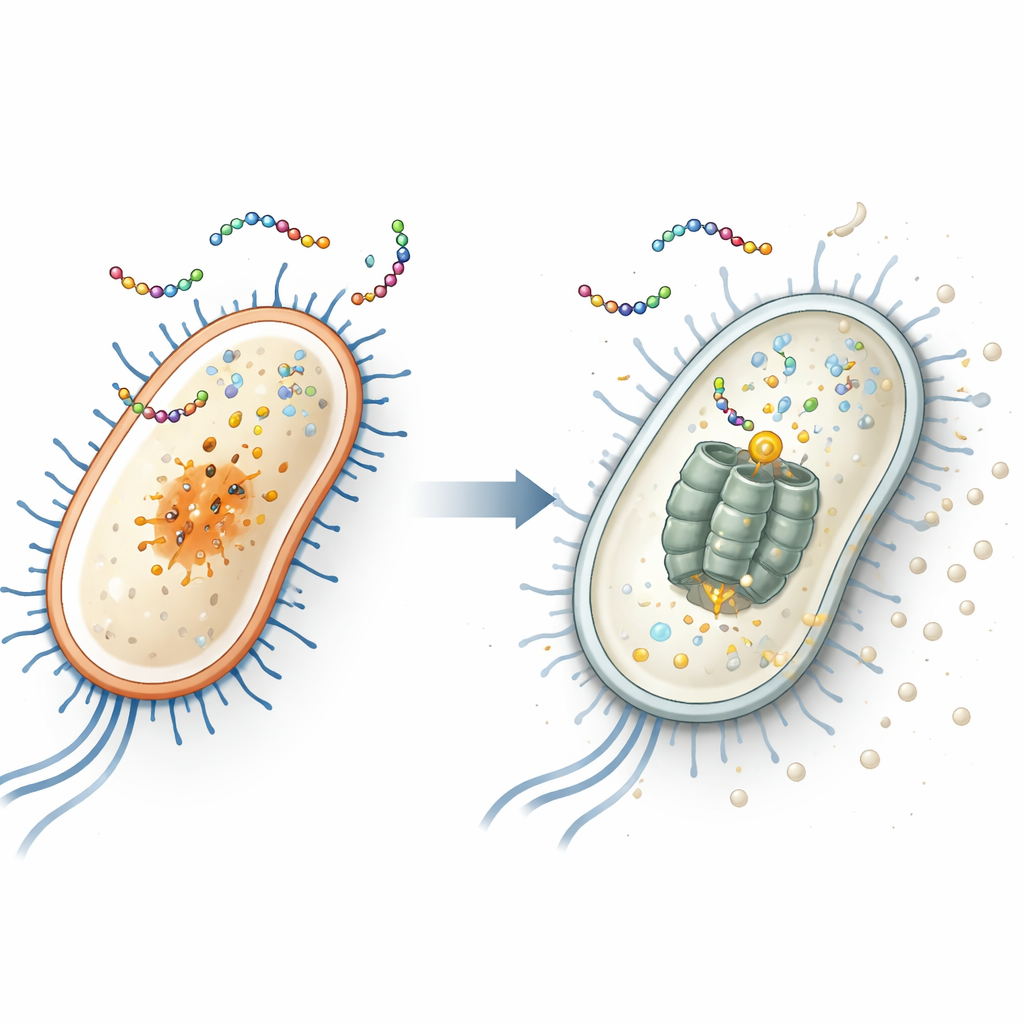
Att hitta det dolda målet inne i E. coli
För att avslöja peptidens intracellulära mål exponerade forskarna upprepade gånger två vanliga bakterier — Escherichia coli (en tarmbakterie som inkluderar farliga stammar) och Staphylococcus aureus (en vanlig orsak till hud- och sjukhusinfektioner) — för EWAMP-R tills resistenta stammar uppstod. Genom att sekvensbestämma genomerna hos dessa överlevare fann de att resistenta E. coli bar en specifik mutation i en gen kallad clpX. Denna gen kodar för en del av en molekylär ”malare” som bryter ner skadade eller reglerande proteiner. När de återskapade denna exakta mutation med CRISPR-genredigering blev E. coli mindre känslig för EWAMP-R, vilket starkt antyder att ClpX-proteinet är peptidens viktiga interna mål.
Att sätta sig i vägen för bakteriens proteinslaktare
Ytterligare experiment visade hur EWAMP-R stör denna proteinmaskin. Med bindningstester, datorbaserad dockning och molekylära simuleringar fann författarna att peptiden lägger sig i en region av ClpX som normalt binder och använder ATP, cellens energivaluta, för att driva proteinbrytning. När EWAMP-R binder här begränsar det de formförändringar ClpX behöver för att fungera korrekt och minskar kraftigt dess ATP-drivna aktivitet. Ett viktigt protein som normalt bearbetas av ClpX-systemet är en fragment av en huvudregulator kallad LexA, som styr det bakteriella SOS-svaret — ett stressprogram som slår på DNA-reparationsgener. När ClpX blockeras byggs detta LexA-fragment upp och fortsätter att undertrycka SOS-generna, vilket förhindrar korrekt DNA-reparation och driver cellen mot en irreversibel, apoptosliknande död.
Oväntade förändringar i bakteriellt livsstil
Teamet upptäckte också att resistens bär en kostnad. E. coli som utvecklat resistens mot EWAMP-R bar inte bara clpX-mutation utan producerade också ovanligt långa och många flageller — de piskliknande svansar bakterier använder för att röra sig. Genuttrycksmönster bekräftade att flagellrelaterade gener var starkt överaktiva. Tidigare arbete antyder att sådana ”hyperflagellerade” bakterier faktiskt kan bli mindre benägna att fästa vid värdvävnader och mer synliga för immunsystemet, vilket potentiellt minskar deras förmåga att orsaka sjukdom. I S. aureus, däremot, centrerade inte resistens kring ClpX. Istället saktade resistenta celler ner sin metabolism, särskilt i aminosyra- och andra byggblocksbanor, växte långsammare och blev sannolikt mindre aggressiva som patogener.
Designa smartare peptider för framtida läkemedel
Eftersom EWAMP-R både stör bakteriella membran och stoppar en intern proteinmaskin tvingar det bakterier att anpassa sig på flera nivåer samtidigt — en energimässigt kostsam utmaning. Få befintliga läkemedel riktar sig direkt mot ClpX-systemet, och detta arbete identifierar det som en ny svag punkt i bakterier som påverkar människor. Författarna skisserar sätt att vidare förfina EWAMP-R, såsom att justera specifika aminosyror för att binda ClpX hårdare eller hjälpa peptiden att smidigare ta sig genom olika bakteriella membran, samt att använda icke-naturliga byggstenar för att göra den mer stabil i kroppen. 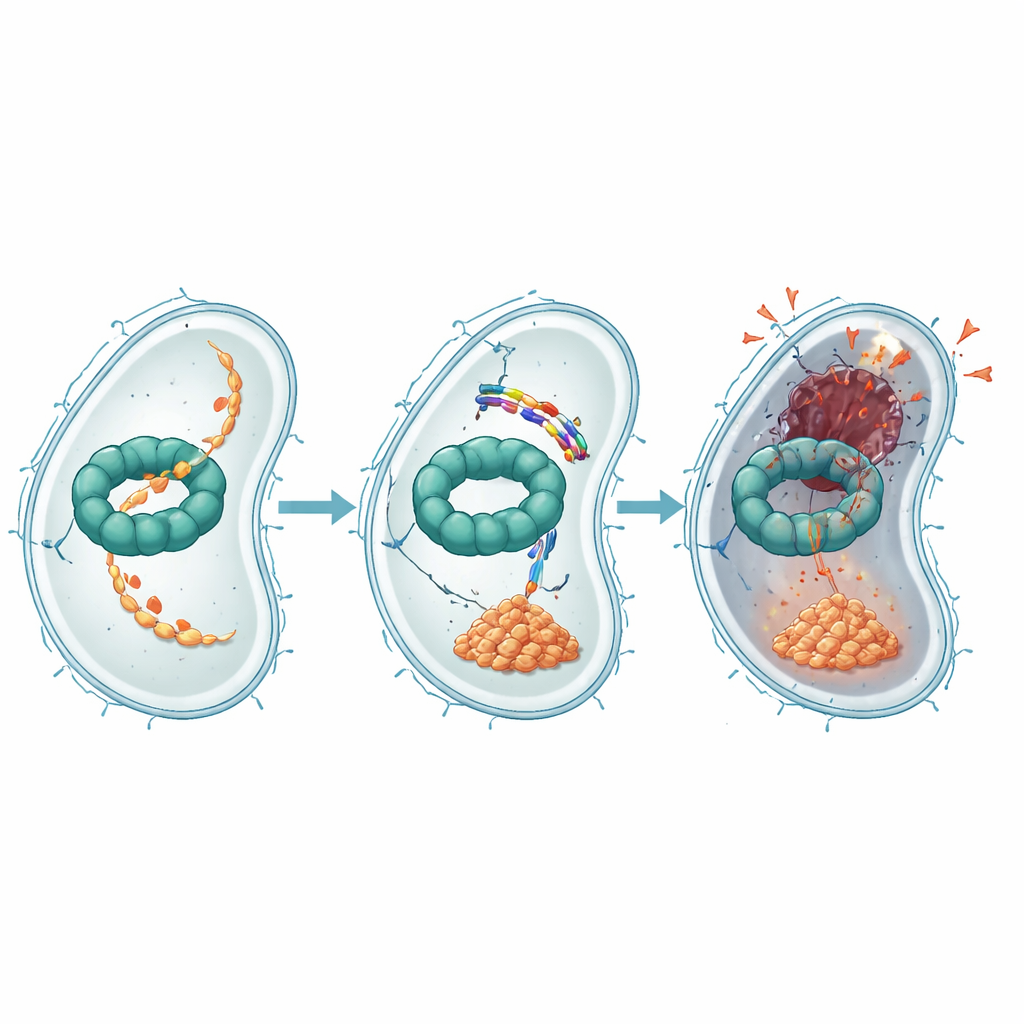
Vad detta betyder för kampen mot resistenta infektioner
I enkla ordalag visar denna studie att ett litet maskhärlett peptid kan smyga in i bakterier och blockera en livsviktig intern maskin, samtidigt som det skapar hål i deras yttre hölje. Genom att blockera systemet som normalt rensar en nyckelstressregulator fångar EWAMP-R E. coli i ett självförstörande tillstånd där den inte kan reparera sitt DNA på rätt sätt. Även när bakterier utvecklar viss resistens betalar de ett pris i långsammare tillväxt eller potentiellt minskad förmåga att orsaka sjukdom. Tillsammans tyder dessa fynd på att EWAMP-R, och molekyler baserade på den, skulle kunna inspirera en ny generation av mångsidiga antibakteriella medel som är svårare för patogener att överlista.
Citering: Wu, Y., Tang, H., Hao, P. et al. Identification of intracellular target of antimicrobial peptide EWAMP-R in bacteria. Commun Biol 9, 564 (2026). https://doi.org/10.1038/s42003-026-09822-5
Nyckelord: antimikrobiella peptider, antibiotikaresistens, bakteriellt stressvar, protein-kvalitetskontroll, ClpX-proteas