Clear Sky Science · pt
Identificação do alvo intracelular do peptídeo antimicrobiano EWAMP-R em bactérias
Por que uma molécula minúscula de minhoca importa para os supermicróbios
À medida que a resistência a antibióticos aumenta, os médicos ficam sem maneiras eficazes de deter infecções bacterianas perigosas. Este estudo explora uma alternativa promissora: uma pequena molécula natural, um peptídeo antimicrobiano chamado EWAMP-R, originalmente encontrada em minhocas. Os pesquisadores mostram que esse peptídeo faz mais do que perfurar membranas bacterianas — ele também sabota uma máquina interna crucial que as bactérias precisam para sobreviver, apontando para uma nova classe de tratamentos que podem se manter à frente da resistência.
Um ataque em duas frentes às bactérias
A maioria dos antibióticos age visando um único processo vital, como a construção da parede celular. As bactérias podem eventualmente evoluir para contornar esses ataques. Peptídeos antimicrobianos, porém, frequentemente atingem as bactérias em múltiplas frentes. Já se sabia que o EWAMP-R danificava membranas bacterianas e desencadeava um tipo de morte programada nas bactérias, algo semelhante à apoptose em células humanas. Neste estudo, a equipe procurou entender o que acontece dentro da célula depois que o EWAMP-R atravessa a membrana — especificamente, qual molécula interna ele mira e como essa interação leva à morte bacteriana.
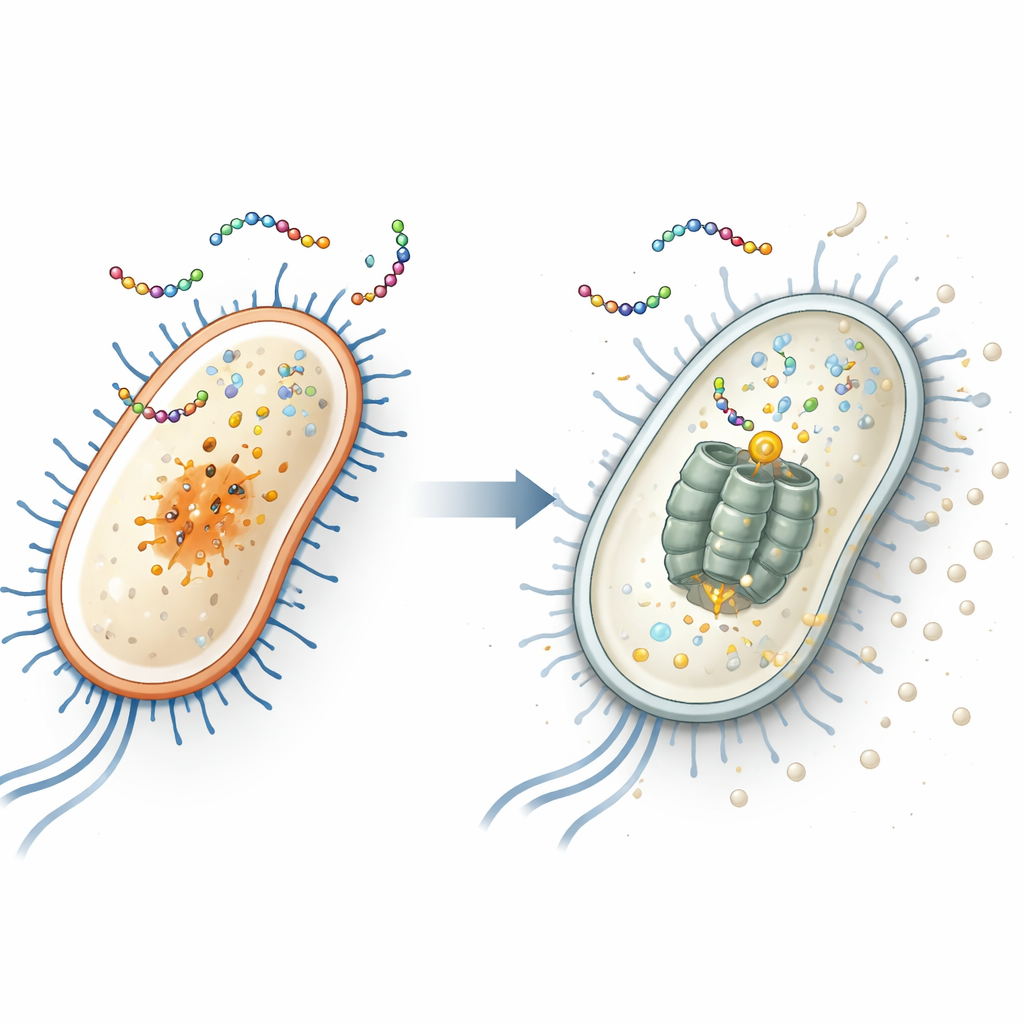
Encontrando o alvo oculto dentro de E. coli
Para descobrir o alvo interno do peptídeo, os pesquisadores expuseram repetidamente duas bactérias comuns — Escherichia coli (uma bactéria intestinal que inclui cepas perigosas) e Staphylococcus aureus (causa frequente de infecções de pele e hospitalares) — ao EWAMP-R até que surgissem cepas resistentes. Ao sequenciar os genomas desses sobreviventes, descobriram que E. coli resistente carregava uma mutação específica em um gene chamado clpX. Esse gene codifica parte de um “triturador” molecular que degrada proteínas danificadas ou regulatórias. Quando recriaram essa mutação exata usando edição de genes por CRISPR, a E. coli tornou-se menos sensível ao EWAMP-R, implicando fortemente que a proteína ClpX é o principal alvo interno do peptídeo.
Travando o triturador de proteínas bacteriano
Experimentos adicionais mostraram como o EWAMP-R interfere nessa máquina proteica. Usando testes de ligação, acoplamento por computador e simulações moleculares, os autores observaram que o peptídeo se aloja em uma região da ClpX que normalmente se liga e utiliza ATP, a moeda de energia celular, para impulsionar a degradação de proteínas. Quando o EWAMP-R se liga ali, ele restringe as mudanças conformacionais que a ClpX precisa para funcionar corretamente e reduz acentuadamente sua atividade dependente de ATP. Uma proteína importante normalmente processada pelo sistema ClpX é um fragmento de um regulador mestre chamado LexA, que controla a resposta SOS bacteriana — um programa de estresse que ativa genes de reparo do DNA. Quando a ClpX é bloqueada, esse fragmento de LexA se acumula e continua a reprimir os genes da SOS, impedindo o reparo adequado do DNA e empurrando a célula para uma morte irreversível semelhante à apoptose.
Mudanças inesperadas no estilo de vida bacteriano
A equipe também descobriu que a resistência tem um custo. A E. coli que evoluiu resistência ao EWAMP-R não só carregava a mutação em clpX, como também produzia flagelos incomumente longos e numerosos — as caudas semelhantes a chicotes que as bactérias usam para se mover. Padrões de expressão gênica confirmaram que genes relacionados a flagelos estavam fortemente hiperativos. Trabalhos anteriores sugerem que bactérias “hiperflageladas” podem, na verdade, tornar-se menos capazes de aderir a tecidos do hospedeiro e mais visíveis ao sistema imune, potencialmente reduzindo sua capacidade de causar doença. Em S. aureus, por outro lado, a resistência não se centrou na ClpX. Em vez disso, as células resistentes desaceleraram seu metabolismo, particularmente em vias de aminoácidos e outros blocos de construção, crescendo mais lentamente e provavelmente tornando-se menos agressivas como patógenos.
Projetando peptídeos mais inteligentes para medicamentos futuros
Porque o EWAMP-R tanto perturba membranas bacterianas quanto trava uma máquina proteica interna, ele força as bactérias a se adaptarem em múltiplos níveis ao mesmo tempo — um desafio energeticamente custoso. Poucos medicamentos existentes miram diretamente o sistema ClpX, e este trabalho o identifica como uma nova vulnerabilidade em bactérias que afetam humanos. Os autores delineiam maneiras de refinar ainda mais o EWAMP-R, como ajustar aminoácidos específicos para ligar-se à ClpX com mais afinidade ou ajudar o peptídeo a atravessar mais facilmente membranas bacterianas diferentes, e usar blocos construtores não naturais para torná‑lo mais estável no corpo. 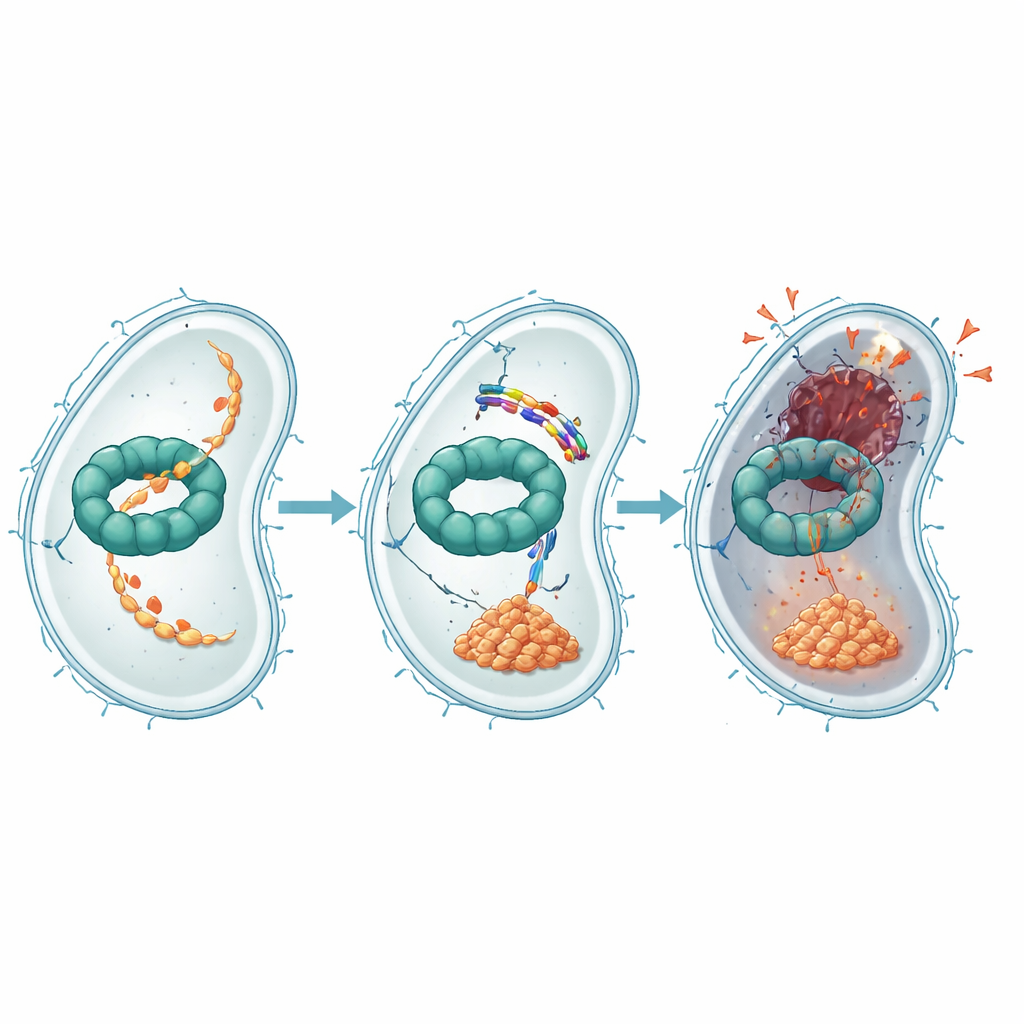
O que isso significa para combater infecções resistentes
Em termos simples, este estudo mostra que um pequeno peptídeo derivado de minhoca pode infiltrar-se nas bactérias e travar uma máquina interna vital, ao mesmo tempo em que perfura sua camada externa. Ao bloquear o sistema que normalmente elimina um regulador chave de estresse, o EWAMP-R prende a E. coli em um estado autodestrutivo onde não consegue reparar adequadamente seu DNA. Mesmo quando as bactérias evoluem alguma resistência, elas pagam um preço em crescimento mais lento ou potencial redução da capacidade de causar doença. Juntos, esses achados sugerem que o EWAMP-R, e moléculas modeladas a partir dele, podem inspirar uma nova geração de agentes antibacterianos multifacetados que são mais difíceis para os patógenos contornarem.
Citação: Wu, Y., Tang, H., Hao, P. et al. Identification of intracellular target of antimicrobial peptide EWAMP-R in bacteria. Commun Biol 9, 564 (2026). https://doi.org/10.1038/s42003-026-09822-5
Palavras-chave: peptídeos antimicrobianos, resistência a antibióticos, resposta ao estresse bacteriano, controle de qualidade de proteínas, protease ClpX