Clear Sky Science · de
Identifizierung des intrazellulären Zieles des antimikrobiellen Peptids EWAMP-R in Bakterien
Warum ein winziges Wurm-Molekül für Superkeime wichtig ist
Während die Antibiotikaresistenz zunimmt, gehen Ärzten die Mittel aus, um gefährliche bakterielle Infektionen zu stoppen. Diese Studie untersucht eine vielversprechende Alternative: ein kleines natürliches Molekül, ein antimikrobielles Peptid namens EWAMP-R, das ursprünglich in Regenwürmern entdeckt wurde. Die Forschenden zeigen, dass dieses Peptid mehr tut, als Löcher in bakterielle Membranen zu stechen — es sabotiert auch eine entscheidende interne Maschine, die Bakterien zum Überleben brauchen, und weist damit auf eine neue Klasse von Therapien hin, die der Resistenzentwicklung vorausbleiben könnten.
Ein Angriff auf zwei Fronten gegen Bakterien
Die meisten Antibiotika wirken, indem sie einen einzelnen lebenswichtigen Prozess angreifen, etwa den Aufbau der Zellwand. Bakterien können sich schließlich um diese Angriffe herum entwickeln. Antimikrobielle Peptide hingegen treffen Bakterien oft auf mehreren Ebenen. Man wusste bereits, dass EWAMP-R bakterielle Membranen schädigt und eine Art programmierter Zelltod in Bakterien auslöst, ähnlich der Apoptose bei menschlichen Zellen. In dieser Studie wollte das Team verstehen, was innerhalb der Zelle geschieht, nachdem EWAMP-R die Membran passiert hat — insbesondere, welches intrazelluläre Molekül es angreift und wie diese Interaktion zum bakteriellen Tod führt.
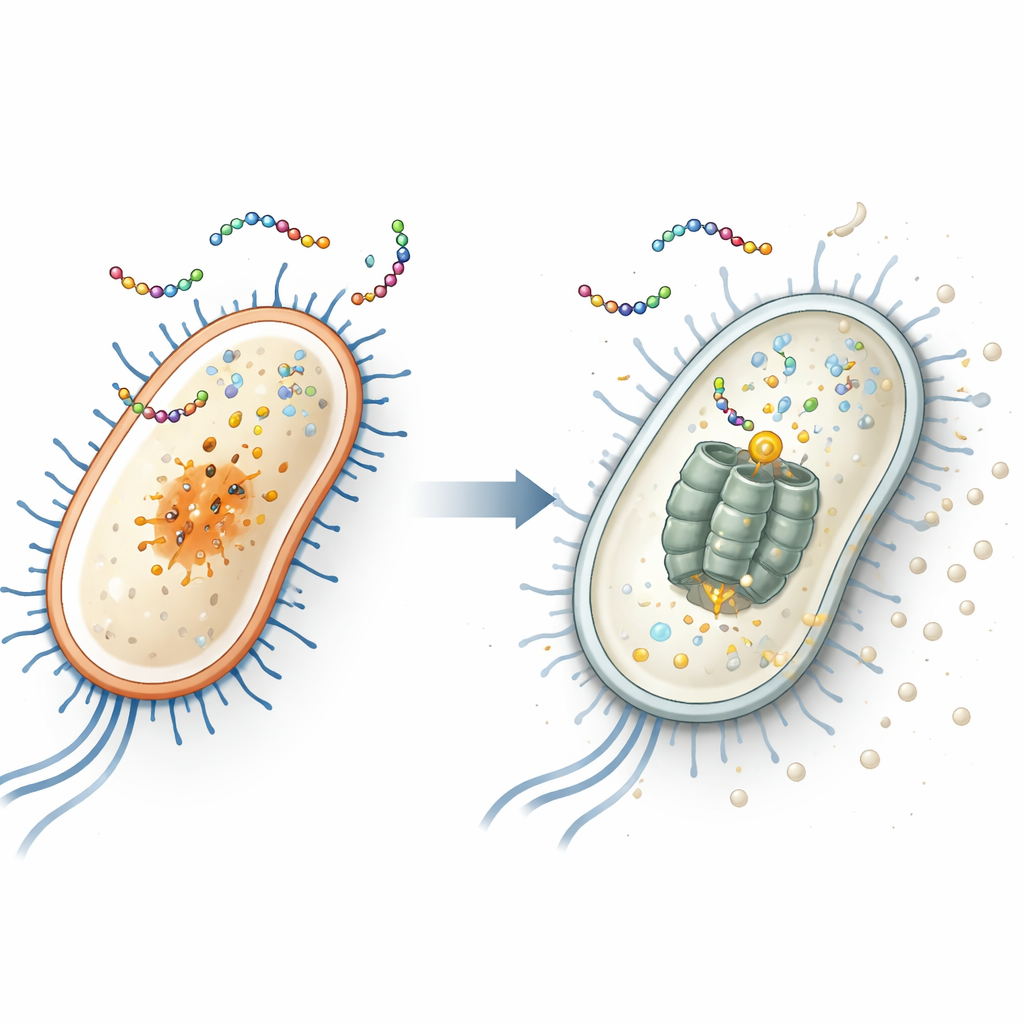
Das versteckte Ziel in E. coli finden
Um das intrazelluläre Ziel des Peptids aufzudecken, setzten die Forschenden wiederholt zwei verbreiteten Bakterien — Escherichia coli (ein Darmbakterium, das auch gefährliche Stämme einschließt) und Staphylococcus aureus (eine häufige Ursache für Haut- und Krankenhausinfektionen) — EWAMP-R aus, bis resistente Stämme auftraten. Durch Sequenzierung der Genome dieser Überlebenden stellten sie fest, dass resistente E. coli eine spezifische Mutation im Gen clpX trugen. Dieses Gen kodiert einen Teil eines molekularen „Schredders“, der beschädigte oder regulatorische Proteine abbaut. Als sie diese genaue Mutation mithilfe von CRISPR-Geneditierung rekonstruierten, wurden E. coli weniger empfindlich gegenüber EWAMP-R, was stark darauf hindeutet, dass das Protein ClpX das zentrale intrazelluläre Ziel des Peptids ist.
Den bakteriellen Protein-Schredder lahmlegen
Weitere Experimente zeigten, wie EWAMP-R diese Proteinanlage stört. Mithilfe von Bindungstests, rechnerischem Docking und molekularen Simulationen fanden die Autorinnen und Autoren heraus, dass sich das Peptid in eine Region von ClpX einlagert, die normalerweise ATP bindet und nutzt — die Energiemünze der Zelle — um den Proteinabbau anzutreiben. Wenn EWAMP-R hier bindet, schränkt es die für die Funktion nötigen Konformationsänderungen von ClpX ein und reduziert dessen ATP-getriebene Aktivität stark. Ein wichtiges Substrat, das normalerweise vom ClpX-System verarbeitet wird, ist ein Fragment eines Masterregulators namens LexA, der die bakterielle SOS-Antwort steuert — ein Stressprogramm, das DNA-Reparaturgene einschaltet. Wenn ClpX blockiert ist, häuft sich dieses LexA-Fragment an und hält die SOS-Gene weiter heruntergefahren, verhindert eine ordnungsgemäße DNA-Reparatur und treibt die Zelle in einen irreversiblen, apoptosisähnlichen Tod.
Unerwartete Veränderungen im bakteriellen Lebensstil
Das Team entdeckte außerdem, dass die Resistenz mit Kosten verbunden ist. E. coli, die Resistenz gegen EWAMP-R entwickelt hatten, trugen nicht nur die clpX-Mutation, sondern bildeten ungewöhnlich viele und sehr lange Geißeln — die peitschenartigen Anhängsel, mit denen Bakterien sich bewegen. Expressionsmuster der Gene bestätigten, dass Geißel-assoziierte Gene stark überaktiv waren. Frühere Arbeiten legen nahe, dass solche „hypergeißelten“ Bakterien tatsächlich weniger fähig sein könnten, an Wirtsgewebe haften zu bleiben, und eher vom Immunsystem erkannt werden, was ihre Fähigkeit, Krankheiten zu verursachen, potenziell verringert. Bei S. aureus hingegen zentrierte sich die Resistenz nicht auf ClpX. Stattdessen verlangsamten resistente Zellen ihren Stoffwechsel, insbesondere in Aminosäure- und anderen Bausteinwegen, wuchsen langsamer und wurden vermutlich als Erreger weniger aggressiv.
Schlauer konstruierte Peptide für künftige Medikamente
Da EWAMP-R sowohl bakterielle Membranen stört als auch eine interne Proteinanlage blockiert, zwingt es Bakterien dazu, sich auf mehreren Ebenen gleichzeitig anzupassen — eine energetisch kostspielige Herausforderung. Nur wenige bestehende Wirkstoffe zielen direkt auf das ClpX-System ab, und diese Arbeit identifiziert es als eine neue Schwachstelle in für den Menschen relevanten Bakterien. Die Autorinnen und Autoren skizzieren Wege, EWAMP-R weiter zu verfeinern, etwa durch Modifikation bestimmter Aminosäuren, um stärker an ClpX zu binden oder das Peptid leichter durch unterschiedliche bakterielle Membranen schlüpfen zu lassen, sowie durch den Einsatz nicht-natürlicher Bausteine, um seine Stabilität im Körper zu erhöhen. 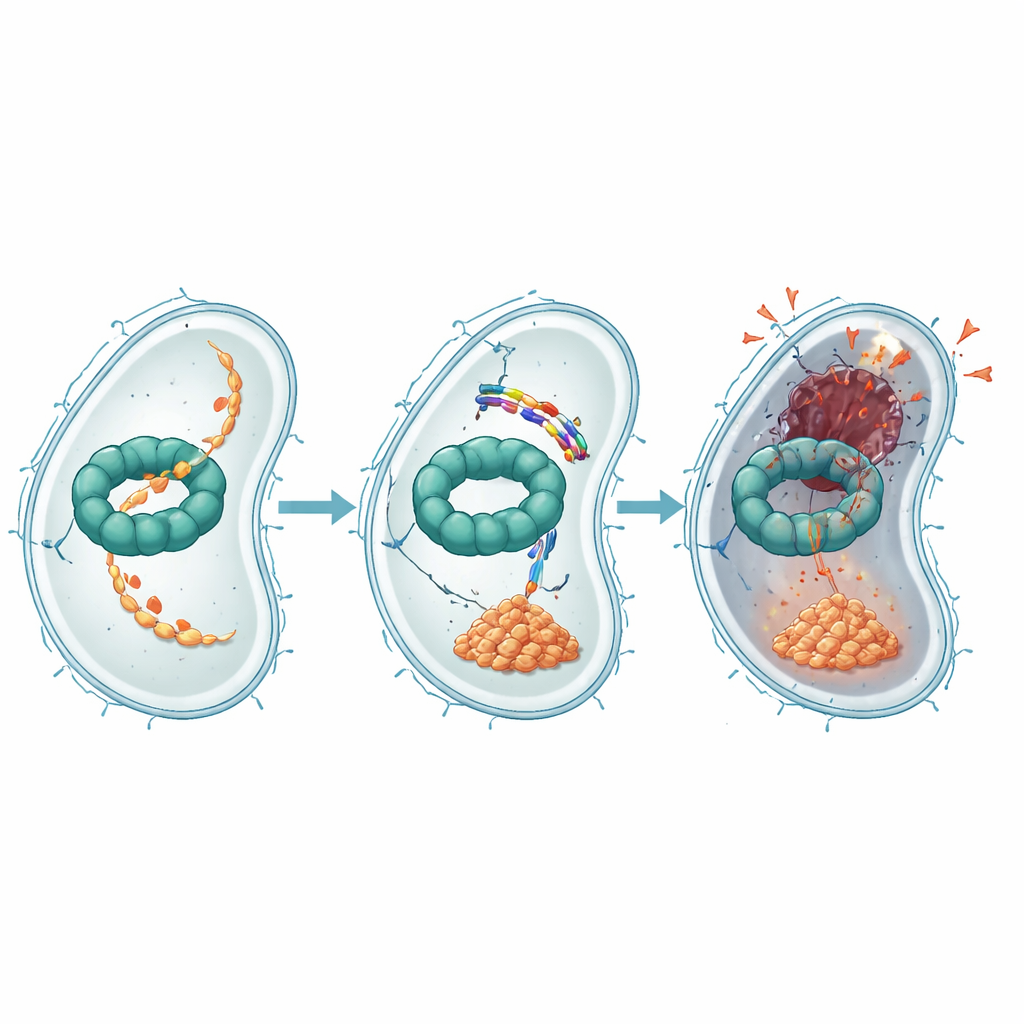
Was das für den Kampf gegen resistente Infektionen bedeutet
Vereinfacht gesagt zeigt diese Studie, dass ein kleines, wurm-abgeleitetes Peptid in Bakterien eindringen und eine lebenswichtige interne Maschine blockieren kann, während es gleichzeitig Löcher in ihre äußere Hülle schlägt. Indem es das System blockiert, das normalerweise einen wichtigen Stressregulator entfernt, fängt EWAMP-R E. coli in einem selbstzerstörerischen Zustand, in dem die Zellen ihre DNA nicht richtig reparieren können. Selbst wenn Bakterien eine gewisse Resistenz entwickeln, zahlen sie dafür mit langsameren Wachstum oder einer potenziell verringerten Fähigkeit, Krankheiten zu verursachen. Zusammengenommen deuten diese Befunde darauf hin, dass EWAMP-R und darauf basierende Moleküle eine neue Generation von vielseitig wirkenden antibakteriellen Mitteln inspirieren könnten, die für Krankheitserreger schwerer zu umgehen sind.
Zitation: Wu, Y., Tang, H., Hao, P. et al. Identification of intracellular target of antimicrobial peptide EWAMP-R in bacteria. Commun Biol 9, 564 (2026). https://doi.org/10.1038/s42003-026-09822-5
Schlüsselwörter: antimikrobielle Peptide, Antibiotikaresistenz, bakterielle Stressantwort, Proteinqualitätskontrolle, ClpX-Protease