Clear Sky Science · zh
ATP酶 N-乙基马来酰亚胺敏感因子介导的钙依赖性融合孔闭合与内吞作用
细胞如何重用它们的分泌包裹
每一秒,你的大脑细胞、分泌激素的细胞和免疫细胞都在释放微小的化学信使包裹,然后迅速将已排空的囊泡回收以便重复使用。这种快速的“发出-回收”系统保持了思维、血糖调节和免疫功能的顺畅运行。本文章所述研究揭示了这个回收环节中的一个缺失环节:允许货物外泄的小开口——“融合孔”——如何以及何时闭合,从而使空囊泡能被拉回细胞内。
一个分泌囊泡的生命周期
许多细胞通过将神经递质、激素或炎症分子等信号装入类似气泡的包裹(囊泡)进行通讯。这些囊泡移动到细胞表面并短暂与外膜结合,形成一个充满水的小通道——融合孔,通过它们的内容物得以释放。通常,囊泡并不完全融合,而是执行“吻别-跑开”(kiss-and-run):它接触膜,打开一个短暂的孔以释放货物,然后孔闭合,囊泡被回收以供再次使用。这个快速且节能的循环对时机要求极高:融合孔打开时间太短,信号无法充分释放;若不能及时闭合,回收系统便会停滞。 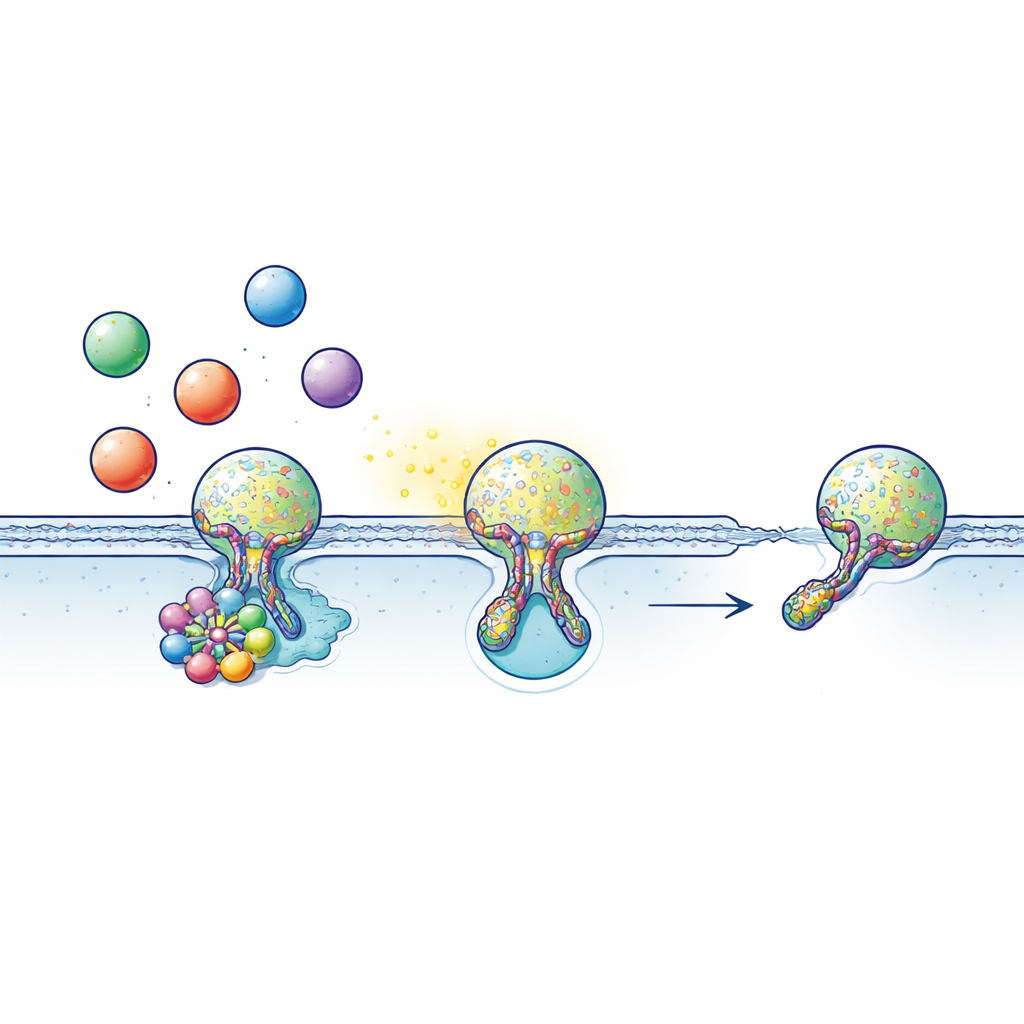
位于孔处的分子马达
囊泡的融合与回收由一些抓住囊泡与细胞膜并像拉绳一样将它们拉拢在一起的蛋白驱动。这些“SNARE”蛋白形成紧密束缚,将两层膜拉到一起并打开融合孔。新研究聚焦于另一种蛋白——NSF,这是一种利用ATP(细胞的能量)来拆解已完成任务的SNARE束的酶。研究者结合对细胞表面积变化敏感的电学记录和活体共焦显微成像,观察了大鼠肾上腺分泌细胞、感觉神经元和胰岛素分泌细胞中单个囊泡的融合与回收。通过化学抑制NSF或基因性地去除它,他们检验了NSF的活性是否不仅在融合前必要,也在随后闭合融合孔时发挥作用。
当NSF停摆,融合孔拒绝闭合
在正常情况下,这些细胞中的许多囊泡经历吻别-跑开:融合孔打开,保持一段短且确定的时间,然后闭合以便囊泡被拉回内部。当研究者用药物抑制NSF的ATP驱动活性或将其敲除时,观察到行为发生了显著变化。囊泡仍可到达膜并打开孔,但完成孔闭合的事件比例明显减少。相反,囊泡常常保持附着于表面,且孔比平时打开的时间长得多。这种改变伴随着若干类型内吞作用的强烈减慢或阻滞,包括极快的、较慢的以及“超过回收”(overshoot)——回收额外膜片的情况。可快速释放的囊泡库也补充得更慢,表明融合孔闭合与囊泡回收是紧密相连的步骤。
钙引导的回收选择
细胞可以通过钙依赖或非钙依赖的方式回收囊泡。研究团队在背根神经节的感觉神经元中比较了这两条途径。在存在钙的情况下,抑制NSF同样减慢了囊泡融合后的回收,表明NSF对钙触发的回收至关重要。但当科学家采用一种诱发无钙、电压驱动回收模式的刺激方案时,NSF抑制剂影响甚微。该对比提示细胞将NSF作为处理高强度钙信号(例如剧烈信号传递期间)的专用工具,而保留一条独立的、非钙依赖通路来支持较安静的背景回收。
NSF如何牵线
为更接近观察NSF在融合孔处的作用,研究者构建了一个荧光传感器:当SNARE蛋白形成束时会发光,束被拆解时亮度减弱。在刺激期间,他们看到这些信号在囊泡融合处出现,然后在孔闭合并囊泡回收的几秒内消退。当NSF被阻断时,发光信号持续时间更长,表明SNARE束保持组装状态而未被拆散。结合对ATP酶活性的测量——NSF的“燃料燃烧”行为——这些结果支持这样一个图景:NSF在融合的后期主动拆解SNARE束。这种拆解似乎有助于收紧并最终使融合孔闭合,完成吻别-回收循环。 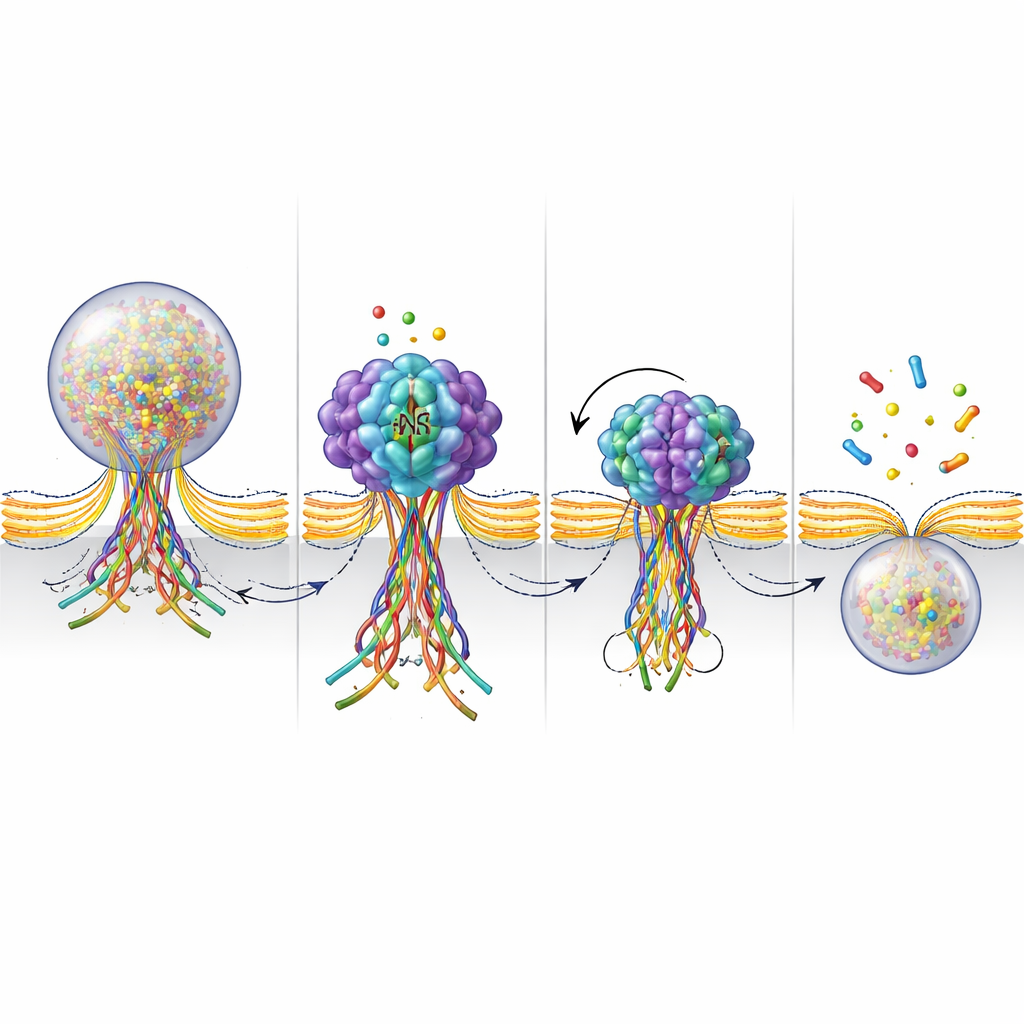
这对健康与疾病为何重要
该研究通过证明NSF的能量驱动行为是闭合融合孔并触发囊泡回收的核心开关,将这一已知的分子马达与细胞间通信的精细调控联系起来。在分泌激素的细胞、肾上腺嗜铬细胞和某些神经元中,这一机制确保囊泡在钙激增时能够被快速且可靠地重复利用。如果NSF功能受损,融合孔可能无法正确闭合,回收变慢,细胞可能难以跟上需求,从而可能影响应激反应、疼痛传导或血糖调节。理解这一闭合步骤为探究囊泡回收微小缺陷如何导致神经或内分泌疾病提供了新途径,并突出了NSF作为未来潜在治疗靶点的意义。
引用: Wang, Y., Ma, S., Song, S. et al. ATPase N-ethylmaleimide-sensitive factor mediated calcium dependent fusion pore closure and endocytosis. Commun Biol 9, 495 (2026). https://doi.org/10.1038/s42003-026-09743-3
关键词: 囊泡回收, 融合孔, 内吞作用, 钙信号, NSF ATP酶