Clear Sky Science · de
ATPase N-ethylmaleimide-sensitiver Faktor vermittelt kalziumabhängigen Verschluss der Fusionspore und Endozytose
Wie Zellen ihre sekretorischen Pakete wiederverwenden
Sekunde für Sekunde entlassen Ihre Gehirnzellen, hormonfreisetzenden Zellen und Immunzellen winzige Pakete chemischer Botenstoffe und nehmen die entleerten Pakete rasch zur Wiederverwendung wieder auf. Dieses schnelle Versand‑und‑Recycling-System hält Denken, Blutzuckerregulation und Immunantworten in Gang. Die Studie hinter diesem Artikel enthüllt ein fehlendes Puzzlestück dieses Recyclingprozesses: wie die kleine Öffnung, die den Frachtstoff herauslässt – die „Fusionspore“ – erkennt, wann und wie sie schließen muss, damit das leere Paket wieder in die Zelle zurückgezogen werden kann.
Der Lebenszyklus eines sekretorischen Pakets
Viele Zellen kommunizieren, indem sie Signale wie Neurotransmitter, Hormone oder entzündliche Moleküle in blasige Pakete, sogenannte Vesikel, verpacken. Diese Vesikel bewegen sich zur Zelloberfläche und verbinden sich für kurze Zeit mit der Außenmembran, wobei ein winziger wassergefüllter Kanal – die Fusionspore – entsteht, durch den ihr Inhalt entweicht. Häufig verschmelzen die Vesikel nicht vollständig, sondern führen ein „Kuss‑und‑Lauf“‑Verhalten aus: Sie berühren die Oberfläche, öffnen eine Pore nur lange genug, um ihre Ladung freizugeben, dann schließt die Pore und das Vesikel wird zur Wiederverwendung zurückgewonnen. Dieser schnelle, ökonomische Zyklus hängt entscheidend vom Timing ab: Öffnet sich die Fusionspore zu kurz, kommt zu wenig Signal heraus; gelingt das Schließen nicht, gerät das Recycling ins Stocken. 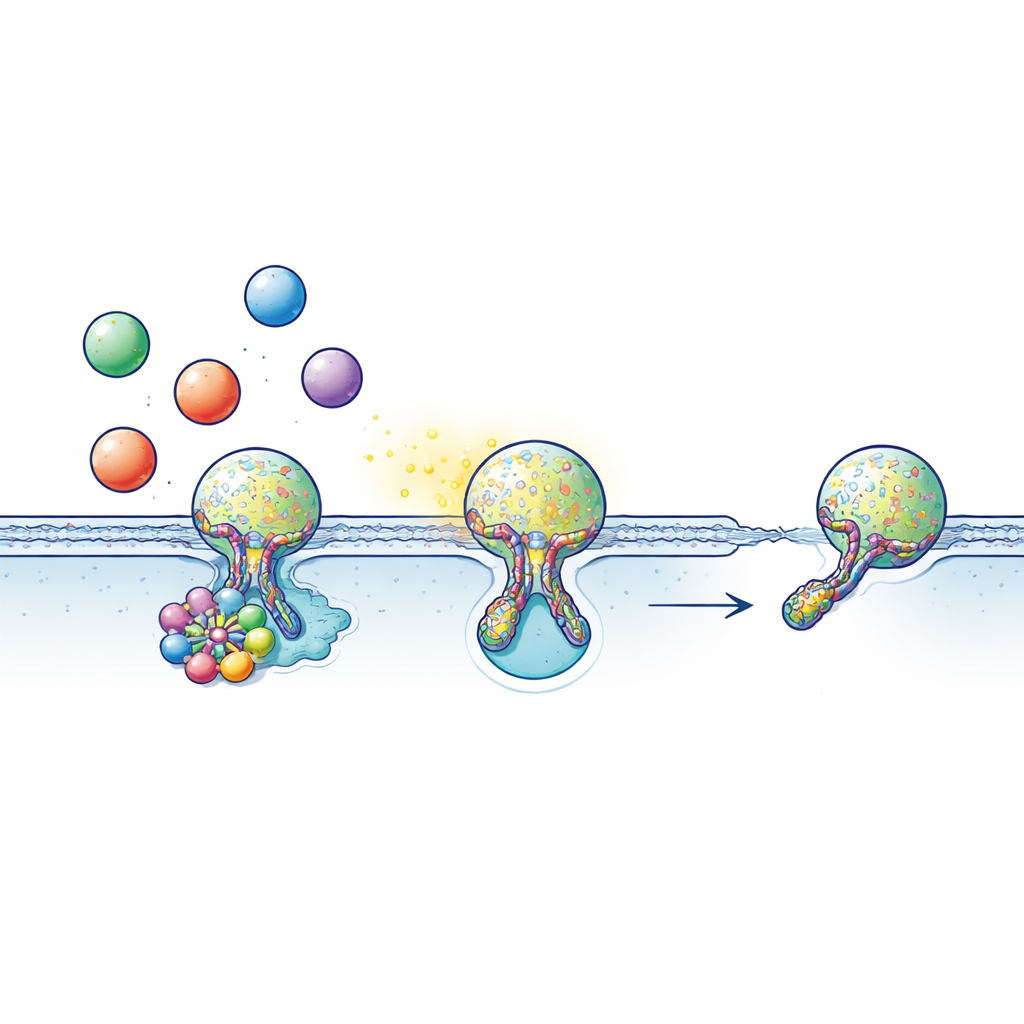
Ein molekularer Motor an der Pore
Vesikelfusion und -rückgewinnung werden von Proteinen angetrieben, die das Vesikel und die Zellmembran packen und wie an einer Kordel zusammenziehen. Diese „SNARE“‑Proteine bilden enge Bündel, die die beiden Membranen zusammenbringen und die Fusionspore öffnen. Die neue Studie konzentriert sich auf ein weiteres Protein, NSF, ein Enzym, das Energie aus ATP – dem Treibstoff der Zelle – nutzt, um SNARE‑Bündel wieder auseinanderzunehmen, nachdem sie ihre Arbeit getan haben. Mithilfe elektrischer Aufzeichnungen, die empfindlich auf Änderungen der Zelloberfläche reagieren, kombiniert mit Live‑Konfokalmikroskopie, beobachteten die Autoren einzelne Vesikel beim Verschmelzen und bei der Rückgewinnung in Ratten‑Nebenieren‑hormonfreisetzenden Zellen, sensorischen Neuronen und insulinproduzierenden Zellen. Durch chemische Blockade von NSF oder genetisches Entfernen konnten sie prüfen, ob dessen Aktivität nicht nur vor der Fusion, sondern auch für das anschließende Schließen der Pore notwendig ist.
Wenn NSF stockt, verweigern Poren das Schließen
Unter normalen Bedingungen durchlaufen viele Vesikel in diesen Zellen das Kuss‑und‑Lauf‑Verhalten: Die Fusionspore öffnet sich, bleibt für eine kurze, gut definierte Zeit offen und schließt dann, sodass das Vesikel wieder nach innen gezogen werden kann. Als die Forscher die ATP‑getriebene Aktivität von NSF mit Wirkstoffen hemmten oder das Protein ausschalteten, beobachteten sie eine auffällige Verhaltensänderung. Vesikel erreichten weiterhin die Membran und Poren konnten sich öffnen, doch ein deutlich geringerer Anteil der Ereignisse schloss die Pore vollständig. Stattdessen blieben Vesikel häufig an der Oberfläche angeheftet, mit Poren, die sehr viel länger offen blieben als üblich. Diese Änderung ging einher mit einer starken Verlangsamung oder Blockade mehrerer Formen der Endozytose, einschließlich sehr schneller, langsamer und der sogenannten „Overshoot“‑Rückgewinnung, bei der zusätzlich Membran zurückgenommen wird. Der Pool an Vesikeln, die für eine schnelle Freisetzung bereitstanden, wurde ebenfalls langsamer wieder aufgefüllt, was zeigt, dass Pore‑Verschluss und Vesikel‑Recycling eng miteinander verknüpfte Schritte sind.
Kalziumgesteuerte Recycling‑Entscheidungen
Zellen können Vesikel sowohl kalziumabhängig als auch kalziumunabhängig recyceln. In sensorischen Neuronen des dorsalen Wurzelganglions verglich das Team diese beiden Wege. In Gegenwart von Kalzium verlangsamte die Blockade von NSF erneut die Rückgewinnung nach Vesikelfusion, was darauf hinweist, dass NSF für das kalziumgetriggerte Recycling essenziell ist. Als die Wissenschaftler jedoch ein Stimulationsmuster verwendeten, das einen kalziumfreien, spannungsgetriebenen Recyclingmodus hervorruft, zeigten NSF‑Blocker kaum Wirkung. Dieser Unterschied deutet darauf hin, dass Zellen NSF als spezialisiertes Werkzeug für mit Kalzium verknüpfte Aktivitätsausbrüche reservieren – etwa bei intensiver Signalübertragung –, während ein separater, kalziumunabhängiger Weg leisere, Hintergrund‑Recyclingaufgaben übernimmt.
Wie NSF die Fäden zieht
Um NSFs Rolle an der Fusionspore näher zu beleuchten, konstruierten die Forscher einen fluoreszenten Sensor, der aufleuchtet, wenn SNARE‑Proteine ein Bündel bilden, und wieder abdunkelt, wenn dieses Bündel auseinandergezogen wird. Während der Stimulation sahen sie diese Signale an den Stellen erscheinen, an denen Vesikel verschmolzen, und innerhalb weniger Sekunden verblassen, wenn die Pore schloss und das Vesikel zurückgewonnen wurde. Wenn NSF blockiert war, hielt das aufleuchtende Signal deutlich länger an, was darauf hindeutet, dass das SNARE‑Bündel zusammengebaut blieb, statt demontiert zu werden. Zusammen mit Messungen der ATPase‑Aktivität – NSFs „Brennstoffverbrauch“ – stützen diese Ergebnisse das Bild, dass NSF aktiv SNARE‑Bündel in einer späten Phase der Fusion auseinanderbaut. Diese Demontage scheint zu helfen, die Pore zuzuziehen und schließlich abzutrennen, womit der Kuss‑und‑Lauf‑Zyklus abgeschlossen wird. 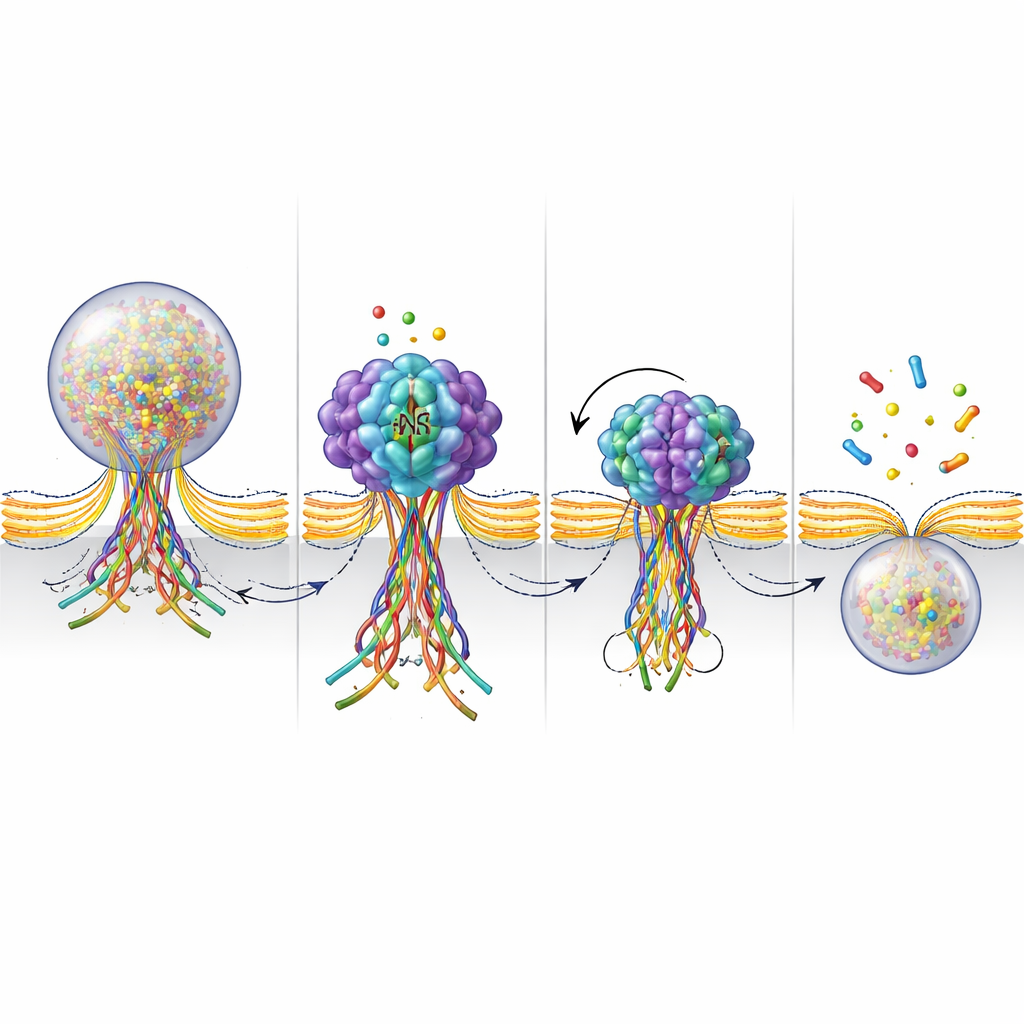
Warum das für Gesundheit und Krankheit wichtig ist
Indem gezeigt wird, dass NSFs energiegetriebene Aktion ein zentraler Schalter für das Schließen der Fusionspore und das Auslösen des Vesikel‑Recyclings ist, verknüpft diese Arbeit einen bekannten molekularen Motor mit der feinen Steuerung der zellulären Kommunikation. In hormonfreisetzenden Zellen, chromaffinen Nebennierenzellen und bestimmten Neuronen stellt dieser Mechanismus sicher, dass Vesikel bei Kalzium‑Anstiegen schnell und zuverlässig wiederverwendet werden können. Ist die NSF‑Funktion gestört, könnten Poren nicht richtig schließen, das Recycling verlangsamte sich und Zellen kämen mit der Nachfrage nicht mehr nach, was möglicherweise zu Problemen bei Stressreaktionen, Schmerzübertragung oder Blutzuckerregulation beiträgt. Das Verständnis dieses Schlussmechanismus eröffnet neue Wege, um zu erforschen, wie subtile Defekte im Vesikel‑Recycling neurologischen und endokrinen Erkrankungen zugrunde liegen könnten, und weist auf NSF als potenzielles Ziel für künftige therapeutische Strategien hin.
Zitation: Wang, Y., Ma, S., Song, S. et al. ATPase N-ethylmaleimide-sensitive factor mediated calcium dependent fusion pore closure and endocytosis. Commun Biol 9, 495 (2026). https://doi.org/10.1038/s42003-026-09743-3
Schlüsselwörter: Vesikel-Recycling, Fusionspore, Endozytose, Kalzium-Signalisierung, NSF-ATPase